Clear Sky Science · sv
Lipidskosmor i FGFR2c-medierad onkogen signalering via TRPA1-kanalens inblandning i pankreas ductalt adenokarcinom
Varför små öar i cellmembran spelar roll
Bukspottkörtelcancer är en av de dödligaste cancersjukdomarna, delvis därför att dess celler är ovanligt skickliga på att lossna från den ursprungliga tumören och invadera intilliggande vävnader. Denna studie undersöker små ”öar” i cancercellernas yttre hölje, sammansatta av kolesterol och lipider, och ställer en enkel fråga med stora konsekvenser: hjälper dessa öar till att slå på en tillväxtsignal som gör bukspottkörtelcancer mer aggressiv, och kan störning av dem bromsa processen?
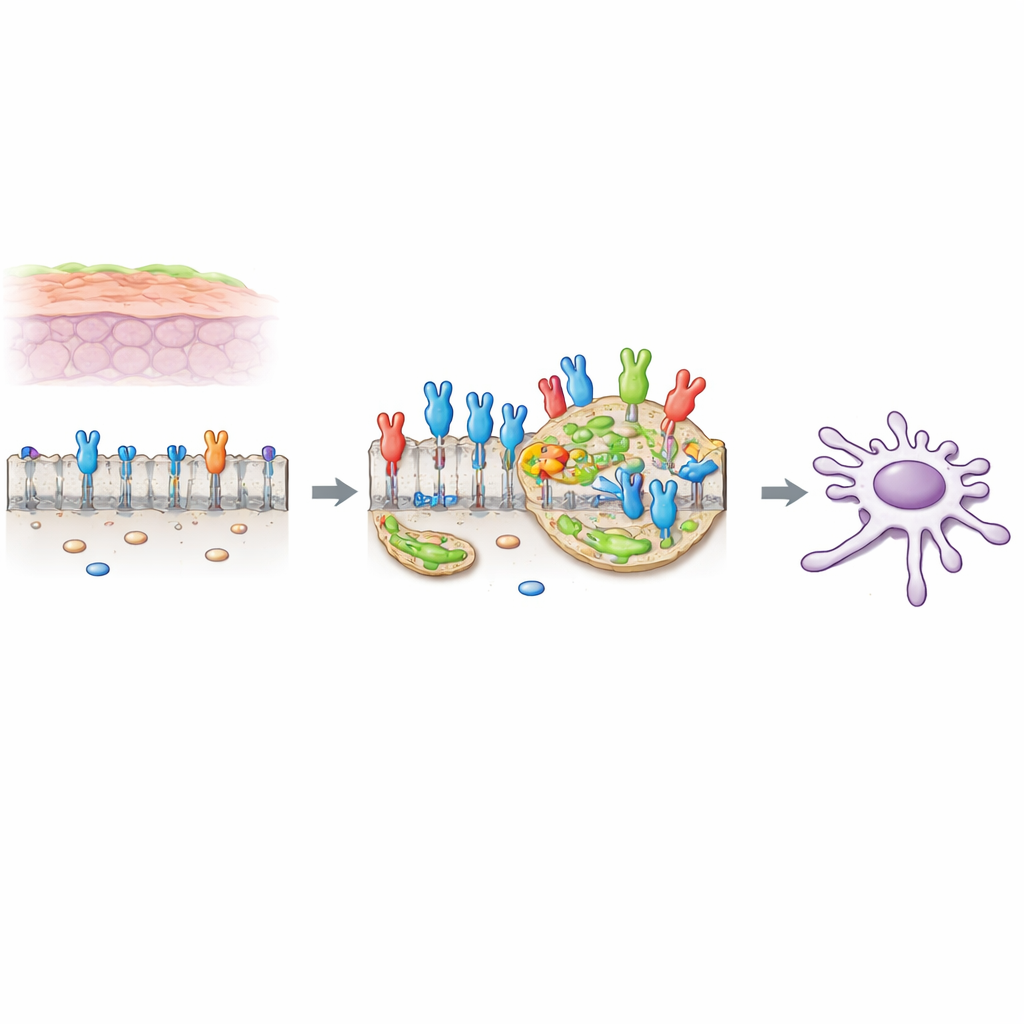
En cancerfrämjande strömbrytare på cellytan
Många celler bär strömbrytare på sin yta som svarar på tillväxtsignaler. En av dessa, kallad FGFR2c, är en variant som normalt finns i mer flexibla, rörliga celler, men den blir onormalt riklig i pankreas ductalt adenokarcinom (PDAC)-celler. När denna strömbrytare aktiveras av sin partnermolekyl i omgivningen driver den förändringar kända som epitelial–mesenkymal transition (EMT), vilket gör cellerna mindre fästa och mer rörliga och invasiva. Tidigare arbete från författarna visade att FGFR2c i PDAC-celler aktiverar en kaskad av interna budbärare som involverar proteinet PKCε och flera klassiska tillväxtvägar, vilket ökar cellöverlevnad, rörelse och invasion.
Kolesterolrika öar som signalförstärkare
Cellens yttre membran är inte enhetligt. Det innehåller små, kolesterolrika fläckar kallade lipidflottar, som fungerar som miniscenaer där signalmolekyler kan klustras och kommunicera mer effektivt. Forskarna fann att när FGFR2c aktiveras av sin externa signal flyttar mer av receptorn in i dessa lipidflottar. Genom att använda fluorescerande markörer och biokemisk fraktionering visade de att aktiverad FGFR2c koncentreras i dessa fläckar, medan dess fördelning utanför flottarna förändras från jämn till prickig, vilket stämmer med receptorgruppering på dessa öar.
Att bryta upp öarna försvagar canceregenskaper
För att testa om dessa lipidöar är nödvändiga för FGFR2c:s cancerfrämjande effekter använde teamet en förening (metyl-β-cyklodextrin) som selektivt avlägsnar kolesterol från membranet och destabiliserar lipidflottar utan att döda cellerna. I PDAC-celler med hög FGFR2c-halt minskade störning av flottarna kraftigt aktiveringen av viktiga signalmolekyler nedströms receptorn och dämpade EMT-programmet: gener och proteiner kopplade till ett rörligt, invasivt tillstånd minskade, medan epiteliala drag delvis återställdes. Samma behandling sänkte också nivåerna av invasionsrelaterade proteiner såsom MCL-1, SRC och matrixnedbrytande enzymer, och minskade cancercellernas förmåga att röra sig och penetrera ett gel som efterliknar omgivande vävnad. Celler med mycket lite FGFR2c visade nästan inget svar, vilket understryker hur central denna receptor–flotta-partnerskap är i dessa tumörer.
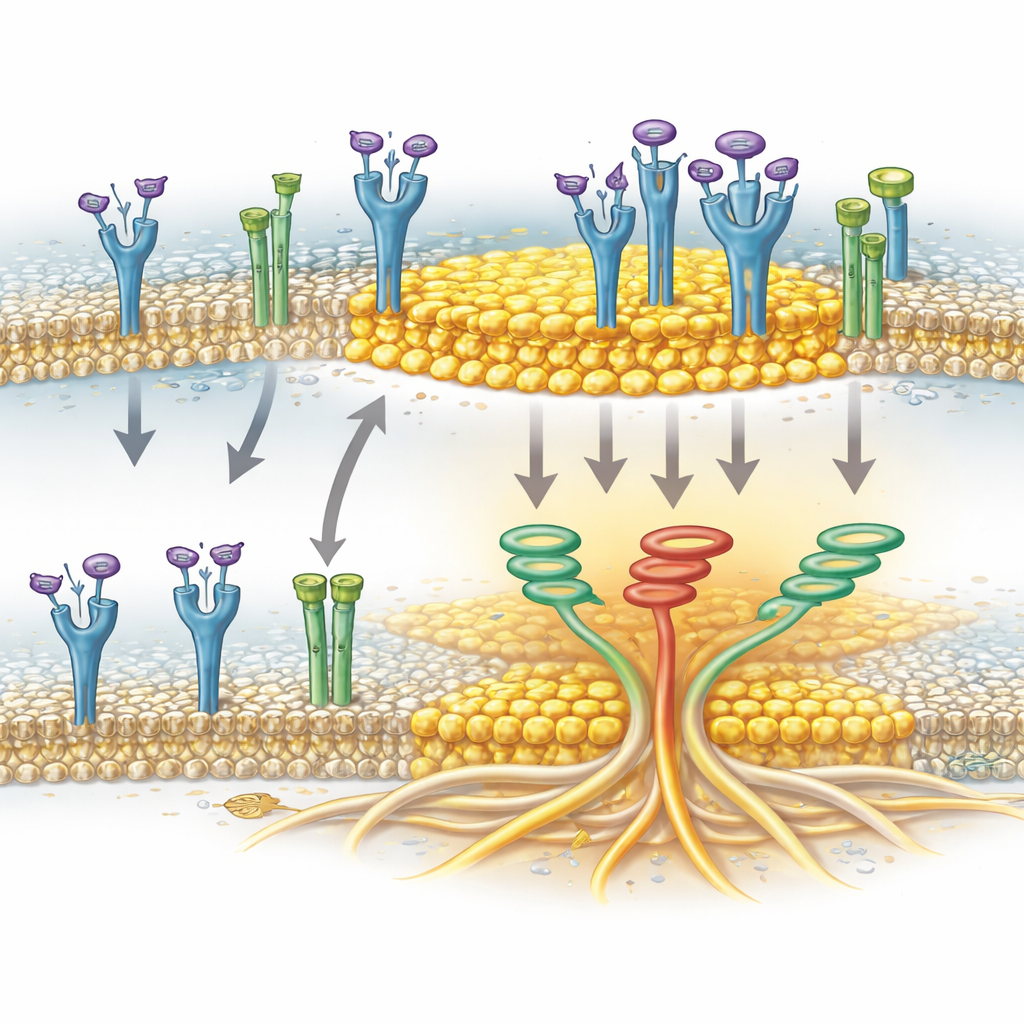
En jonkanal som hjälpare vid klustring
Studien identifierar också en överraskande hjälpare: TRPA1, ett kanalprotein mest känt för att känna av irriterande ämnen och oxidativ stress i nerver. I pankreascellernas cancerceller finns TRPA1 vid membranet och kan lokaliseras i lipidflottar. Författarna visade att TRPA1 fysiskt associerar med FGFR2c när receptorn aktiveras och att denna association sammanfaller med FGFR2c:s berikning i flottfraktionerna. När TRPA1-nivåerna minskades samlades inte aktiverad FGFR2c effektivt i flottregionerna, även om flottarna i sig förblev intakta. Detta indikerar att TRPA1 inte bara är en passagerare utan aktivt hjälper till att eskortera eller stabilisera FGFR2c inom dessa kolesterolrika plattformar, där receptorn kan utlösa det invasiva signalnätverket mer effektivt.
Vad detta innebär för framtida behandlingar
Tillsammans målar arbetet upp en bild där FGFR2c, TRPA1 och lipidflottar bildar en kooperativ enhet som förstärker den invasiva beteendet hos pankreascancerceller. FGFR2c levererar tillväxtsignalen, lipidflottarna ger den fysiska scen där signalcomplex kan samlas, och TRPA1 hjälper till att föra receptorn ut på den scenen. För en lekmannaläsare är huvudbudskapet att inte bara de cancerframkallande molekylerna själva, utan även de små membranlandskapen de uppehåller, kan avgöra hur farlig en tumör blir. Genom att rikta in sig på FGFR2c, TRPA1 eller stabiliteten hos dessa kolesterolrika öar—var för sig eller i kombination—kan framtida terapier potentiellt försvaga den invasiva maskineriet i pankreascancerceller på ett mer precist, tumörspecifikt sätt.
Citering: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Nyckelord: bukspottkörtelcancer, lipidflottar, FGFR2c, TRPA1-kanal, cellinvasion