Clear Sky Science · sv
Riktning mot p53-cancermutationerna Y220C, Y220N och Y220S med småmolekylsstabilisatorn rezatapopt
Varför detta spelar roll för framtida cancerbehandlingar
Cancer oskadliggör ofta p53, ett protein som ibland kallas cellens ”väktare”, genom mutationer som gör att det inte längre kan hålla farliga celler i schack. En särskild förändring i p53, känd som Y220C, är vanlig i solida tumörer och har blivit ett testfall för läkemedel som syftar till att reparera trasigt p53 snarare än att döda celler direkt. Denna studie ställer en praktisk, patientfokuserad fråga: kan ett lovande experimentellt läkemedel, rezatapopt, som redan är i kliniska prövningar för Y220C, också hjälpa personer vars tumörer bär närliggande men mer sällsynta mutationer på samma position i p53?
Ett läkemedel utformat för att täppa igen en spricka i p53
Många p53-mutationer får proteinet att öppna sig och förlora sin precisa form. I Y220C-mutationens fall skapar förändringen en liten kavity på proteinets yta — ett fel som kemister insåg kunde ”täppas till” med skräddarsydda små molekyler för att stabilisera p53. Rezatapopt är en sådan molekyl, konstruerad genom att bygga vidare på tidigare kemiska serier som binder i denna klyfta och fungerar som ett molekylärt stag. Författarna fokuserar på två andra mutationer på samma aminosyraposition, Y220S och Y220N, som också urholkar en liknande ficka men destabiliserar p53 ännu mer än Y220C. Om rezatapopt också kunde täppa igen dessa varianter, skulle det kunna utvidga denna precisionmedicinska strategi till tusentals fler patienter varje år. 
Mätning av hur väl rezatapopt greppar och stadgar muterat p53
För att testa detta renade forskarna p53:s DNA-bindande kärna med Y220C-, Y220S- eller Y220N-förändringar och exponerade var och en för rezatapopt (och nära kemiska släktingar). Med värmebaserade analyser visade de att alla tre mutanta proteiner blev mer stabila när läkemedlet bundit, där Y220C och Y220S effektivt återfick vildtypens liknande stadga. Däremot återfick Y220N endast en del av sin förlorade stabilitet. En andra teknik som mäter den värme som frigörs vid bindning visade varför: rezatapopt fäster mycket tätt till Y220C (i storleksordningen några tiotal nanomolar), något svagare till Y220S, och ännu svagare till Y220N, även om alla binder inom intervall som medicinalkemi betraktar som lovande.
Att se den molekylära lagningen i atomdetalj
Högupplösta röntgenkristallstrukturer gav en visuell förklaring. I alla tre mutanter ligger rezatapopt inbäddad i den mutationsskapade klyftan med en bevarad orientering: dess centrala stomme fyller kaviteten, ena änden når djupt in i fickan med en klunga fluoratomer, och den andra änden interagerar med en närliggande proteinloop. Läkemedlet skapar ett nätverk av kontakter, inklusive en strategiskt placerad fluoratomen som engagerar proteinets ryggrad. För Y220S bevaras dessa interaktioner med endast mindre förskjutningar, vilket möjliggör stark stabilisering. För Y220N tvingar däremot läkemedlets bindning asparagins sidokedja in i proteinets oljiga kärna på ett energimässigt ogynnsamt sätt, och vissa kontakter med läkemedlets fluorerade ”anker” går förlorade. Denna spända passform förklarar både den svagare bindningen och den ofullständiga återställningen av stabilitet. 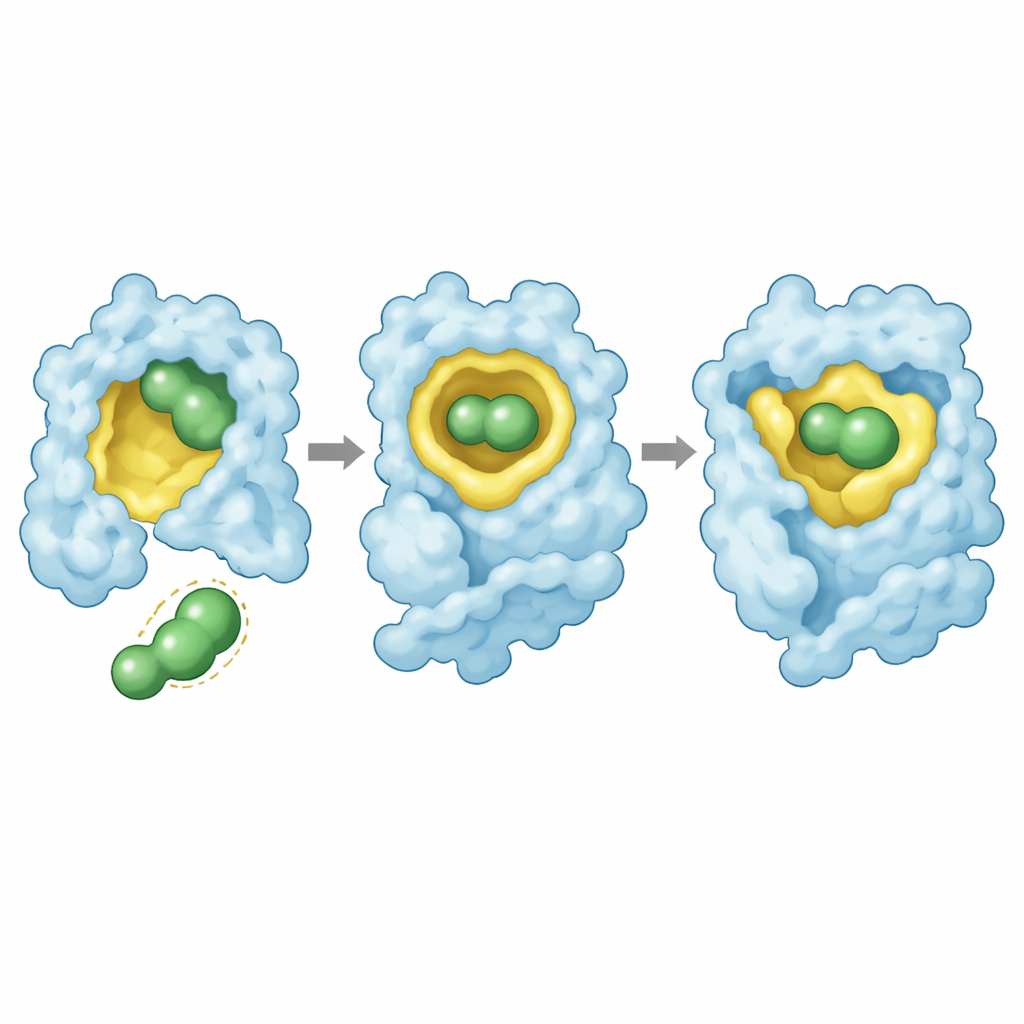
Från proteinreparation till cellbeteende
Det avgörande testet är om sådan stabilisering återupplivar p53:s skyddande roll inne i levande celler. Forskarna konstruerade lungcancerceller som saknar naturligt p53 för att uttrycka antingen Y220C-, Y220S-, Y220N- eller Y220H-varianterna. När de behandlades med rezatapopt visade celler med Y220C en kraftfull aktivering av klassiska p53-målgener som är involverade i att stoppa cellcykeln och utlösa celldöd. Y220S-celler uppvisade ett mycket liknande mönster — återhämtning av den veckade, aktiva formen av p53, stark genaktivering, fördröjd proliferation och ökad celldöd — men endast vid läkemedelskoncentrationer mer än tio gånger högre än de som krävdes för Y220C. Y220N-celler visade, i jämförelse, ingen tydlig målgensaktivering vid tolerabla doser och förblev till stor del i det felveckade tillståndet, även om svaga sena tillväxteffekter antyder enbart partiell funktionell återställning.
Vad detta betyder för patienter och framtida läkemedelsdesign
För personer med tumörer som bär Y220S-mutation ser dessa fynd försiktigt uppmuntrande ut: rezatapopt kan i princip återställa p53:s skyddande funktioner, men endast vid avsevärt högre doser, vilket kan vara svårt att uppnå säkert hos patienter. För Y220N verkar det nuvarande läkemedlet otillräckligt för att fullt reparera p53 under realistiska förhållanden. Ändå visar de strukturella ritningarna i detta arbete varför den nuvarande designen presterar sämre och hur framtida molekyler kan justeras för att engagera alla tre mutanta sidokedjor utan att tvinga dem i ogynnsamma positioner. Med andra ord ser skapandet av ett verkligt "pan-Y220"-p53-reparationsläkemedel ut att vara utmanande men möjligt, och skulle måttligt öka antalet patienter som kan dra nytta av denna framväxande strategi att laga, snarare än att ersätta, kroppens egen tumörsuppressor.
Citering: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Nyckelord: p53-reaktivering, rezatapopt, Y220C-mutation, precisionmedicin för cancer, proteinstabilisering