Clear Sky Science · sv
OTUD4-deubiquitinering stabiliserar EGFR och aktiverar PI3K/AKT-vägen för att främja invasiviteten hos trippelnegativ bröstcancer
Varför denna forskning är viktig för bröstcancer
Trippelnegativ bröstcancer är en av de svåraste formerna av bröstcancer att behandla eftersom den saknar de vanliga hormon- och tillväxtmarkörerna som många läkemedel riktar sig mot. Denna studie avslöjar en dold "beskyddare" som hjälper cancerceller att behålla en kraftfull tillväxtknapp påslagen. Genom att förstå detta osynliga stödsystem kan forskare hitta nya sätt att kapa av signalerna som driver tumörtillväxt och spridning.
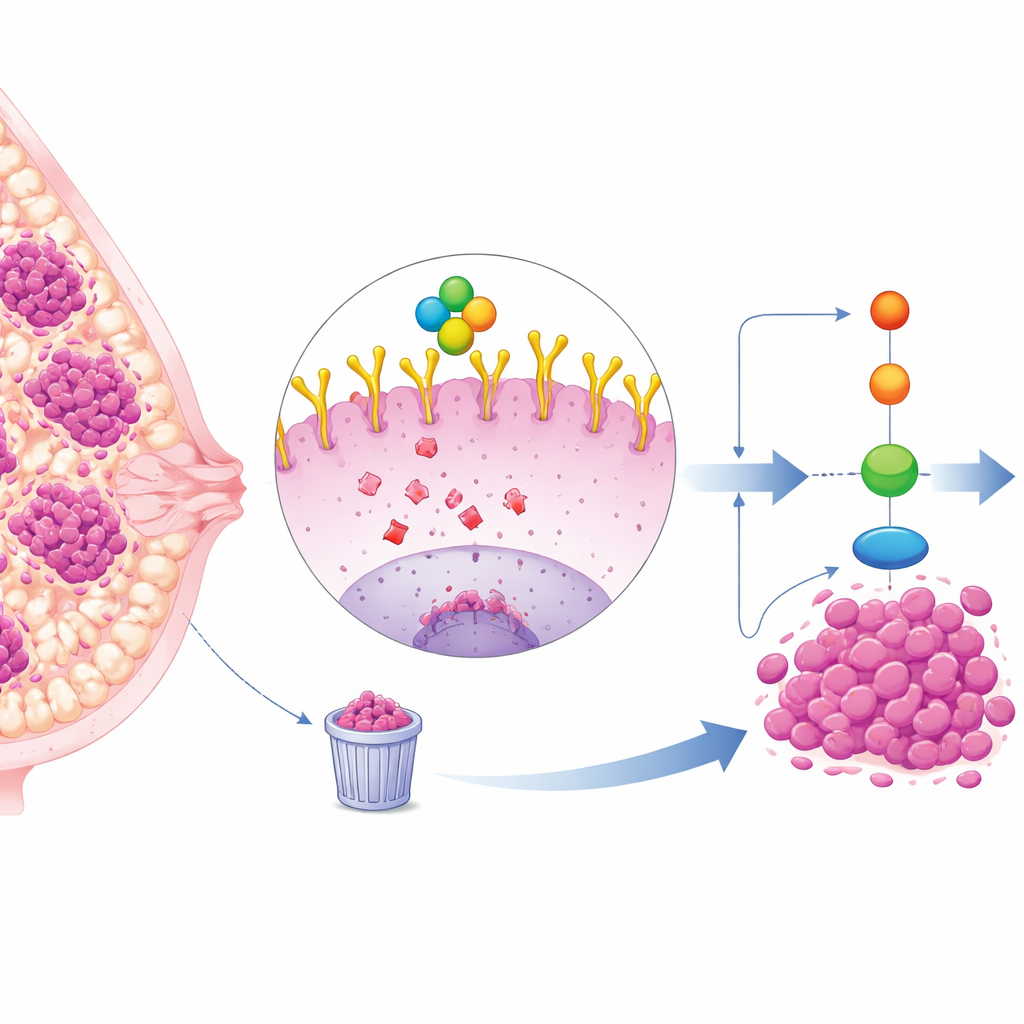
En svårbehandlad bröstcancersubtyp
Trippelnegativ bröstcancer (TNBC) utgör ungefär en fjärdedel av bröstcancerfallen och tenderar att växa och sprida sig snabbare än andra subtyper. Eftersom TNBC-celler inte har östrogen-, progesteron- eller HER2-receptorer är standardiserade riktade terapier mindre effektiva, vilket lämnar cytostatika och kirurgi som huvudalternativ. Många TNBC-tumörer visar dock höga nivåer av ett cellmembranprotein kallat EGFR, som fungerar som en antenn för tillväxt- och överlevnadssignaler. Höga EGFR-nivåer är kopplade till sämre utfall, men läkemedel som direkt blockerar EGFR har haft nedslående resultat kliniskt, vilket tyder på att det finns djupare nivåer av reglering i spel.
Att hitta en dold hjälpare för tumörtillväxt
Forskarlaget fokuserade på OTUD4, ett enzym som tar bort små proteinetiketter kallade ubiquitin från andra proteiner. Dessa etiketter fungerar ofta som bortskaffningssignaler och markerar proteiner för nedbrytning, så att deras borttagande kan stabilisera och skydda det märkta proteinet. Genom att använda omfattande cancer-databaser och vävnadsprover från patienter visade teamet att OTUD4 finns i högre nivåer i TNBC-tumörer och cellinjer än i normalt bröstvävnad. Patienter vars tumörer hade mer OTUD4 tenderade att ha sämre överlevnad, vilket antyder att OTUD4 beter sig som ett onkogen — en gen som hjälper till att driva cancerprogression.
Hur OTUD4 gör cancerceller mer aggressiva
För att testa vad OTUD4 faktiskt gör i TNBC-celler minskade forskarna dess nivåer i två väl studerade TNBC-cellinjer. När OTUD4 slogs ner växte cancercellerna långsammare, bildade färre kolonier och hade minskad förmåga att migrera i sårhelnings- och Transwell-assays, alla tecken på reducerad aggressivitet. När OTUD4 istället ökades upp skedde motsatsen: cellerna prolifererade snabbare och rörde sig lättare, vilket förstärker idén att OTUD4 driver malign beteende. I möss växte tumörer bildade av celler utan OTUD4 långsammare och visade reducerade markörer för celldelning och tillväxtsignaler, vilket bekräftar dessa effekter i levande organismer.
En molekylär sköld som skyddar EGFR
Genom att gräva i mekanismen använde teamet proteininteraktionsskärmar och biokemiska analyser för att identifiera EGFR som en direkt bindningspartner till OTUD4. De fann att OTUD4 binder till en specifik region av EGFR och tar bort K48-kopplade ubiquitinkedjor — den typ av märkning som normalt signalerar för destruktion via cellens återvinningsmaskineri. När OTUD4 minskade, degraderades EGFR snabbare, men dess genaktivitet förblev oförändrad, vilket visar att OTUD4 verkar efter att EGFR har syntetiserats, inte på DNA- eller RNA-nivå. Blockering av cellens proteinnedbrytningssystem återställde EGFR-nivåerna, vilket understryker att nyckelsteget är skydd mot nedbrytning. Med en mer stabil EGFR på cellytan förblir en huvudintern signalväg, PI3K/AKT/mTOR, påslagen och driver celltillväxt och överlevnad.
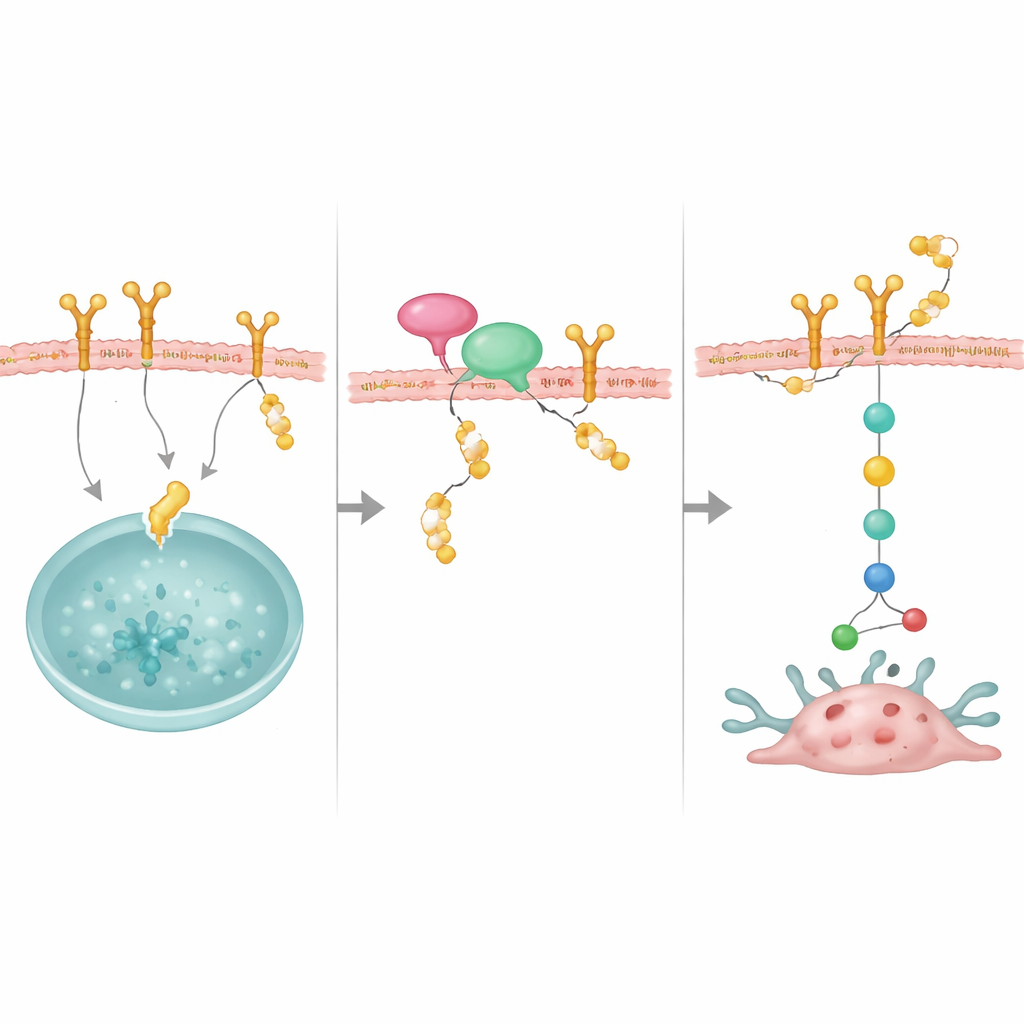
En adapter som för beskyddaren till dess mål
Studien avslöjade också en viktig partner, NRP1, ett membranprotein tidigare kopplat till aggressiva bröstcancerformer. NRP1 binder både OTUD4 och EGFR och hjälper till att föra OTUD4 i position för att rädda EGFR från nedbrytning. När NRP1 minskades blev EGFR mindre stabilt och dess tillväxtsignaler försvagades, även om OTUD4-nivåerna inte förändrades. Överproduktion av OTUD4 kunde delvis kompensera för förlusten av NRP1, vilket tyder på att NRP1 fungerar som en dokningsplattform som rekryterar OTUD4 till EGFR. Tillsammans bildar dessa molekyler ett stabiliserande komplex som håller EGFR rikligt närvarande på cellytan.
Vad detta betyder för framtida behandling
Genom att avslöja hur OTUD4 och NRP1 samarbetar för att skydda EGFR från nedbrytning identifierar denna studie en ny kontrollpunkt för en nyckeltillväxtsignal i trippelnegativ bröstcancer. Istället för att försöka blockera EGFR:s aktivitet vid dess aktiva säte kan framtida terapier sikta på att störa OTUD4:s skyddande funktioner eller dess rekrytering via NRP1, vilket skulle sänka EGFR-nivåerna och dämpa PI3K/AKT-vägen som driver tumörtillväxt. Även om mer arbete krävs för att hitta säkra och effektiva OTUD4-hämmare och för att förstå möjliga undanflyktsvägar som cancerceller kan använda, öppnar fynden lovande vägar för mer precisa behandlingar mot denna utmanande bröstcancersubtyp.
Citering: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Nyckelord: trippelnegativ bröstcancer, EGFR-signalering, OTUD4, PI3K AKT-vägen, proteinnedbrytning