Clear Sky Science · sv
Kortkedjig acyl‑CoA‑dehydrogenas initierar mtDNA‑demetylering och läckage för att främja antitumörimmunitet vid kolorektal cancer
Varför våra egna celler ibland döljer cancer för immunsystemet
Kolorektal cancer är en av världens dödligaste tumörer, delvis därför att kroppens immunsvar ofta misslyckas med att känna igen och attackera den. Denna studie avslöjar en oväntad koppling mellan hur cancerceller förbränner fetter, hur deras små kraftverk (mitokondrier) hanterar sitt DNA och huruvida immunsystemet varnas om tumörens närvaro. Genom att spåra denna händelsekedja framhäver forskarna också en gammal naturlig förening, hypericin, som ett potentiellt sätt att återväcka immunsvaret mot kolorektal cancer.
En saknad mitokondriell ”väktare” i kolonstumörer
Teamet började med att söka i stora mänskliga och musdatabaser efter metabola gener som konsekvent förändras vid kolorektal cancer. Ett enzym stack ut: kortkedjig acyl‑CoA‑dehydrogenas, eller ACADS, som normalt hjälper mitokondrier att bryta ner korta fettsyror. I både patientprover och flera musmodeller var ACADS‑nivåerna märkbart lägre i tumörvävnad än i närliggande frisk tarm. När forskarna minskade ACADS i muskolonceller växte tumörerna snabbare och mer aggressivt; att öka ACADS bromsade tumörtillväxten. Möss konstruerade att sakna ACADS specifikt i tarmens slemhinna utvecklade fler och större tumörer i en kemisk modell för kolit‑associerad cancer, vilket stöder idén att ACADS fungerar som en tumörsuppressor i tarmen.
Hur tumörer tystar immalarm
Dessa tillväxteffekter kunde inte förklaras bara av hur snabbt cancerceller delade sig i odling, vilket förändrades lite. Istället drev ACADS‑bortfall tumörtillväxt endast i djur med intakta immunsystem, vilket pekar på förändringar i tumörmikromiljön. Encellsanalyser av mänskliga kolorektala cancer visade att tumörer med låg ACADS omges av fler tumörceller och immunsuppressiva celler—såsom myeloida supressorceller, vissa makrofager och regulatoriska T‑celler—och färre hjälpsamma T‑celler och naturliga mördarceller. Detta mönster pekar på ett ”immunosuppressivt kvarter” som skyddar cancern från angrepp. 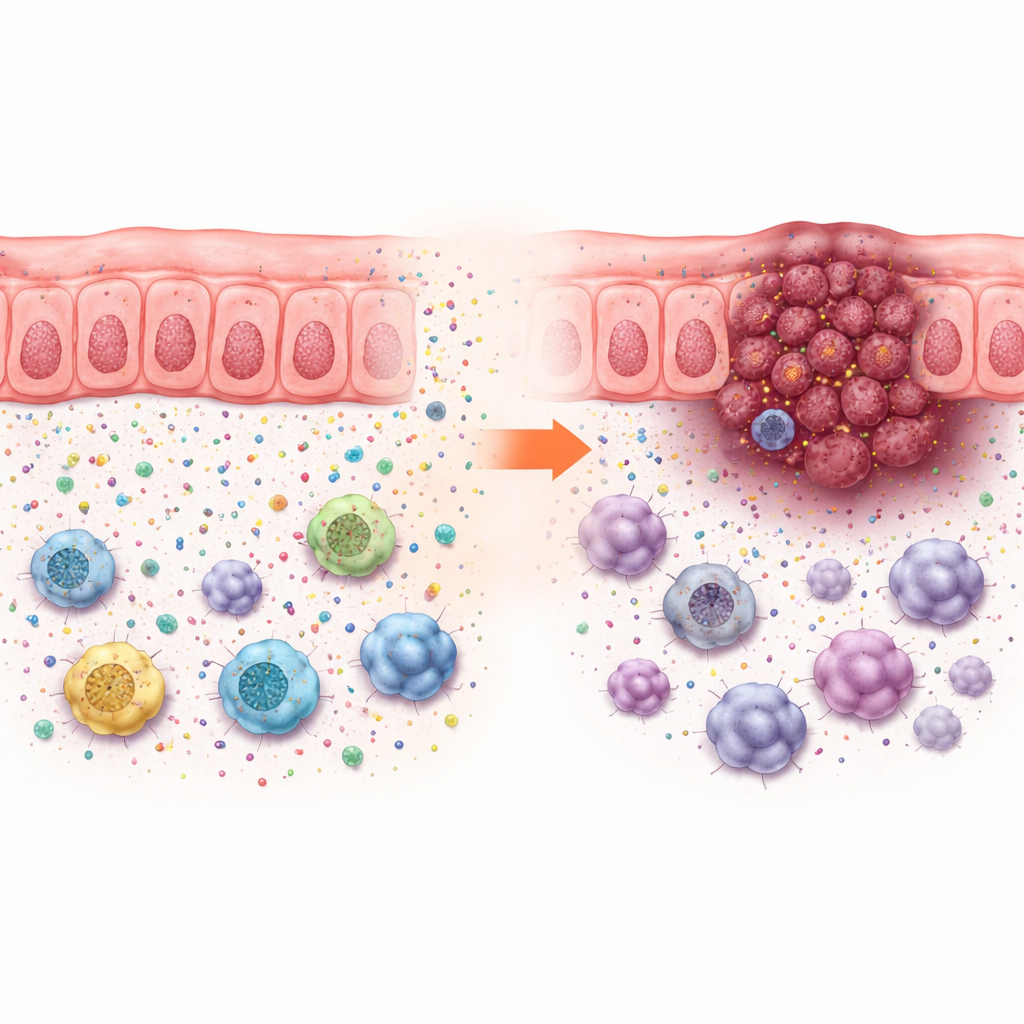
Mitokondriellt DNA‑läckage som den dolda utlösaren
Vad binder ett fettförbrännande enzym till en DNA‑sensor i immunsystemet? Svaret ligger i mitokondriellt DNA (mtDNA). Vid stress kan fragment av mtDNA läcka från mitokondrierna ut i cellens inre vätska, där cGAS upptäcker dem som en fara. Forskarna visade att ACADS‑bristiga cancerceller hade mindre mtDNA i detta utrymme, även om totalt mtDNA var oförändrat. Blockera mtDNA‑läckage i ACADS‑rika celler stängde av cGAS–STING, vilket bekräftar att dessa undkomna DNA‑fragment är det avgörande larmet. Överraskande nog kunde klassiska mitokondriella stressfaktorer som reaktiva syreradikaler, kalciumpyningar och stora förändringar i mitokondriell form inte fullt ut förklara skillnaden. Istället pekar studien på ”grindarna” i mitokondriemembranet och, viktigast, de kemiska markeringarna på mtDNA själv. 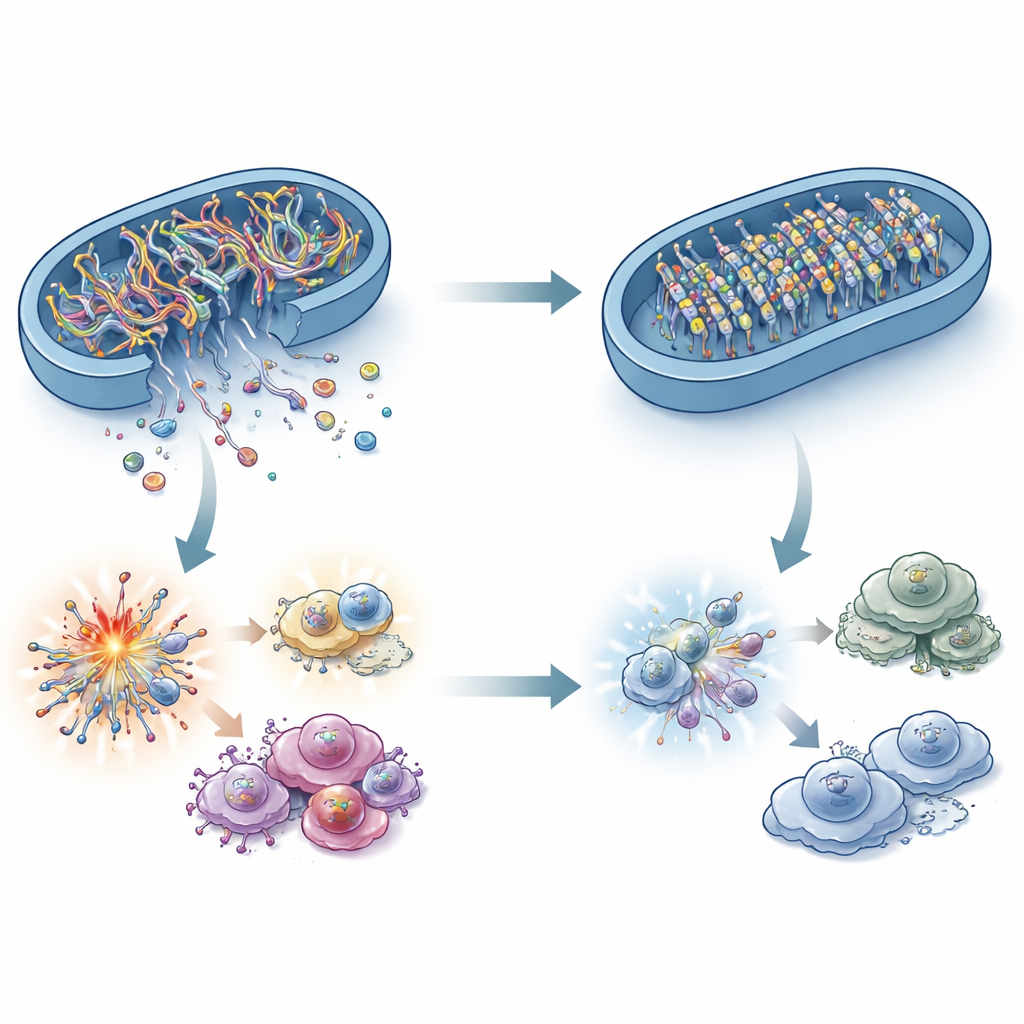
En DNA‑metylerande partner som låser in larmet
Genom proteininteraktionsskärmar fann man att ACADS associerar med en form av DNA‑metyleringsenzymet DNMT1 som lokaliserar till mitokondrier. När ACADS förlorades ackumulerades denna mitokondriella DNMT1 och satte extra metylgrupper på mtDNA. Dessa märkningar gör mtDNA mer stabilt och mindre benäget att brytas sönder och läcka. Att överuttrycka mitokondriell DNMT1 minskade mtDNA‑flykt, dämpade cGAS–STING‑signalering och påskyndade tumörtillväxt, medan blockering av DNMT1 med läkemedlet decitabin återställde mtDNA‑läckage och bromsade ACADS‑defekta tumörer. Patientprover speglade dessa fynd: låg ACADS sammanföll med hög mitokondriell DNMT1, svagare STING‑signalering, färre effektor‑T‑celler, fler suppressiva immunceller och sämre förväntade svar på checkpoint‑immunoterapi.
Återväckning av immunsvar med en gammal förening
För att se om denna väg kunde utnyttjas terapeutiskt använde forskarna datorbaserad screening för att söka efter molekyler som binder ACADS. De identifierade hypericin, ett naturligt pigment tidigare testat som ljusaktiverad behandling för vissa hudlymfom. I kolorektala cancerceller ökade hypericin ACADS‑nivåer, minskade mitokondriell DNMT1, ökade mtDNA‑läckage och återaktiverade cGAS–STING‑signalering—förändringar som var beroende av närvaro av ACADS. I musmodeller för tumörer och i korttidsodlingar av mänskliga kolorektala tumörer krympte tumörer eller skiftade immuncellsammansättningen mot ett mer aktivt, T‑cellsrikt tillstånd efter behandling med hypericin. Trots att ytterligare arbete krävs före klinisk användning tyder dessa resultat på att farmakologisk "återinkoppling" av ACADS kan hjälpa till att omvandla en kall, immunundertryckt tumör till en som svarar bättre på immunoterapi.
Vad detta betyder för patienter och framtida behandlingar
I vardagliga termer visar detta arbete att vissa kolorektala cancerformer växer delvis därför att de tystar ett mitokondriellt enzym som normalt hjälper till att läcka ut små DNA‑snuttar i cellens inre, där de fungerar som signaler för att kalla in immunsystemet. Genom att låta en DNA‑metylerande partner låsa det mitokondriella DNA:t på plats håller ACADS‑defekta tumörer dessa signaler dolda och undviker immunigenkänning. Att återställa ACADS‑aktivitet, till exempel med hypericinliknande läkemedel, kan återöppna detta mitokondriella alarmsystem, stärka antitumörimmuniteten och förbättra svaren på befintliga immunoterapier. ACADS, mitokondriell DNMT1 och STING‑vägens aktivitet kan därför tjäna som användbara biomarkörer och måltavlor i jakten på mer effektiva behandlingar mot kolorektal cancer.
Citering: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Nyckelord: kolorektal cancer, tumörimmunitet, mitokondriellt DNA, lipidmetabolism, cGAS‑STING‑vägen