Clear Sky Science · sv
Att rikta in sig på fused in sarcoma (FUS): en ny antisense‑strategi för behandling av idiopatisk lungs Fibros
Varför ärrade lungor spelar roll
Idiopatisk lungsfibros (IPF) är en obeveklig lungsjukdom där de känsliga luftblåsorna långsamt förvandlas till stel ärrvävnad, vilket gör varje andetag tyngre. Dagens läkemedel kan bromsa denna ärrbildning men kan inte stoppa eller vända den. Denna studie undersöker ett nytt mål kallat FUS, ett protein som hjälper celler att hantera sina genetiska budskap, och testar om att stänga av det med en utformad tråd av DNA‑liknande material kan dämpa ärrbildningsprocessen och hjälpa skadade lungor att reparera sig själva.
En cellulär trafikledare som går fel
FUS är ett protein som normalt finns i cellkärnan, där det hjälper till att hantera hur RNA — våra geners arbetsexemplar — processas och används. I hjärnsjukdomar som ALS kan FUS uppföra sig fel, lämna kärnan, klumpa ihop sig i cellens yttre områden och störa normal cellfunktion. Författarna undrade om ett liknande felaktigt beteende kan driva ärrbildning vid IPF. De studerade lungfibroblaster — bindvävscellerna som deponerar ärrmaterial — från patienter med IPF och från friska donatorer. I IPF‑celler var FUS‑nivåerna högre överlag och, avgörande, mycket mer FUS återfanns i cytoplasman än i friska celler. Med högupplöst elektronmikroskopi bekräftade de att detta protein var onormalt rikligt utanför kärnan, vilket antyder att dess normala kontroll över RNA kan vara förvriden i fibrotiska lungor. 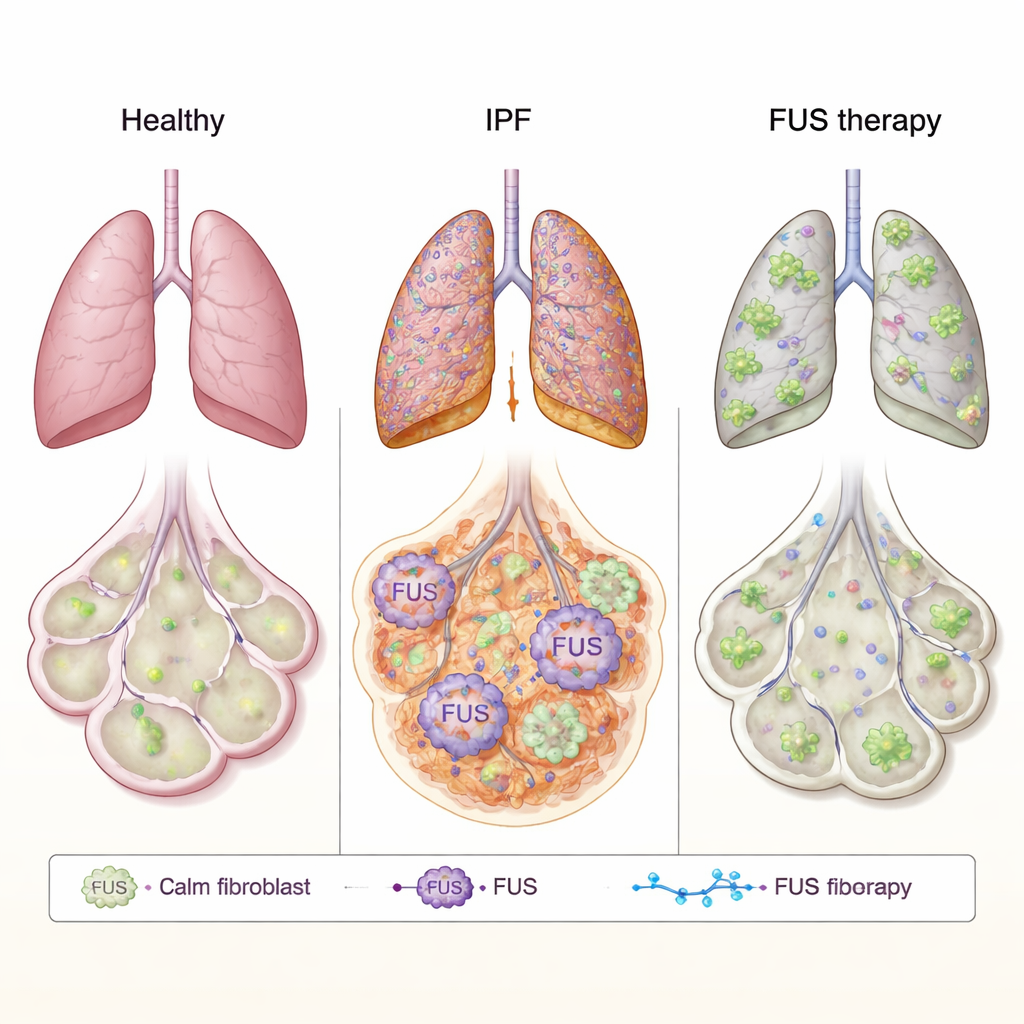
Hur FUS när bränsle åt ärrbildande celler
För att se vad detta felaktiga protein faktiskt gjorde ökade forskarna FUS i friska fibroblaster och minskade det i IPF‑fibroblaster. Extra FUS fick friska celler att dela sig snabbare, medan minskad FUS i IPF‑celler saktade ner deras tillväxt och förflyttning — två beteenden som är centrala för ärrbildning. Teamet använde sedan en teknik som ”fryser” protein–RNA‑partnerskap på plats och läser av vilka RNA som är bundna till FUS. I IPF‑fibroblaster hittades FUS bundet till många genetiska budskap som främjar fibros, inklusive de som kodar för kollagen, tillväxtfaktorer som TGF‑β och inflammatoriska signaler. Med andra ord agerade FUS som en nav som kopplade ihop ett helt nätverk av pro‑ärrande budskap.
Tysta signalen med ett precisionsläkemedel
Studien testade ett antisens‑oligonukleotid kallat ION363 — en kort, kemiskt modifierad sträng utformad för att binda FUS‑RNA och utlösa dess nedbrytning. När IPF‑fibroblaster behandlades med ION363 sjönk FUS‑nivåerna, cellerna saktade sin proliferation och migration, och nyckelgener för ärrbildning tystnade. Viktigt är att denna effekt inte berodde på att cellerna dödades eller tvingades in i åldrande; istället verkade det återställa deras beteende. När samma behandling applicerades på tunna skivor av IPF‑lungvävnad som hölls levande i laboratoriet, dämpades stora grupper av gener kopplade till extracellulär matrix, inflammation och onormalt epitel, medan gener associerade med hälsosam surfaktantproduktion och alveolär funktion förstärktes. Behandlingen minskade också kollagenfärgning och ökade markörer för funktionella lungsurfaceceller, vilket tyder på en förskjutning från ärrbildning mot reparation.
Hjälpa skadade luftblåsor att återväxa
Eftersom de små cellerna som bekläder luftblåsorna, kända som typ II alveolära celler, är avgörande för lungreparation byggde forskarna tredimensionella ”alveolosfärer” från patientceller för att efterlikna miniatyrlung‑enheter. I odlingar från IPF‑patienter överlever dessa strukturer normalt dåligt. Med ION363‑behandling bildades fler alveolosfärer, de växte större och visade ökad lysosomal aktivitet — ett kännetecken för aktiv förnyelse. Detaljerad färgning visade fler celler med markörer för mogna gasutbytesceller, vilket indikerar att tystnad av FUS inte bara lugnade fibroblasterna utan också uppmuntrade det skadade epitelet att återbygga en hälsosammare yta. 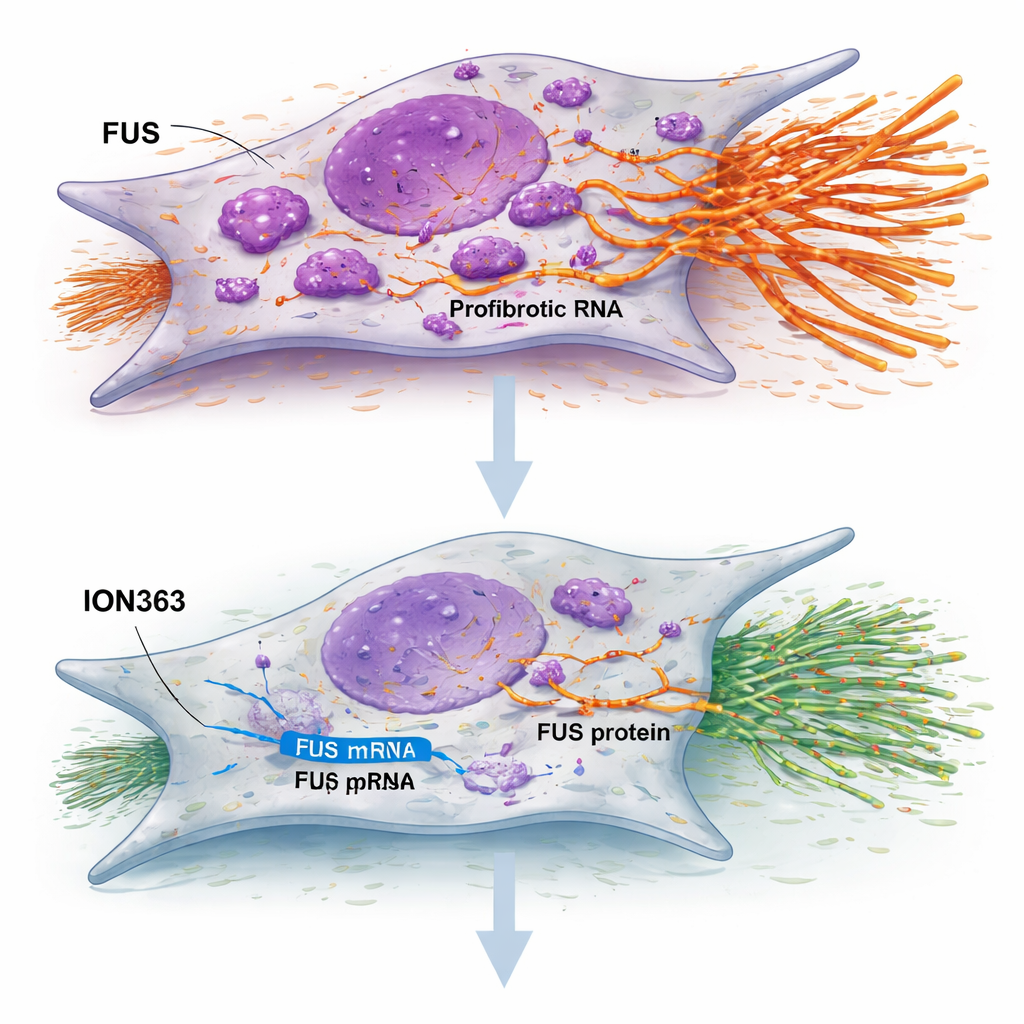
Vad detta kan innebära för patienter
Tillsammans målar arbetet upp FUS som en huvudavstängare i IPF som kopplar överaktiva ärrbildande fibroblaster till misslyckad reparation av de känsliga luftblåsorna. Genom att dämpa FUS med ett riktat antisensläkemedel kunde forskarna reducera profibrotiska genprogram, lätta kollagenuppbyggnad och främja regeneration i patient‑härledda lungmodeller. Även om detta tillvägagångssätt fortfarande är på laboratoriestadiet och kommer att kräva noggranna tester i djurmodeller och kliniska prövningar, tyder det på att IPF en dag kanske kan behandlas inte bara genom att bromsa ärrbildning utan genom att direkt återbalansera de cellulära program som styr lungskada och reparation.
Citering: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Nyckelord: idiopatisk lungsfibros, antisens‑oligonukleotid, FUS‑protein, lungsfibros, alveolär reparation