Clear Sky Science · sv
Delvis förkortning av PTCH1:s C-terminala domän i cancer främjar tumörbildning genom icke-kanonisk aktivering av en GLI–PI3K-loop
Varför en liten proteinförändring spelar roll vid koloncancer
Koloncancer uppstår vanligen genom en långsam ansamling av genetiska skador. Denna studie fokuserar på en överraskande liten förändring i ett cellmembranprotein kallat PTCH1 och visar hur avkapning av en del av dess svans kan få koloncancerceller att växa snabbare, sprida sig lättare och potentiellt bli motståndskraftiga mot vissa befintliga läkemedel. Att förstå denna dolda tillväxtbrytare kan öppna dörren för nya, mer precisa behandlingar för en undergrupp av patienter.
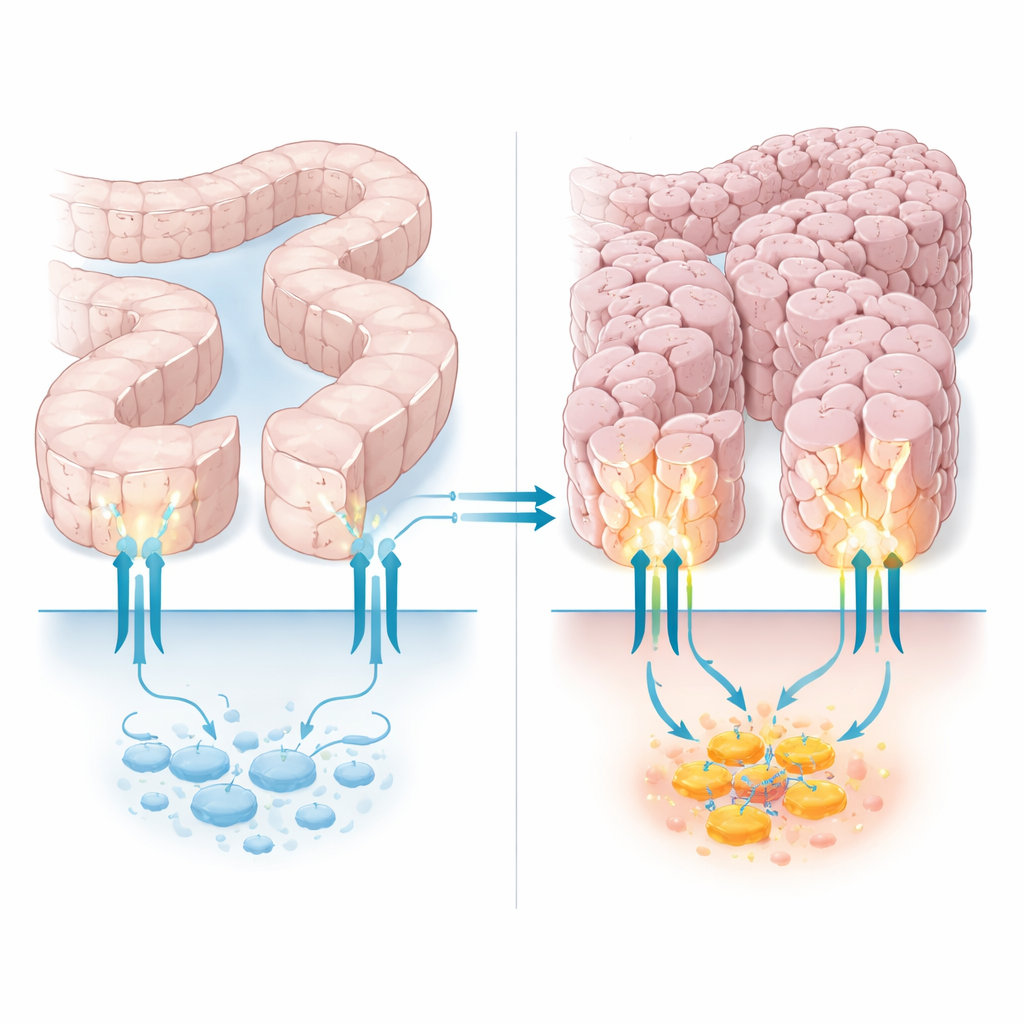
Cellens grindvakt med en dold sidofunktion
PTCH1 är mest känd som grindvakten i Hedgehog‑vägen, en kommunikationslinje celler använder under utveckling och vävnadsreparation. I sin klassiska roll håller PTCH1 en partnerprotein, Smoothened, i schack och reglerar därigenom en familj av DNA‑regulatorer kallade GLI. Men PTCH1 har också en lång, flexibel svans som hänger inuti cellen och fungerar som en fästyta för andra proteiner som påverkar celldöd, återvinning av cellkomponenter och mer. Tidigare arbete visade att vissa cancerformer i tjocktarm, magsäck och livmoder bär mutationer som kapar bort en del av denna inre svans. Dessa mutationer verkade inte rubba den klassiska Hedgehog‑strömbrytaren men gjorde att cancerceller klarade stress bättre, vilket antyder att denna svanssektion tyst bidrar till PTCH1:s tumörsuppressiva funktion.
Konstruera cancerceller för att testa effekten
För att se vad dessa svansförkortande mutationer verkligen gör använde forskarna CRISPR/Cas9‑genredigering för att återskapa dem i en koloncancercellinje. De jämförde två redigerade kloner, vardera med en annan truncering i PTCH1‑svansen, med i övrigt identiska celler som bar normal PTCH1. De mutanta cellerna delade sig snabbare, bildade många fler kolonier och klarade sig även när de måste växa utan fäste—ett beteende kopplat till förmåga att sprida sig i kroppen. När de implanterades i möss gav svansmutanterna mycket större tumörer på några veckor, med fler celler i delning. Viktigt är att de redigerade cellerna fortfarande producerade PTCH1 och behöll dess huvudfunktion som grindvakt, vilket visar att den ökade aggressiviteten beror på förlusten av svansens specialiserade interna uppgifter, inte på att PTCH1 tagits bort helt.
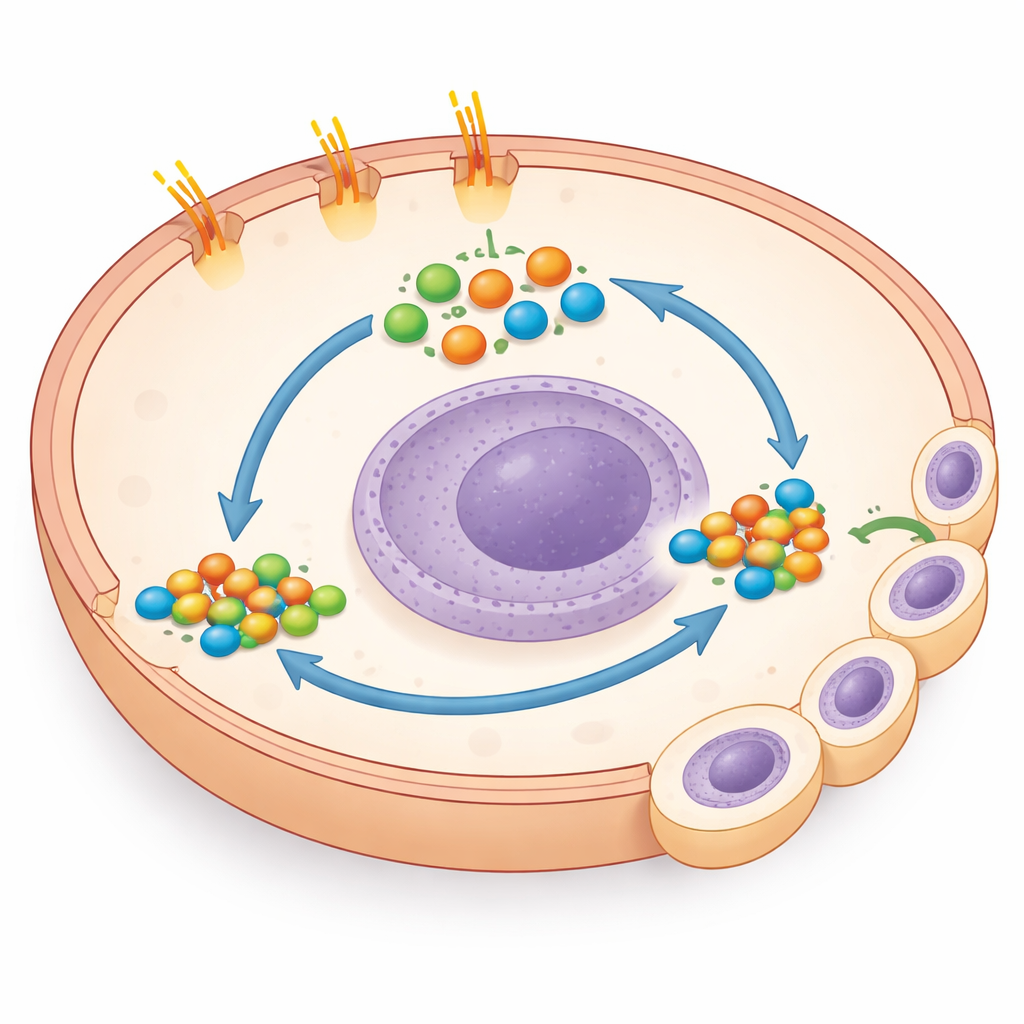
En överraskande genväg till en kraftfull tillväxtbrytare
När forskarna grävde i den bakomliggande biologin gjorde de en oväntad upptäckt: de svansförkortade cellerna hade starkt förhöjda nivåer av GLI1 och GLI2, nyckeldrivare av genprogram som främjar tillväxt och överlevnad. Normalt ökar GLI‑aktivitet när Smoothened släpps lös, men att blockera Smoothened hade ingen effekt här. I stället minskade direkt blockad av GLI med en liten molekyl, eller sänkning av GLI1 med genetiska verktyg, kraftigt tillväxten hos de mutanta cellerna i odling och i ytterligare koloncancercellinjer som naturligt bär PTCH1‑svansmutationer. Detta visade att svansförlusten aktiverar GLI via en ”icke‑kanonisk” väg som kringgår den vanliga Hedgehog‑brytaren, och att cancercellerna blir starkt beroende av denna genväg för sitt aggressiva beteende.
Flera tillväxtkretsar aktiveras, men en loop dominerar
Genom att sekvensera RNA från cellerna fann forskarna tusentals gener vars aktivitet förändrades när PTCH1‑svansen förkortades. Många tillhörde välkända cancerkretsar, inklusive de som styrs av epidermal tillväxtfaktorreceptor (EGFR), Ras, och signalvägar som reglerar cellmetabolism och stamliknande egenskaper. De mutanta cellerna visade ökad aktivitet av EGFR och dess ligander samt högre aktivitet i två stora nedströmsvägar: MAPK‑ och PI3K/Akt‑vägarna. När forskarna blockerade EGFR eller dess MAPK‑gren saktade de mutanta cellerna dock bara delvis ner. I kontrast hämmade låga doser av PI3K‑hämmare deras tillväxt och kolonibildning kraftigt och sänkte GLI1‑nivåerna, vilket lyfter fram PI3K/Akt som en kritisk partner i denna nya mekanism för GLI‑aktivering.
En självförstärkande loop som driver tumörtillväxt
Ytterligare experiment avslöjade en återkopplingscykel: förkortning av PTCH1:s svans ökar GLI‑aktivitet; GLI i sin tur hjälper till att hålla PI3K/Akt‑signaleringen hög; och PI3K/Akt bidrar till att stabilisera och aktivera GLI. Att störa antingen GLI eller PI3K bröt denna loop och berövade de mutanta cellerna deras tillväxtfördel, medan enkel uppreglering av PI3K/Akt inte kunde övervinna direkt GLI‑blockad. Cellerna visade också dämpad aktivitet av PKA, ett enzym som normalt märker GLI‑proteiner för inaktivering, vilket sannolikt ytterligare tippar balansen mot GLI‑drivna program.
Vad detta kan innebära för framtida behandling
För patienter är huvudbudskapet att vissa koloncancer bär PTCH1‑svansmutationer som tyst kopplar ihop en GLI–PI3K‑positiv återkopplingsloop, vilket hjälper tumörer att växa och undvika läkemedel som riktar sig mot den mer kända Hedgehog‑brytaren eller EGFR–MAPK‑vägen. Dessa tumörer kan i stället vara särskilt sårbara för behandlingar som stänger av GLI direkt eller angriper PI3K/Akt. Arbetet föreslår att sekvensering av PTCH1 i kolonstumörer—särskilt de från höger sida av tjocktarmen, där sådana mutationer är vanligare—kan hjälpa till att identifiera patienter som kan dra nytta av PI3K‑ eller GLI‑inriktade strategier, och göra en subtil proteinkapning till en användbar terapeutisk ledtråd.
Citering: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Nyckelord: koloncancer, Hedgehog-signalering, PTCH1-mutationer, GLI-transkriptionsfaktorer, PI3K–Akt-vägen