Clear Sky Science · ru
Нарушение гомеостаза нейтрофилов связано с функциональными изменениями митохондрий у критически больных пациентов с COVID−19
Почему это важно для пациентов с COVID-19
Большинство людей теперь знают, что COVID-19 — это не просто инфекция легких, но то, как вирус обращает собственные защитные механизмы организма против него, по-прежнему уточняется. В этом исследовании подробно изучают нейтрофилы — распространенный тип белых кровяных клеток — у пациентов с угрожающим жизни COVID-19 в отделении интенсивной терапии. Исследователи, анализируя жизненный цикл этих клеток, их гибель и работу их «мини-электростанций» (митохондрий), выявляют картину настырных, гиперактивных нейтрофилов, которая может объяснять стойкое воспаление, повреждение крови и органов при тяжелом течении болезни.
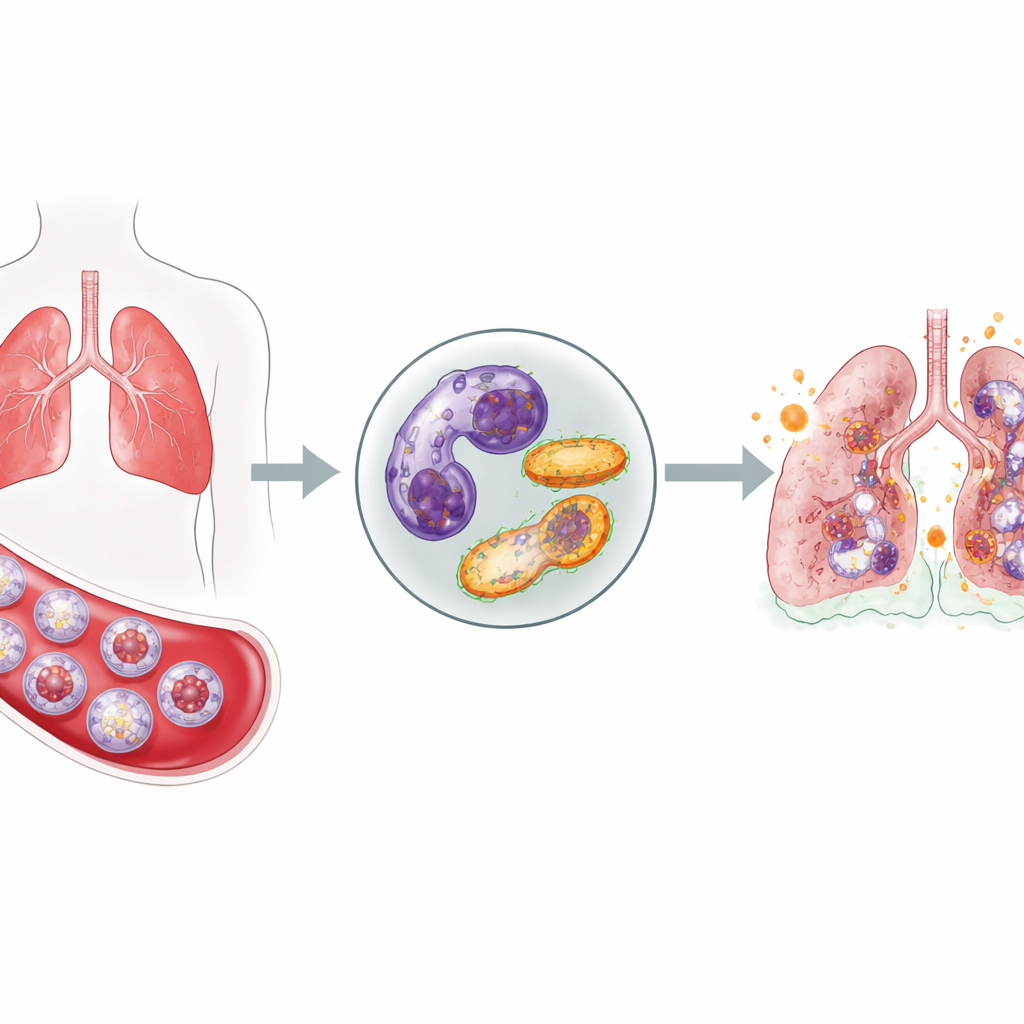
Передовые клетки, которые не отступают
Нейтрофилы — одни из первых реагирующих на инфекцию: они быстро попадают в кровь, проникают в ткани и выделяют токсичные молекулы для уничтожения вторгающихся микроорганизмов. Обычно после выполнения своей функции они тихо самоустраняются и утилизируются, чтобы не повредить здоровые ткани. У критически больных пациентов с COVID-19 исследователи обнаружили совсем иную картину. По сравнению со здоровыми добровольцами у этих пациентов отмечалось резкое увеличение числа нейтрофилов в крови и, что важно, многие из них были незрелыми клетками, поспешно выпущенными из костного мозга. Одновременно несколько тестов показали, что меньшее число нейтрофилов подвергалось нормальной программируемой смерти, что говорит о том, что эти агрессивные клетки задерживаются дольше положенного.
Тонкие генетические сигналы, но ясный паттерн выживания
Исследователи также изучали крошечные регуляторные молекулы — микроРНК — в нейтрофилах у выживших и не выживших пациентов из отделения интенсивной терапии. Некоторые из этих молекул были изменены таким образом, что на бумаге это указывало на нарушение путей, контролирующих гибель клетки и баланс кальция. Однако при измерении прямых маркеров клеточной смерти существенных различий между выжившими и не выжившими не обнаружилось — обе группы демонстрировали одинаково сниженную самоуничтожение нейтрофилов по сравнению со здоровыми людьми. Это означает, что паттерны микроРНК больше служат подсказкой для будущих исследований, чем твердым индикатором исхода, и подчеркивает, что общая неспособность нейтрофилов выключаться является общей чертой тяжелого COVID-19.
Сдвиги кальция и перенапряженные «электростанции»
Чтобы понять, почему нейтрофилы не умирали по расписанию, команда сосредоточилась на двух тесно связанных системах внутри клеток: кальциевых сигналах и митохондриях. Ионы кальция выступают в роли крошечных выключателей для множества клеточных решений, включая самоуничтожение. Исследователи обнаружили, что в нейтрофилах у пациентов с тяжелым COVID-19 было меньше свободного кальция внутри, а также снижены уровни ключевых белков, которые обычно помогают переносить кальций в митохондрии и открывать предохранительный клапан, способный запустить клеточную смерть. В то же время сами митохондрии были необычно «заряжены» — с более высоким электрическим градиентом через мембраны и повышенным потреблением кислорода, особенно по одному основному дыхательному пути. Вместо того чтобы выключаться, эти сверхактивные митохондрии продуцировали больше реактивных кислородных молекул, которые могут повреждать окружающие ткани и подпитывать воспаление.
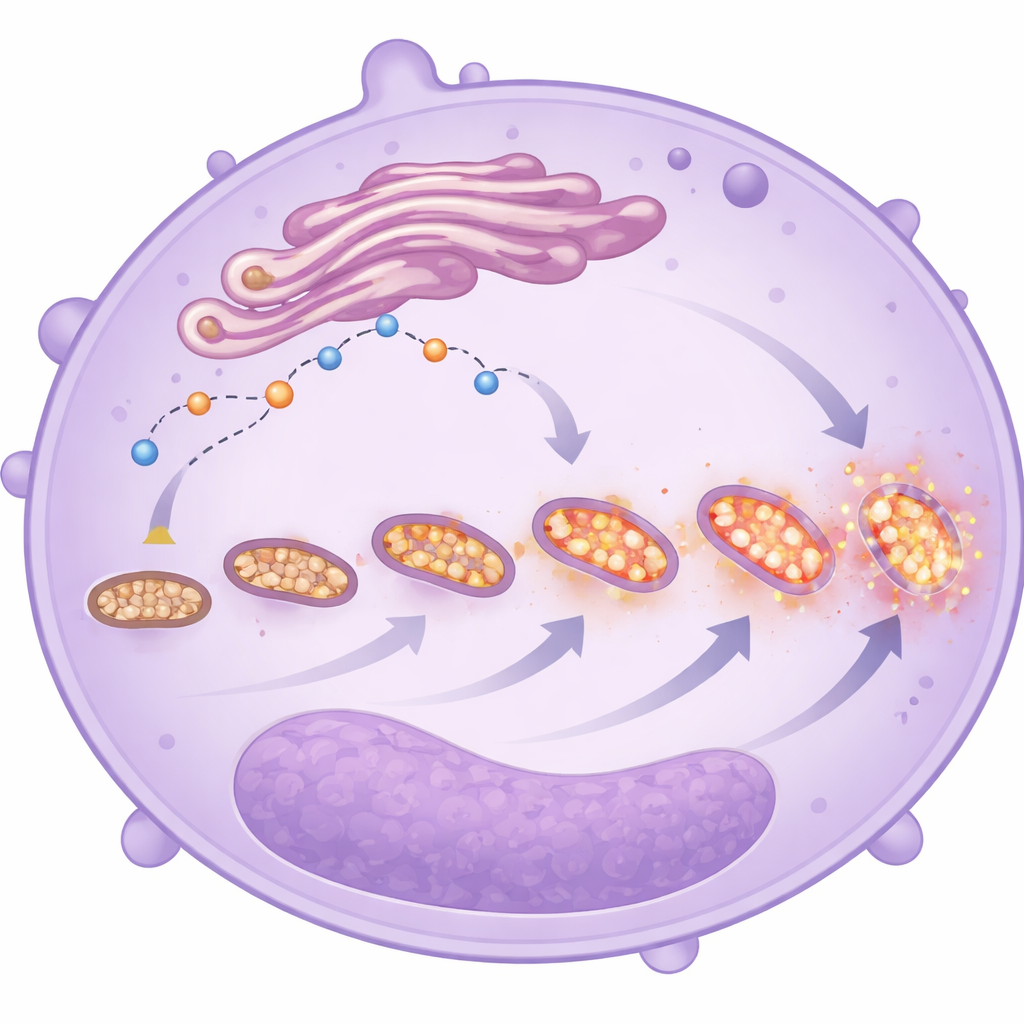
Напряженные и фрагментированные митохондрии
Изображения электронного микроскопа и флуоресцентные красители дали более детальный взгляд на форму и поведение этих митохондрий. В нейтрофилах самых больных пациентов митохондрий было больше, но они были мельче и сильнее фрагментированы — признаки, которые часто указывают на стресс. Эти клетки также демонстрировали повышенные уровни митохондриальных реактивных видов кислорода, независимо от того, выжил ли пациент в конечном итоге. В сочетании с измененным обращением кальция и отсроченной клеточной смертью эти изменения рисуют картину нейтрофилов, изменивших свою энергетическую стратегию: вместо того чтобы в основном полагаться на простой распад сахара, они все больше полагаются на митохондриальный метаболизм, особенно незрелые клетки. Этот переключатель может повышать их способность мигрировать, сохраняться и выделять повреждающие молекулы в легких и других органах, хотя исследование не может доказать, что они являются прямой причиной худших исходов.
Что это может означать для будущего лечения
Проще говоря, исследование предполагает, что при критическом COVID-19 нейтрофилы становятся слишком многочисленными, слишком молодыми и слишком трудными для отключения. Их внутриклеточные кальциевые сигналы и митохондрии перепрограммированы таким образом, что сохраняют клетки живыми и очень активными, порождая вспышки вредных кислородсодержащих соединений. Хотя работа носит наблюдательный характер и не доказывает причинно-следственной связи, она выделяет несколько потенциальных «регуляторов» в этих клетках — такие как регуляторы кальция и митохондриальные контрольные точки — которые однажды могут стать целью для мягкого восстановления нормального поведения нейтрофилов. Если будущие исследования подтвердят эти идеи, методы, восстанавливающие правильную остановку нейтрофилов или успокаивающие их перенапряженные митохондрии, могут помочь уменьшить побочный ущерб, который эти ключевые клетки наносят при тяжелом COVID-19 и, возможно, при других критических состояниях.
Цитирование: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Ключевые слова: COVID-19, нейтрофилы, митохондрии, воспаление, критическое состояние