Clear Sky Science · ru
Синтез и биологическая оценка шифтовых комплексов ибупрофена/о‑ванилина с противовоспалительной, антипролиферативной и анти‑SARS‑CoV‑19 активностью
Зачем модернизировать хорошо знакомое обезболивающее
Ибупрофен — одно из самых широко используемых в мире средств от боли и температуры, но при длительном применении он может раздражать желудок и изначально не был создан для борьбы с инфекциями, раком или новыми вирусами. В этом исследовании химики переработали ибупрофен: присоединили к нему природное, напоминающее ваниль соединение и затем связали с разными металлами. В результате получилась серия новых соединений, которые действуют не только как обезболивающие, но и как потенциальные антибиотики, противораковые и противовоспалительные средства, а также как ингибиторы ключевого фермента SARS‑CoV‑2, при этом давая подсказки о том, как проектировать более умные лекарства на основе повседневных препаратов.
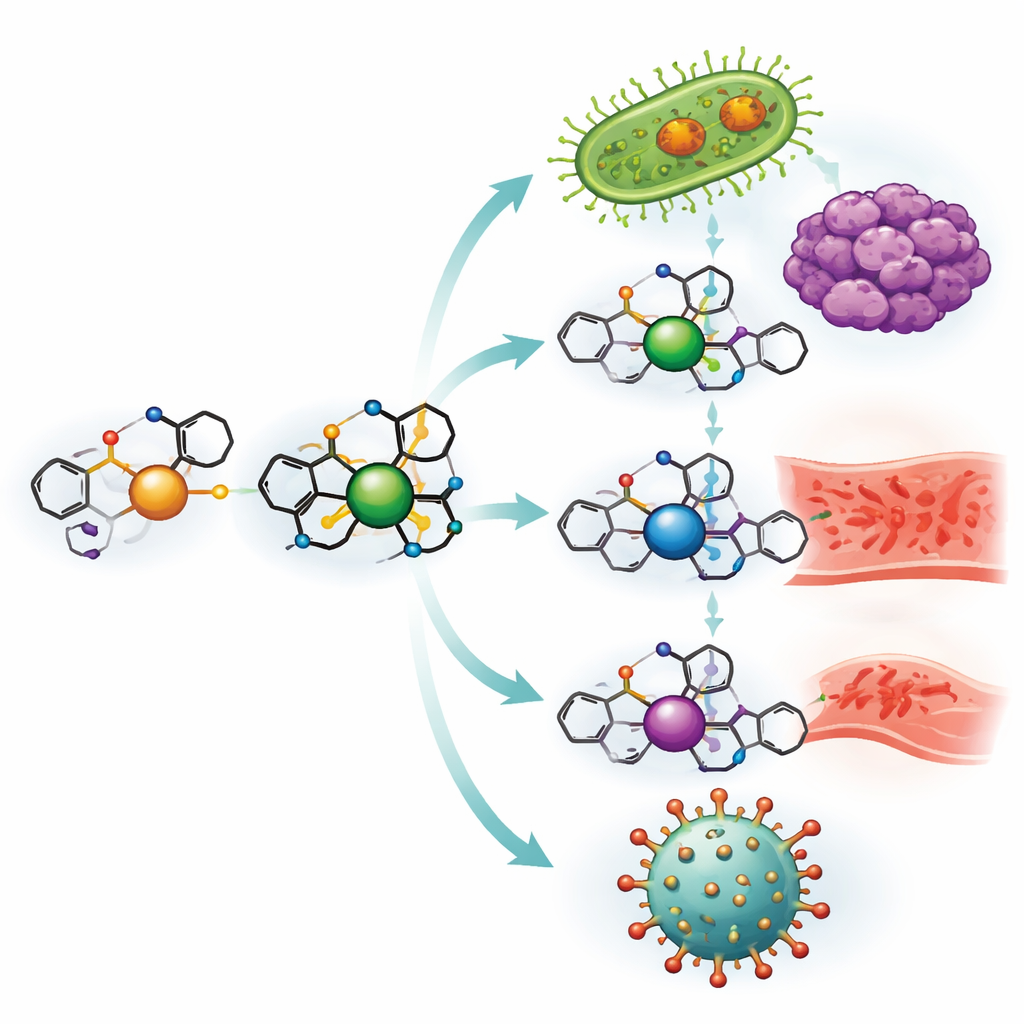
Создание новых похожих на лекарства молекул из ибупрофена
Команда начала с превращения ибупрофена в более универсальный строительный блок и затем связала его с о‑ванилином, близким по структуре соединением к ароматическому компоненту ванили. Вместе они образуют «шифтовую основу» (Schiff base) — по сути, специализированный «хват», который может удерживать ионы металлов. Этот лигант отдельно комбинировали с солями меди, никеля, цинка и ванадия, получив четыре различных металлических комплекса. Тщательные лабораторные испытания, включая измерения поведения при плавлении, поглощения света, магнитных свойств и кристаллической структуры, подтвердили, как лигант обвивает каждый металл и насколько устойчивы полученные комплексы, даже при высоких температурах и в широком диапазоне кислотности.
Как комплексы взаимодействуют с клетками и ДНК
Поскольку эффективность препарата часто зависит от того, как он встречается с биологическими мишенями, исследователи изучили взаимодействие этих новых комплексов с ДНК и живыми клетками. В пробирочных экспериментах особенно медный комплекс прочно связывался с цепочками ДНК и мог повреждать или «расщеплять» их — поведение, часто наблюдаемое у мощных противораковых и антибактериальных агентов. При проверке против линий раковых человеческих клеток из опухолей груди, толстой кишки и печени все четыре комплекса оказались токсичнее для раковых клеток, чем сам ибупрофеновый лиганд, при этом медный комплекс по силе подходил к химиотерапевтическому препарату винбластину при сопоставимых дозах.
Борьба с микробами, грибами и воспалением
Те же соединения подвергли испытаниям против обычных патогенных микробов, включая грамположительные и грамотрицательные бактерии, а также два проблемных гриба. Опять же, металлические комплексы превзошли свободный лиганд, и лидером оказалась медь, сильно ингибирующая и бактерии, и грибы. Авторы интерпретируют это через призму теории хелатирования: когда металл удерживается лигандом, его заряд частично экранируется и весь комплекс становится более липофильным, что позволяет ему проникать через мембраны микроорганизмов и нарушать жизненно важные ферменты. В простом тесте на воспаление, основанном на денатурации белка яйца, новые комплексы также эффективнее снижали денатурацию белка, чем сам ибупрофен, что указывает на возможность подавления воспалительных процессов при более низких дозах.
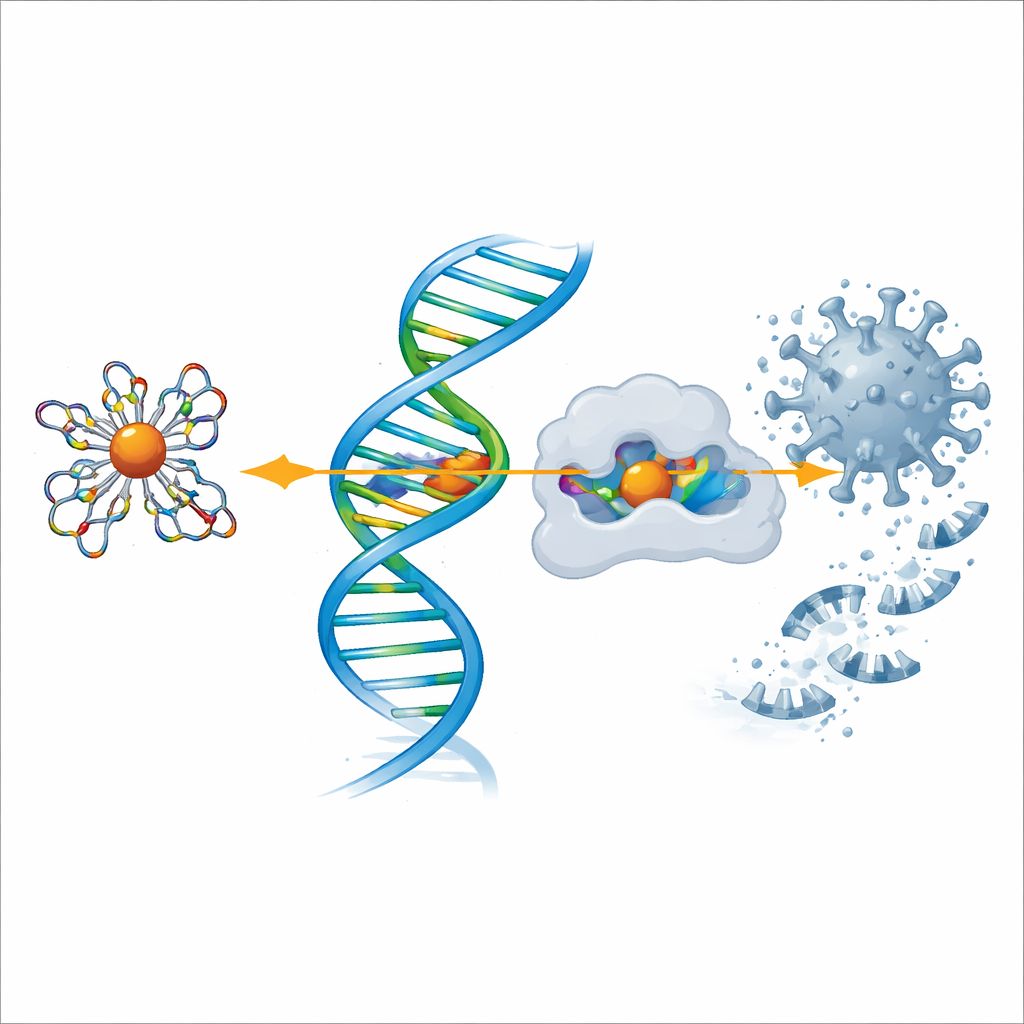
Изучение действия против COVID‑19 и ферментов боли
Чтобы оценить антивирусный потенциал, команда использовала компьютерное моделирование для докинга лиганда и каждого металлического комплекса в трехмерные структуры двух ключевых белков: главной протеазы SARS‑CoV‑2, которой вирус разрезает свои полипротеиды, и циклооксигеназы‑2 (COX‑2), фермента, вовлеченного в боль и воспаление. Симуляции показали, что комплексы, особенно медные и цинковые, удачно встраивались в активные карманы этих белков и образовывали многочисленные стабилизирующие взаимодействия. Чем более отрицательная рассчитанная энергия связывания, тем сильнее предсказанная аффинность, и снова медный комплекс выделялся, за ним следовали цинк и никель, что поддерживает лабораторные наблюдения по противовоспалительному и антимикробному действию.
Что это может означать для будущих лекарств
В целом работа показывает, что хорошо знакомый безрецептурный препарат можно превратить в многоцелевой химический инструмент, объединив его с тщательно выбранным органическим партнером и подходящим ионом металла. Среди четырех испытанных металлов медь дала наиболее перспективного кандидата с выраженными антибактериальными, противогрибковыми, противораковыми, противовоспалительными и по моделям — противо‑SARS‑CoV‑2 активностями, тогда как никель и цинк показали несколько более мягкие, но все же заметные эффекты. Хотя эти результаты пока получены на уровне лаборатории и компьютерного моделирования, они указывают на стратегию, при которой повседневные препараты «апгрейдят» в таргетные металлические комплексы, способные действовать при более низких дозах и на более широкий спектр заболеваний, чем исходные лекарства.
Цитирование: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Ключевые слова: производные ибупрофена, металлические лекарственные комплексы, противораковые препараты, антимикробная терапия, протеаза COVID-19