Clear Sky Science · ru
Структурная основа транспорта простагландинов и лекарств через SLCO2A1
Как молекулярный привратник формирует эффекты лекарств и гормонов
Многие повседневные препараты и молекулы, подобные гормонам, должны пройти через крошечные ворота в наших клетках, прежде чем начать действовать. В этой работе изучается один такой шлюз — белок SLCO2A1, который помогает переносить мощные сигнальные липиды простагландины и несколько распространённых лекарств внутрь клеток. Раскрывая трёхмерную структуру этого белка и то, как он захватывает свой груз, исследователи показывают, почему одни препараты проходят через него, а другие просто блокируют ворота. Эти знания могут направлять создание более безопасных лекарств и новых методов лечения состояний, связанных с воспалением, болью, заболеваниями кишечника и плохим заживлением ран.
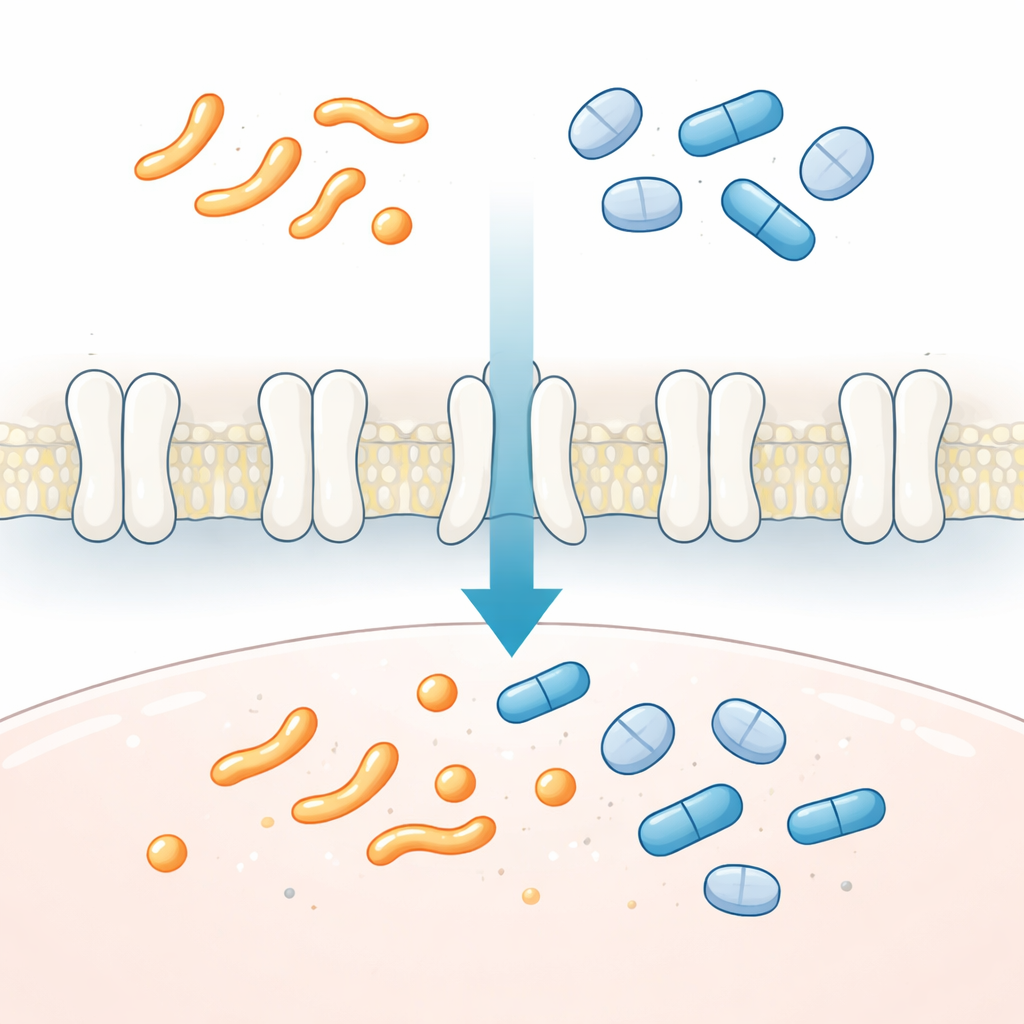
Контролёр трафика в организме для сигналов боли и воспаления
Простагландины — короткоживущие липиды, похожие на гормоны, которые регулируют воспаление, боль, жар, кровообращение и развитие органов. Они действуют рядом с местом синтеза и должны быстро удаляться после выполнения своей функции. SLCO2A1 располагается в клеточной мембране и помогает забирать простагландины и родственные молекулы, такие как тромбоксаны, из внеклеточной жидкости внутрь клетки, где их можно разрушить. При нарушении этого транспорта уровни простагландинов могут оставаться аномально высокими. Наследственные дефекты SLCO2A1 связаны с редкими заболеваниями избыточного роста костей и кожи, хроническими заболеваниями кишечника и плохим заживлением язв. Поскольку простагландины и многие широко применяемые препараты используют этот путь проникновения в клетки, понимание работы SLCO2A1 важно для прогнозирования эффектов лекарств и побочных действий по всему организму.
Увидеть ворота в атомных деталях
Чтобы выяснить, как SLCO2A1 распознаёт и перемещает свой груз, команда использовала криогенную электронную микроскопию — метод, позволяющий получать изображения замороженных белков с почти атомным разрешением. Они исследовали близкий по свойствам белок крыс, который ведёт себя очень похоже на человеческий. Получены структуры белка в комплексе с двумя натуральными простагландинами и с четырьмя лекарствами, применяемыми при астме, высоком давлении, воспалении и болезни Паркинсона. Во всех этих снимках SLCO2A1 представлен как пучок из двенадцати мембранных спиралей, образующих центральную полость, открытую к наружной стороне клетки. Простагландины располагаются глубоко в этой полости: их кольцевое ядро соседствует с группой ключевых аминокислот, а жировые хвосты проходят в основном по маслянистой борозде, соответствующей их липидной природе.
«Рукоять», которая выбирает, что проходит
Сравнивая структуры и проводя длительные компьютерные симуляции, исследователи выделили признаки, позволяющие SLCO2A1 отличать истинный груз от похожих молекул. Положительно заряженная аминокислота аргинин 561 и рядом расположенные триптофан и фенилаланин формируют ключевую «рукоять» для отрицательно заряженного конца простагландинов. При мутациях этих остатков транспорт практически прекращается, что демонстрирует критическую важность этого контакта. Окружающая полость в основном гидрофобна, что благоприятствует маслянистым, любящим мембрану молекулам, и содержит «полосу», действующую как шарнир во время смены формы белка. Два препарата, зафирлукаст и лозартан, фактически транспортируются, потому что они имитируют то, как простагландины предъявляют отрицательную группу аргинину, одновременно взаимодействуя с теми же гидрофобными поверхностями. В отличие от них, противовоспалительный фентиазац и препарат от болезни Паркинсона толкапоне связываются менее плотно и не стабилизируют нужную позу, поэтому они блокируют сайт, вместо того чтобы пройти через него.
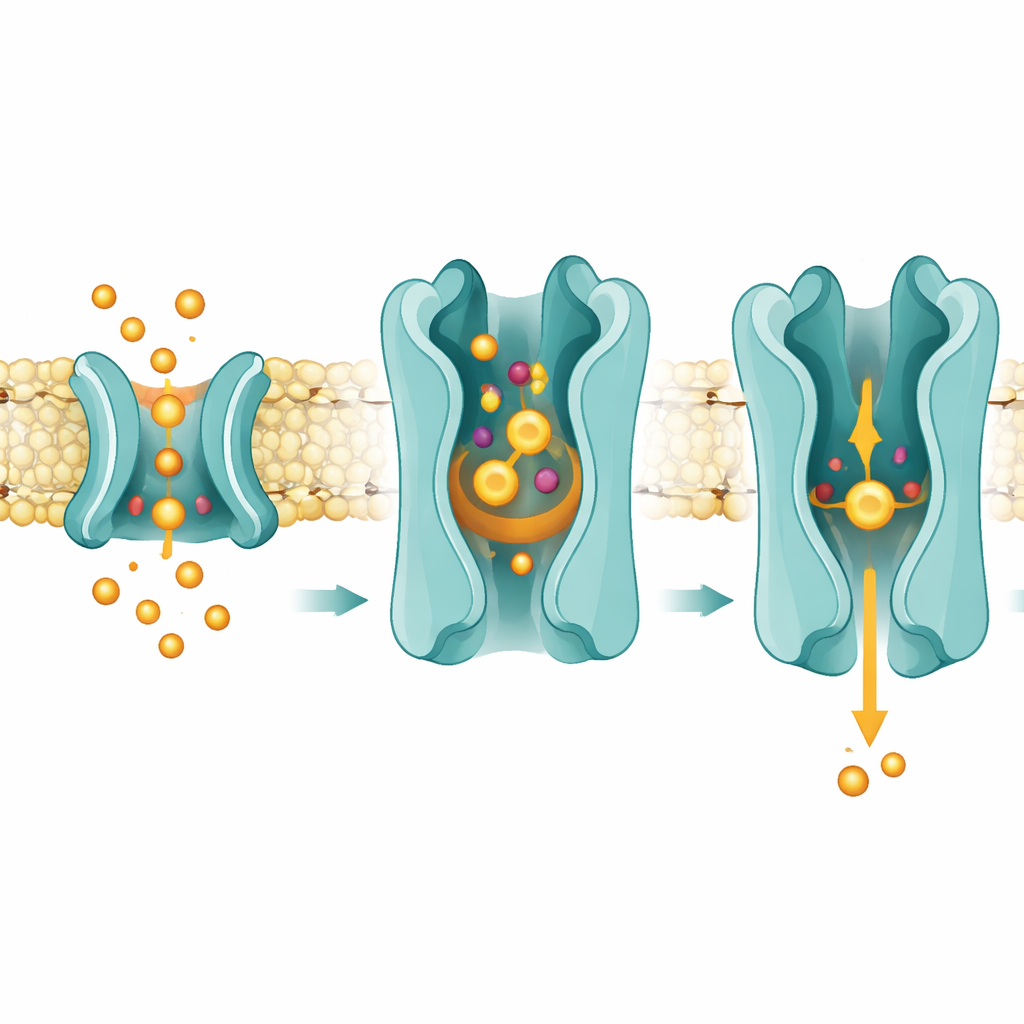
Боковая дверь через мембрану
Структуры также указывают на то, что простагландины попадают в SLCO2A1 не из открытой водной фазы, а скользя боком через жировое ядро мембраны. Исследователи наблюдали электронные плотности, соответствующие липидоподобным молекулам, расположенным в боковом отверстии между двумя спиралями, прямо над местом связывания простагландинов. Болезнетворные мутации и функциональные тесты обозначили эту область как ключевую для транспорта. Предложенный механизм таков: простагландины сначала растворяются во внешнем листке мембраны, затем просачиваются в транспортер через это отверстие. Оказавшись в центральном кармане, они разрушают консервативный солевой мост между аргинином 561 и остатком глутамата, что, в свою очередь, способствует тому, чтобы транспортер качнулся из состояния, открытого наружу, в состояние, открытое внутрь, выпуская простагландин в сторону внутреннего листка мембраны и клеточной внутренности.
Почему это важно для лекарств и болезней
Главный вывод для неспециалиста состоит в том, что SLCO2A1 действует как тонко настроенные ворота, регулирующие, насколько быстро химические сигналы боли, жара и воспаления отключаются, а также каким образом некоторые лекарства попадают в клетки. Это исследование показывает в молекулярных деталях, как ворота распознают простагландины и почему только некоторые препараты могут «попутно» транспортироваться, в то время как другие заклинивают дверь. Отображая ключевые контактные точки и боковой вход через мембрану, работа предоставляет чертёж для проектирования новых препаратов, которые либо эффективно используют эту транспортную систему, либо намеренно блокируют её контролируемым образом. В конечном счёте такие знания могут улучшить терапию воспалительных заболеваний, расстройств кишечника, связанных с дисбалансом простагландинов, и режимов приёма лекарств, где взаимодействия с транспортёром сейчас приводят к непредсказуемым реакциям.
Цитирование: Joshi, C., Deme, J.C., Nakamura, Y. et al. Structural basis for prostaglandin and drug transport via SLCO2A1. Nat Commun 17, 2285 (2026). https://doi.org/10.1038/s41467-026-70227-3
Ключевые слова: транспорт простагландинов, транспортёры лекарств, SLCO2A1, мембранные белки, структура крио-ЭМ