Clear Sky Science · ru
Каталитическое асимметричное функционализирование бицикло[1.1.0]бутановых борановых эфиров, обеспеченное 1,2‑перемещением кислорода
Почему важны крошечные квадратные кольца
Химики любят собирать новые лекарства и материалы, соединяя маленькие молекулярные кусочки, как кубики Лего. Четырёхчленные углеродные кольца — циклобутаны — особенно ценны, потому что в небольшом объёме они аккумулируют много энергии и определённую форму, что может сильно менять поведение препарата в организме. В статье описан новый способ получения таких колец в очень контролируемой «одно‑ручной» (хиральной) форме с помощью хитроумной реакции, которая заставляет содержащую кислород группу перескочить с одного атома на соседний. Эта работа открывает возможности для проектирования более сложных и точных молекул для фармации и прогрессивных материалов.
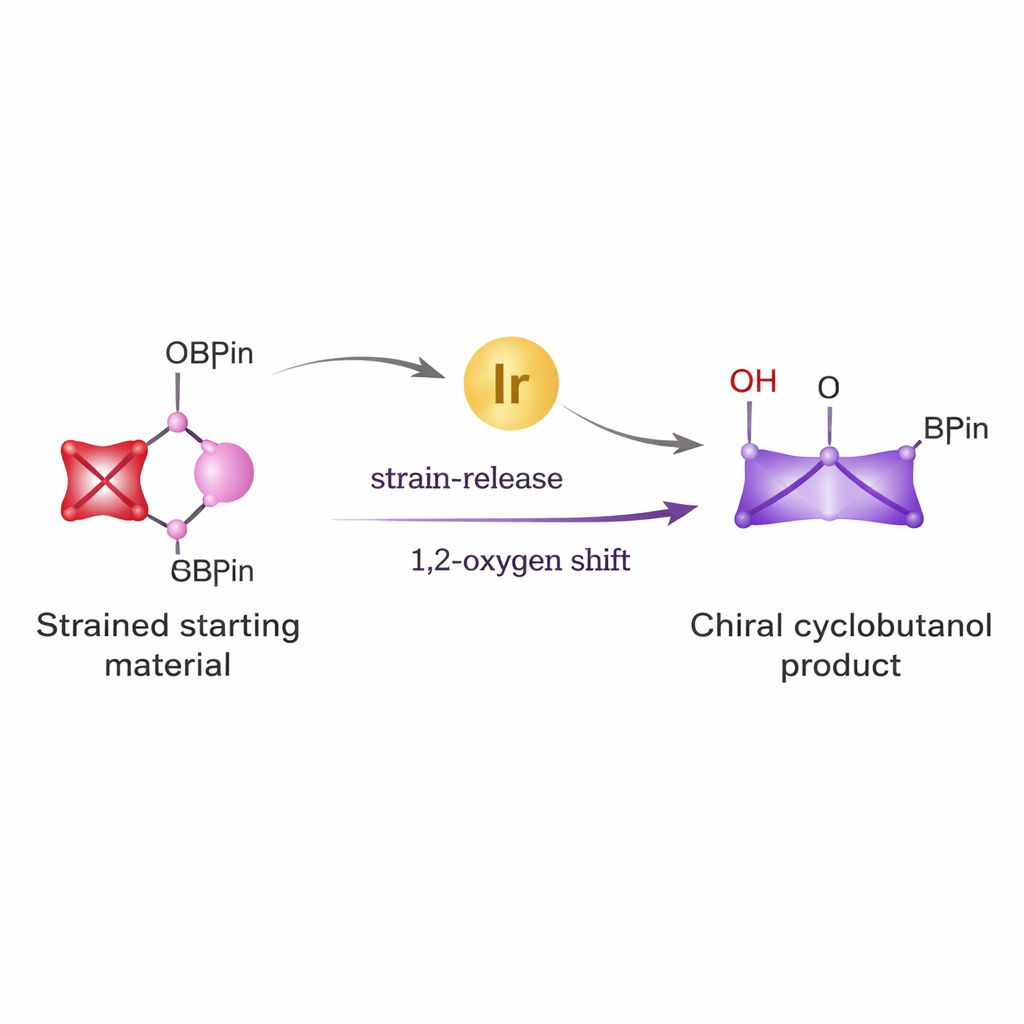
От простых строительных блоков к мощным кольцам
Циклобутаны встречаются в различных противовирусных средствах, кандидатах на противораковую терапию и других биоактивных молекулах. Тем не менее получить их с нужной трёхмерной организацией, требуемой для лекарств, было непросто. Традиционные пути часто требуют жёстких реагентов и дают смеси зеркально‑симметричных продуктов, которые трудно разделить. Авторы решили решить эту проблему, объединив две сильные идеи: необычную реактивность крошечного, сильно напряжённого кольца бицикло[1.1.0]бутана и универсальность борановых эфиров — хорошо известных реагентов, широко используемых в реакциях кросс‑спаривания для образования углерод‑углеродных связей.
Преобразование недостатка в новый реакционный путь
В стандартных каталитических реакциях с участием металлов борановые эфиры образуют промежуточный комплекс с алкоксидом (основанием на кислородной основе). Этот комплекс почти всегда следует избитому пути — трансметаллированию, которое затем ведёт прямо к новым связям углерод–углерод или углерод–галоид. Этот «дефолтный» маршрут затруднял изучение других возможностей, например смещение самой кислородной группы. Команда поняла, что если начать с боранового эфира бицикло[1.1.0]бутана, внутреннее напряжение маленького кольца можно использовать, чтобы переиграть обычный путь. Сочетая эту напряжённую систему с иридиевым катализатором и тщательно подобранным хиральным лигандом, они надеялись направить миграцию кислорода контролируемо, пока кольцо раскрывается и вновь замыкается в циклобутан.
Пошаговый танец под руководством напряжения
Эксперименты подтвердили, что стратегия работает. Используя литиевые алкоксиды, полученные из широкого круга спиртов — в том числе сахаров, терпенов, стероидов и простых алифатических спиртов — авторы превратили борановые эфиры бицикло[1.1.0]бутана в цис‑циклобутанолы с высоким выходом и отличным контролем хиральности. Иридиевый катализатор сначала формирует реактивный аллиловый комплекс из аллилового карбоната‑со‑участника. Этот комплекс затем атакует напряжённую систему бицикло[1.1.0]бутана, формируя новую углерод‑углеродную связь при открытии крошечного кольца. Важно, что вместо немедленного следования привычному пути трансметаллирования, получающийся боросодержащий промежуточный продукт подвергается тонкому вращению вокруг связи углерод–бор, что позиционирует присоединённую кислородную группу так, чтобы она могла чисто перескочить на соседний атом углерода. Это 1,2‑перемещение кислорода фиксирует желаемое цис‑расположение в новом циклобутановом кольце.
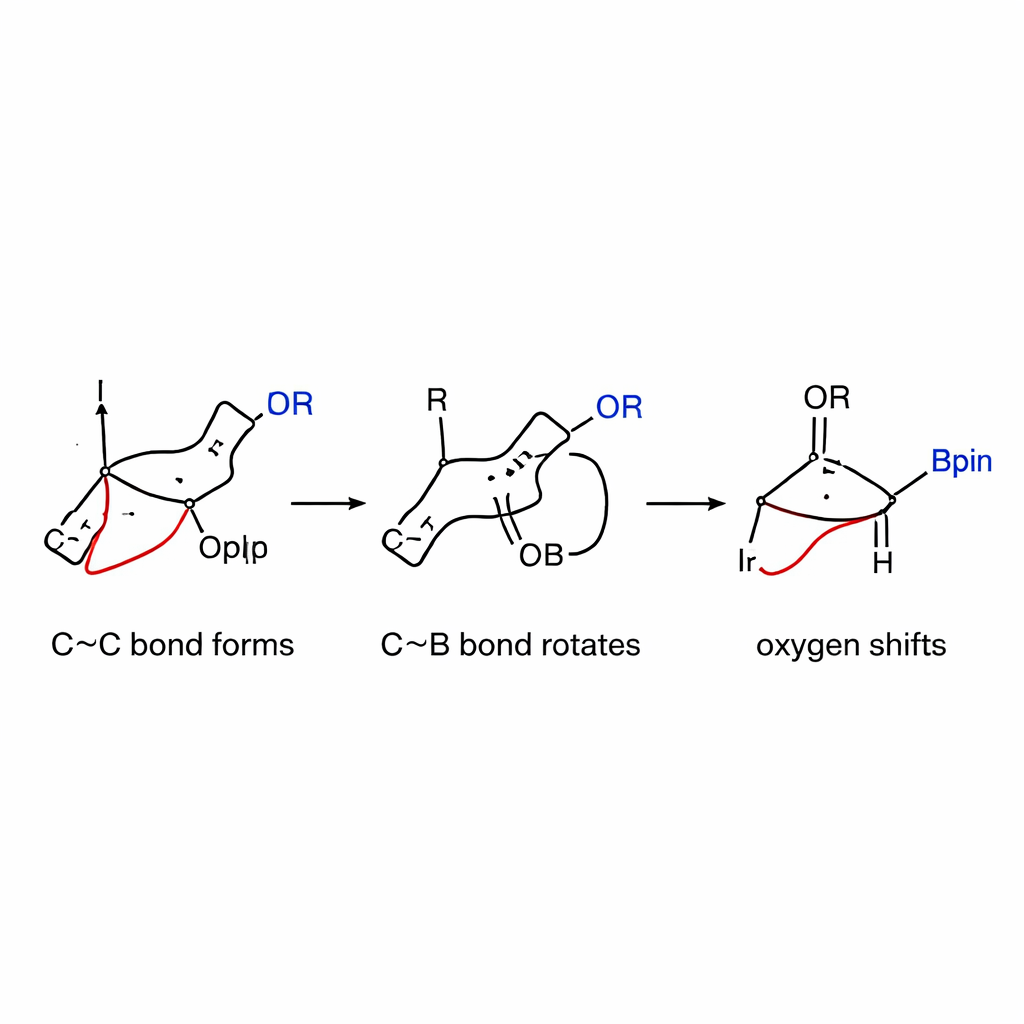
Заглядывая под капот механизма
Чтобы понять, почему реакция столь селективна, авторы совместили кинетические измерения с подробными компьютерными моделями. Они выяснили, что медленной, лимитирующей скоростью стадией является начальное образование углерод‑углеродной связи между иридий‑аллиловым видом и напряжённым боранатным комплексом, а не ранняя активация аллилового карбоната. Электронные тесты показали, что аллил‑партнёры, стабилизирующие положительный заряд, реагируют быстрее, что поддерживает механизм с образованием частично заряженного промежуточного состояния. Расчёты дополнительно показали, что вращение вокруг связи углерод–бор — ранее считавшееся затруднительным — имеет в этой системе необычно низкий энергетический барьер благодаря накопленному напряжению кольца. Как только вращение выравнивает кислородную группу, 1,2‑сдвиг проходит гладко и предпочтительно даёт цис‑продукт, а не более распространённую транс‑форму.
Новые инструменты для создания будущих лекарств
Помимо подтверждения механистической идеи, реакция даёт универсальные продукты. Циклобутанолы сохраняют борановый эфир, который можно превратить во множество других функциональных групп с помощью уже отработанных приёмов. Авторы продемонстрировали многочисленные «поздние» модификации, такие как гидрирование, окисление, метатезис олефинов и дальнейшие сопряжения, при этом сохраняя точную трёхмерную форму кольца. Проще говоря, эта работа превращает некогда проблемный боковой путь — миграцию кислорода в боратовых комплексах — в мощный синтетический инструмент. Используя напряжение кольца и тонко настроенный иридиевый катализатор, исследователи предоставляют химикам надёжный способ собирать сложные хиральные циклобутаны, которые могут сыграть ключевую роль в лекарствах следующего поколения и передовых молекулярных материалах.
Цитирование: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Ключевые слова: циклобутан, органоборонная химия, асимметричный катализ, бициклобутан, перемещение кислорода