Clear Sky Science · ru
Ассоциированные с опухолью CD19+ макрофаги формируют иммуносупрессивную микросреду при гепатоцеллюлярной карциноме
Почему защитники организма иногда помогают раку печени
Рак печени — одно из самых смертоносных заболеваний в мире, отчасти потому что опухоли умеют обращать иммунную систему организма против него самого. В этом исследовании обнаружен неожиданный подтип иммунных клеток в опухолях печени, которые вместо того чтобы бороться с раком, активно помогают ему скрываться и развиваться. Понимание того, кто эти «предательские» клетки и как они действуют, открывает новые пути для повышения эффективности иммунотерапии у пациентов с гепатоцеллюлярной карциномой, самой распространённой формой рака печени.
Особая группа иммунных клеток внутри опухолей
Авторы сосредоточили внимание на опухоле-ассоциированных макрофагах — иммунных клетках, которые обычно «поедают» микробы и мусор, но нередко оказываются коррумпированными в опухолевой среде. Анализируя образцы печёночных опухолей многих пациентов, исследователи выявили отдельную подгруппу макрофагов, несущих на поверхности молекулу CD19, которая обычно характерна для В-клеток, а не для макрофагов. Эти CD19-положительные макрофаги были значительно более многочисленны в опухолях печени по сравнению с рядом здоровой ткани печени или кровью и также обогащались в нескольких других солидных опухолях. Анализы на уровне отдельных клеток подтвердили, что это именно макрофаги с уникальным генным и белковым профилем, а не ошибочно идентифицированные В-клетки.
Как эти клетки формируют благоприятную для опухоли среду
У пациентов, чьи опухоли содержали много CD19-положительных макрофагов, как правило, отмечались более крупные, агрессивные опухоли и более короткое выживание. Образцы опухолей, богатые этими клетками, демонстрировали меньше CD8+ Т-клеток-киллеров и больше регуляторных T-клеток — картину, типичную для выраженной иммуносупрессии. В мышиных моделях добавление CD19-положительных макрофагов к клеткам рака печени приводило к ускоренному росту опухолей и снижению числа полезных Т-клеток, одновременно увеличивая другие супрессивные миелоидные клетки. Что важно, когда исследователи использовали генетически модифицированные Т-клетки, распознающие CD19, чтобы селективно уничтожать эти макрофаги, опухоли печени уменьшались даже у мышей, лишённых нормальных В-клеток, что указывало именно на макрофаги как терапевтическую мишень.
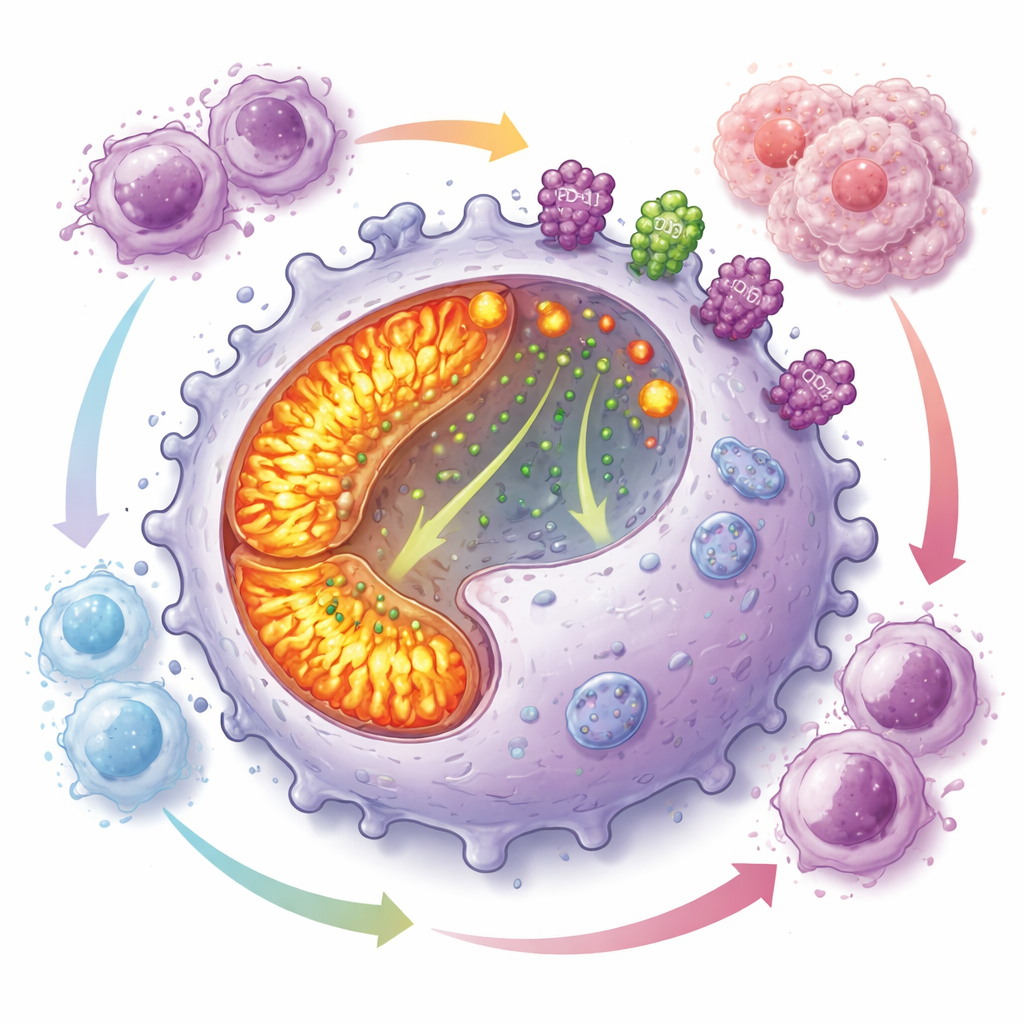
Энергозатратная программа, которая подавляет иммунный ответ
Глубже изучив эти клетки, группа обнаружила, что CD19-положительные макрофаги работают с внутренними «электростанциями» на высоких оборотах. Их митохондрии — органеллы, производящие энергию — были многочисленнее и активнее, чем у других макрофагов, с повышенной окислительной фосфорилизацией и образованием реактивных форм кислорода. Несмотря на такое энергетическое состояние, эти клетки плохо фагоцитировали мишени, но быстро делились, что способствовало их накоплению в опухоли. Одновременно на их поверхности экспрессировались высокие уровни PD-L1 и CD73 — двух молекул, известных способностью подавлять Т-клеточные ответы и генерировать аденозин, малое соединение, мощно ослабляющее иммунитет. Совместные культуры показали, что эти макрофаги сильно ингибируют пролиферацию нескольких типов Т-клеток.
Главный переключатель за программой «предательских» макрофагов
Исследователи выявили фактор транскрипции PAX5 как центральный драйвер этой вредоносной программы макрофагов. PAX5 наиболее известен своей ролью в развитии В-клеток, но здесь он был высокоактивен в CD19-положительных макрофагах. Вынужденная экспрессия PAX5 в макрофагоподобных клетках усиливала образование митохондрий, повышала производство энергии и повышала уровень белков — но не мРНК — PD-L1, CD73 и CD19. Механистические эксперименты показали, что PAX5 перемещает кальций в митохондрии, снижая его содержание в цитозоле и препятствуя транслокации ключевого регулятора TFEB в ядро. При удержании TFEB в цитоплазме падает биогенез и функция лизосом, поэтому белки вроде PD-L1 и CD73 перестают эффективно деградироваться и накапливаются на поверхности клетки, усиливая иммуносупрессию.
От открытия к лучшим вариантам лечения
Поскольку эти макрофаги сильно зависят от активности CD73 и митохондриального метаболизма, авторы проверили, помогут ли блокирование этих путей улучшить иммунотерапию. В модели рака печени у мышей сочетание блокировки PD-L1 с антителами к CD73 или с ингибитором CD73 приводило к уменьшению опухолей, увеличению инфильтрации Т-клеток и снижению пролиферации раковых клеток. Аналогично, сочетание антител к PD-L1 с ингибитором митохондриальной окислительной фосфорилизации улучшало контроль над опухолью и повышало вход иммунных клеток в опухоль. Поразительно, эти преимущества исчезали у мышей с макрофагами, лишёнными PAX5, что подтвердило, что эффект препаратов связан с подавлением программы CD19-положительных макрофагов, зависящей от PAX5. В целом работа указывает на то, что селективное нацеливание на эту подгруппу макрофагов — через CD19-ориентированные клеточные терапии, ингибирование CD73 или метаболические препараты — может помочь превратить иммунохолодную опухоль печени в ту, которая гораздо лучше отвечает на существующую блокаду контрольных точек.
Цитирование: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Ключевые слова: гепатоцеллюлярная карцинома, опухоле-ассоциированные макрофаги, иммунотерапия, PD-L1 и CD73, митохондриальный метаболизм