Clear Sky Science · ru
Опухолеспецифичное экспрессирование HORMAD1 нарушает митотическую паузу и повышает чувствительность к ингибиторам митотических киназ
Почему это важно для лечения рака
Когда наши клетки делятся, они полагаются на сложные механизмы контроля, чтобы передать правильный набор хромосом. Рак часто захватывает или ослабляет эти защитные механизмы, что приводит к хаотичным геномам, которые не только продвигают развитие болезни, но и определяют, как опухоли реагируют на лекарства. В этом исследовании показано, как необычный белок HORMAD1, обычно активный только в репродуктивных клетках, включается во многих агрессивных раках молочной железы и других опухолях. Тонко подрывая ключевой контрольный пункт деления клетки, HORMAD1 делает раковые клетки более нестабильными — но одновременно необычно уязвимыми к новому классу экспериментальных препаратов.
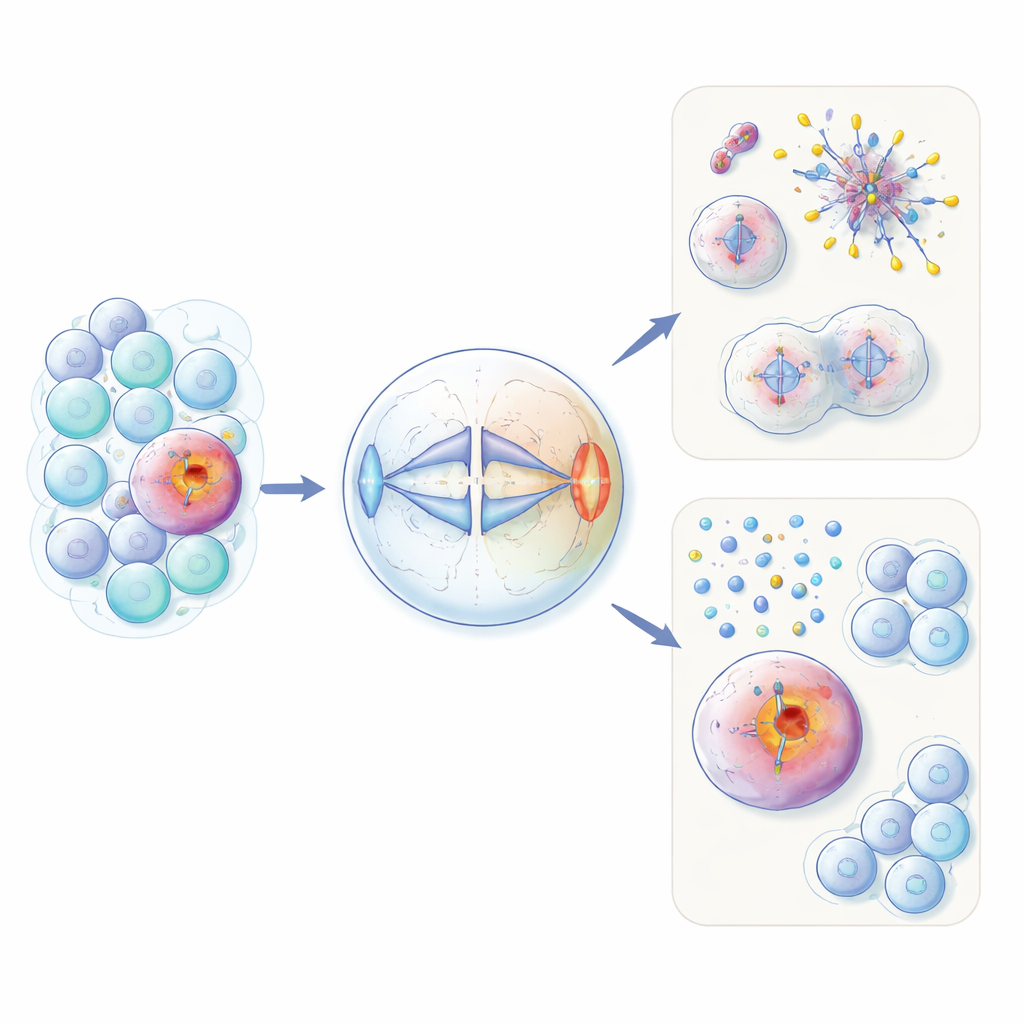
Ненадлежащий белок фертильности в раковых клетках
HORMAD1 обычно встречается только в зародышевых клетках, где образуются яйцеклетки и сперматозоиды. Там он помогает управлять перестройкой ДНК и контролем качества во время особого типа деления — мейоза. Авторы показывают, что примерно в 60% случаев тройного негативного рака молочной железы — а также в подгруппах нескольких других типов опухолей — этот белок неправильно вновь активируется. На моделях как переэкспрессированных незлокачественных клеток, так и раковых линиях исследователи обнаружили, что избыточный HORMAD1 нарушает равномерное распределение хромосом в обычном митозе. Клетки, экспрессирующие HORMAD1, демонстрировали больше отстающих хромосом, дополнительные или отсутствующие хромосомы (анеуплоидия) и небольшие ДНК-содержащие «микроядра» — все признаки геномного хаоса, характерные для агрессивных опухолей.
Как обычно работают проверки деления клетки
Для корректного деления клетка формирует шпиндель из микротрубочек, которые прикрепляются к каждой хромосоме. Система наблюдения, называемая контрольным пунктом сборки веретена (spindle assembly checkpoint), действует как чувствительный к натяжению тормоз: если какая-либо хромосома неправильно прикреплена, тормоз блокирует прогрессию и предотвращает разделение, пока ошибки не будут исправлены. Несколько ферментов, называемых митотическими киназами, включая MPS1, Aurora B и BUB1, помогают обнаруживать плохие прикрепления и способствуют «исправлению ошибок», чтобы каждая дочерняя клетка получила правильный набор хромосом. Нарушение этой системы может как способствовать развитию рака, так и создавать особые уязвимости, на которые можно нацелиться с помощью лекарств.
HORMAD1 тихо ослабляет тормоз
Исследователи обнаружили, что HORMAD1 подрывает этот предохранительный механизм тонким, но значимым способом. Вместо того чтобы вмешиваться в классические компоненты контрольного пункта, такие как HORMA-белок MAD2L1, HORMAD1 связывается напрямую с киназой Aurora B. Aurora B обычно взаимодействует с другим белком, INCENP, чтобы стать полностью активной и модифицировать белки на центромерах и кинетохорах — критических участках хромосом, к которым прикрепляются веретенные волокна. Когда HORMAD1 присутствует в делящихся клетках опухоли, он конкурирует с INCENP за доступ к Aurora B, ослабляя их взаимодействие и снижая активность Aurora B. В результате фосфорилирование обычных мишеней Aurora B ослабляется, исправление ошибок становится менее эффективным, и контрольный пункт становится «протекающим»: клетки преждевременно покидают митоз, даже при наличии дефектных прикреплений, что приводит к неправильному распределению хромосом и геномной нестабильности.
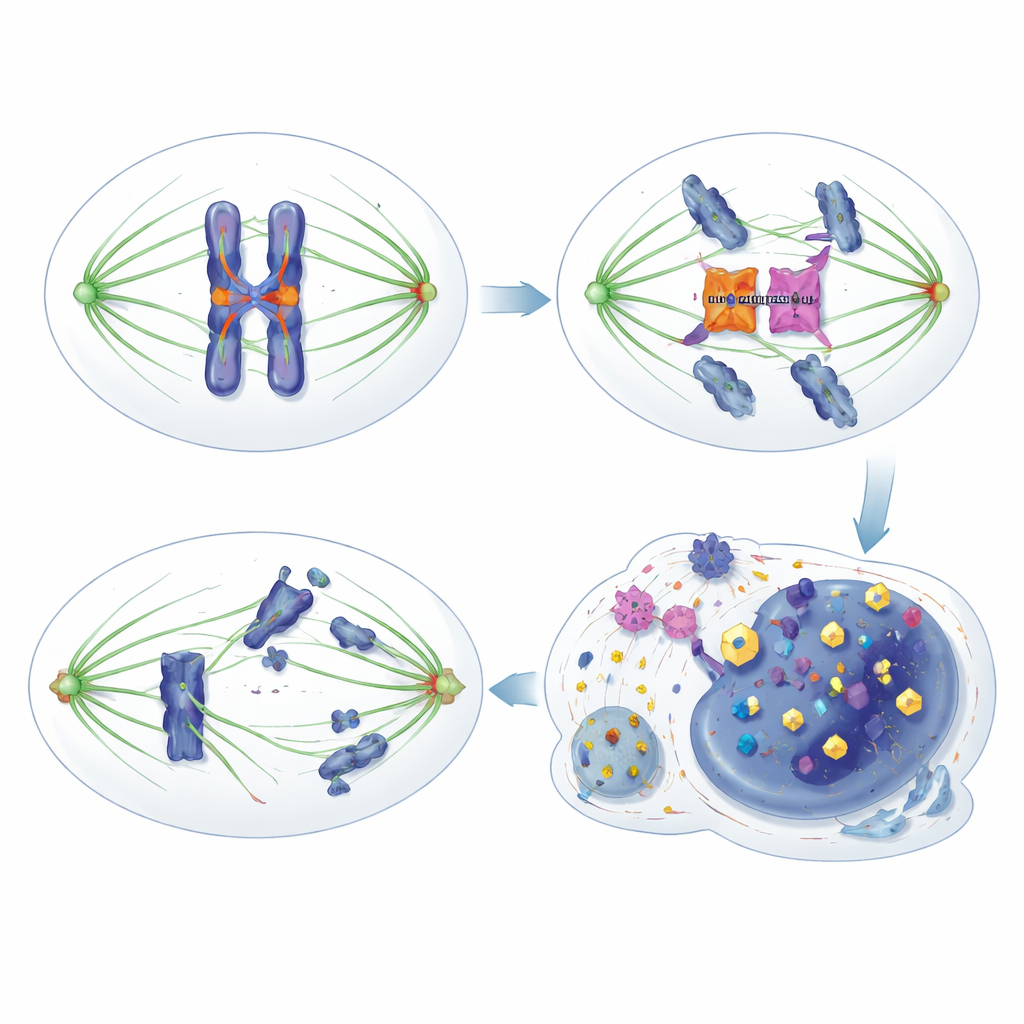
От уязвимости к терапевтической возможности
Поскольку HORMAD1 лишь частично нарушает функцию Aurora B и сопутствующих защит, раковые клетки остаются достаточно жизнеспособными для роста, но сильно зависят от оставшейся активности митотических киназ, чтобы переживать повторяющиеся ошибочные деления. Команда проверила это, обрабатывая HORMAD1-положительные и HORMAD1-отрицательные клетки экспериментальными ингибиторами MPS1, Aurora B и BUB1. Во множестве моделей экспрессия HORMAD1 делала клетки гораздо более чувствительными к этим препаратам, резко снижая их способность к пролиферации и образованию колоний. Генетическое истощение BUB1 оказывало особенно летальный эффект только в присутствии HORMAD1, выявляя сильную селективную зависимость. В моделях на мышах с опухолями тройного негативного рака молочной железы, полученными от пациентов, опухоли с высоким уровнем HORMAD1 уменьшались или росли медленнее при лечении наночастичной формой ингибитора Aurora B, тогда как HORMAD1-отрицательные опухоли в основном сопротивлялись той же терапии.
Что это означает для пациентов
Для непрофессионала HORMAD1 действует как палка о двух концах в раке: он толкает опухолевые клетки к большей хромосомной дезорганизации, что может ускорять болезнь, но в то же время делает их шатко зависимыми от оставшихся механизмов контроля деления. В работе показано, что этот неправильно включённый белок фертильности ослабляет ключевой контрольный пункт, перенаправляя Aurora B, из-за чего опухоли с HORMAD1 особенно уязвимы к препаратам, нацеленным на Aurora B, MPS1 и BUB1. Поскольку HORMAD1 в значительной степени отсутствует в нормальных тканях, но присутствует в чётком подмножестве опухолей, он может служить биомаркером для идентификации пациентов, которые с наибольшей вероятностью получат пользу от этих новых ингибиторов митотических киназ, открывая потенциально новые таргетные подходы в лечении трудно поддающихся терапии опухолей, таких как тройной негативный рак молочной железы.
Цитирование: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Ключевые слова: HORMAD1, тройной негативный рак молочной железы, хромосомная нестабильность, киназа Aurora B, ингибиторы митотического контрольного пункта