Clear Sky Science · ru
Гетеробифункциональные протеомиметические полимеры для целенаправленного разрушения MYC и KRAS
Новые инструменты для устранения самых стойких белков рака
Многие из наиболее опасных онкогенных белков, такие как MYC и KRAS, долгое время считались «нелекуемыми», потому что лекарствам трудно за них зацепиться. В этом исследовании представлен новый тип мягкого синтетического материала — полимеры HYDRAC — которые могут захватывать эти скользкие белки и направлять их в клеточную систему утилизации. Для читателей эта работа даёт представление о том, как химия и нанотехнологии могут открыть варианты лечения для тех видов рака, которые сопротивлялись традиционным препаратам.
Гибкий каркас вместо одной таблетки
Большинство таргетных противораковых препаратов — это малые молекулы, которые вписываются в карманы на поверхности белка, как ключ в замок. Но такие белки, как MYC, часто гибкие и лишены удобных карманов, а KRAS часто мутирует так, что привычные лекарства становятся неэффективны. Авторы разработали длинные цепочечные полимеры, состоящие из повторяющихся звеньев. По этим цепям они прикрепили два типа фрагментов: короткие сегменты, связывающие белок и распознающие, например, MYC или RAS, и «дегрон»-сегменты, привлекающие клеточную утилизационную машину. Поскольку множество копий каждого компонента украшает одну и ту же цепь, отдельная молекула HYDRAC может одновременно достать до нескольких белков и ферментов — то, что трудно реализовать с одной жёсткой малой молекулой.
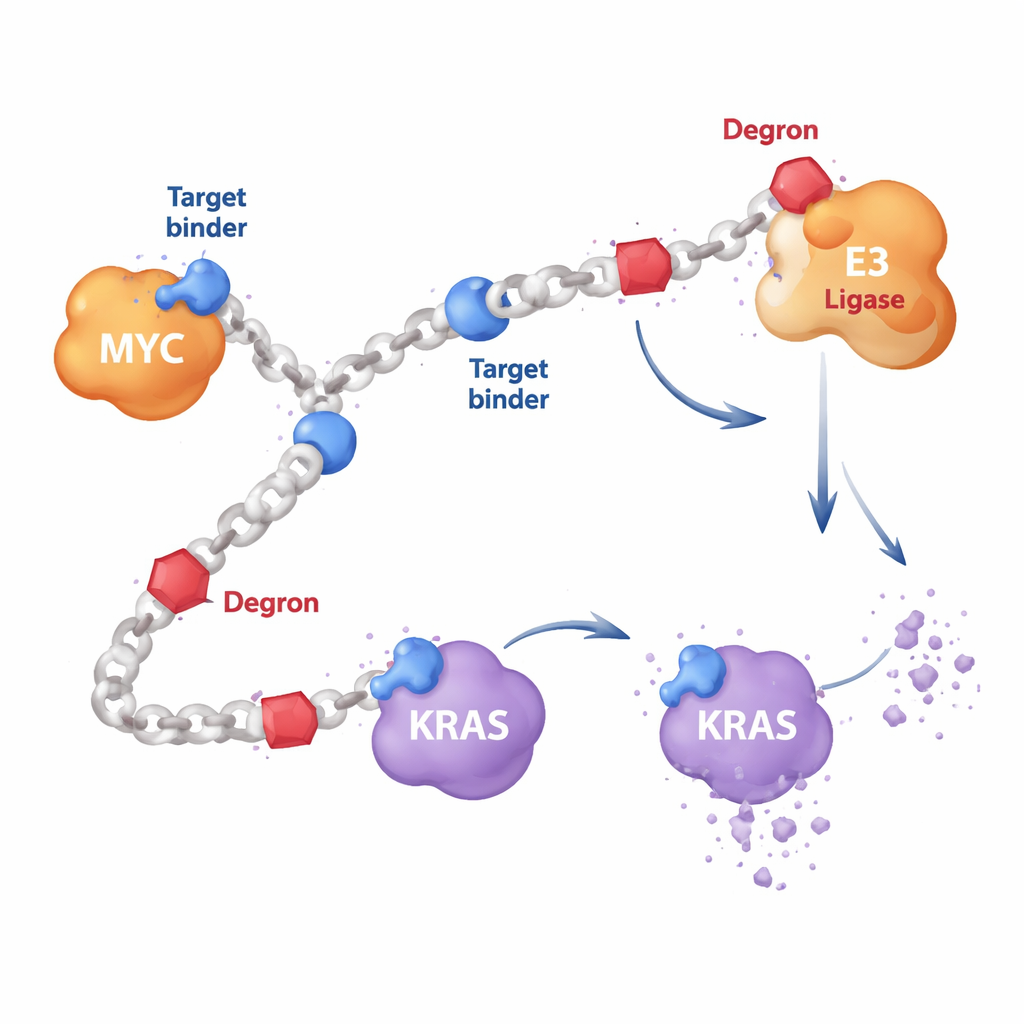
Обучая клетки «пережёвывать» MYC
В первом тесте исследователи сосредоточились на MYC — ключевом регуляторе, который стимулирует рост во многих опухолях, но десятилетиями сопротивлялся прямому воздействию. Они создали полимеры HYDRAC, несущие известный пептид, связывающий MYC, вместе с простым дегрон-мотивом, маркирующим белки для разрушения протеасомой — основным «шредером» белков в клетке. В пробирочных экспериментах эти полимеры складывались в компактные, похожие на белки структуры и прочно связывались с MYC, но не с несвязанными белками. В клеточных культурах HYDRAC легко проникали внутрь, нарушали программы генов, контролируемые MYC, и вызывали гибель клеток — эффекты, зависящие от наличия на той же цепи и таргетирующего, и дегрон-компонента.
От клеточной культуры до уменьшения опухолей
Внутри клеток лечение HYDRAC привело к резкому снижению уровней белка MYC без уменьшения его РНК, что указывает на реальное разрушение, а не на простое подавление экспрессии. Блокирование протеасомы или ключевых ферментов, активирующих определённые пути деградации, восстанавливало уровни MYC, показывая, что полимеры действуют, перенаправляя собственные системы утилизации клетки. Анализы протеома показали, что очень немногие другие белки подвергались изменениям, что свидетельствует о высокой селективности. В мышиных моделях опухолей, зависимых от MYC, флуоресцентно меченые HYDRAC преимущественно накапливались в опухолях после инъекции и оставались там в течение нескольких дней. Повторные дозы замедляли рост опухолей без значительной потери веса или очевидного повреждения тканей, а ткани опухолей показывали меньше делящихся клеток и больше признаков запрограммированной гибели.
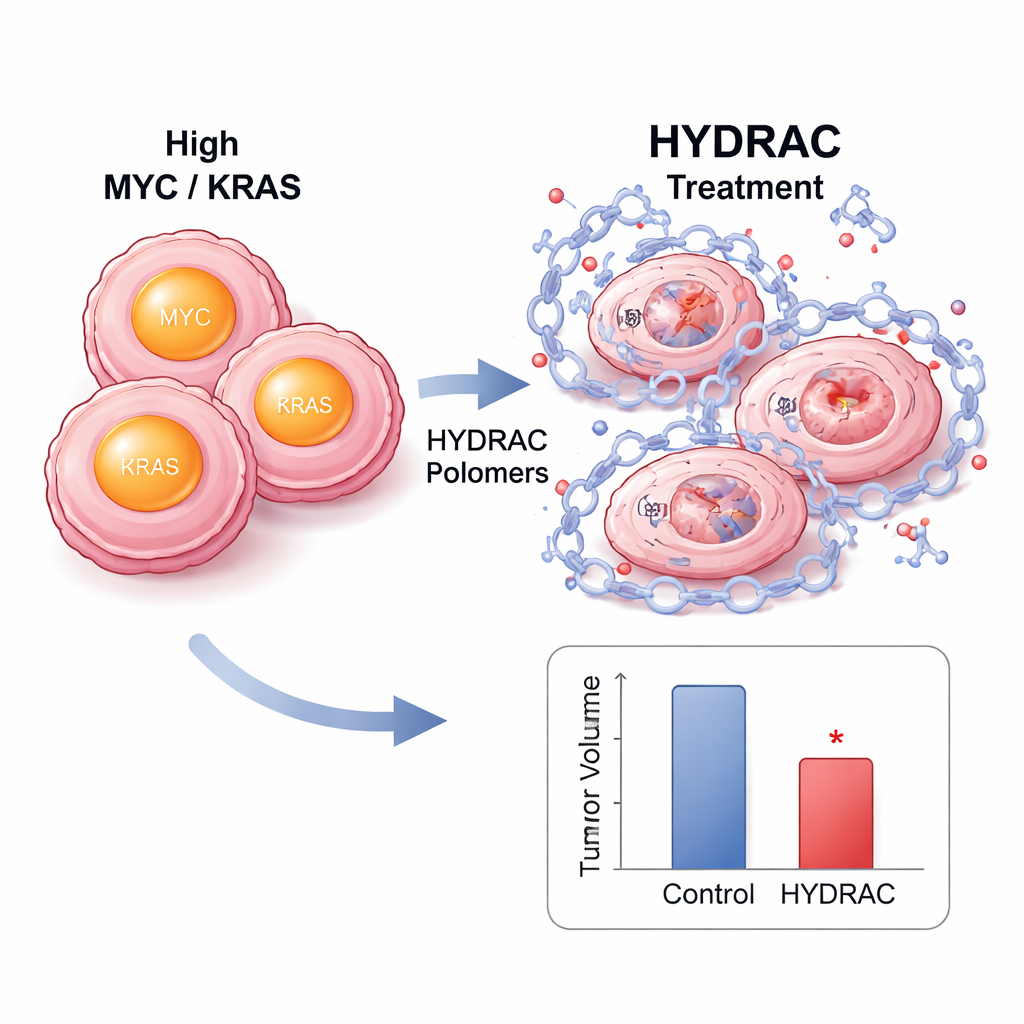
Платформа «включи и используй» для множества мишеней
Одно из преимуществ подхода HYDRAC в том, что его боковые группы можно менять как взаимозаменяемые детали. Команда заменила исходный дегрон другими элементами, привлекающими разные клеточные ферменты, в том числе те, которые распознают препарат талидомид. Каждая версия разрушала MYC только в присутствии и при функциональности соответствующего фермента, подтверждая, что полимеры можно настроить на использование разных внутриклеточных маршрутов. Чтобы проверить обобщаемость, исследователи затем создали HYDRAC, нацеленные на RAS, используя пептид, распознающий белки RAS. Эти конструкции успешно деградировали мутантный KRAS в двух разных линиях раковых клеток, намекая на потенциал «пан-KRAS», не зависящий от конкретной мутации — важный шаг для опухолей, где сосуществует много вариантов KRAS.
Почему это важно для будущего лечения рака
Эта работа вводит HYDRAC как новый класс программируемых материалов, которые не просто блокируют проблемные белки — они помогают клеткам их уничтожать. Сочетая множество таргетирующих и деградационных элементов на гибком полимерном каркасе, HYDRAC обходят ограничения дизайна традиционных малых молекул и PROTAC, которые обычно несут по одному каждому компоненту. Хотя предстоит ещё много работы, прежде чем эти материалы дойдут до клиники, результаты в моделях, управляемых MYC и KRAS, указывают, что долгое время считавшиеся «нелекуемыми» онкобелки могут оказаться уязвимыми, если медицина начнёт выглядеть скорее как настроенная молекулярная щётка, чем как одна малая таблетка.
Цитирование: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Ключевые слова: таргетированное уничтожение белков, MYC, KRAS, полимерные терапевтические средства, наномедицина при раке