Clear Sky Science · ru
Интегративный эпигеномный ландшафт мозгов при болезни Альцгеймера выявляет молекулярные нарушения олигодендроцитов, связанные с тау
Почему это исследование мозга важно
Болезнь Альцгеймера наиболее известна потерей памяти и накоплением двух проблемных белков в мозге: амилоида и тау. Однако у людей с Альцгеймером могут быть очень разные паттерны повреждений, даже при одинаковом диагнозе. В этом исследовании задают ключевой вопрос: какие переключатели внутри клеток мозга определяют, в какой степени накапливаются эти вредные белки и как они влияют на разные типы клеток? Анализируя химические метки на ДНК в сотнях мозгов, исследователи обнаруживают неожиданный связующий фактор между тау и клетками, обеспечивающими работу «проводки» мозга.
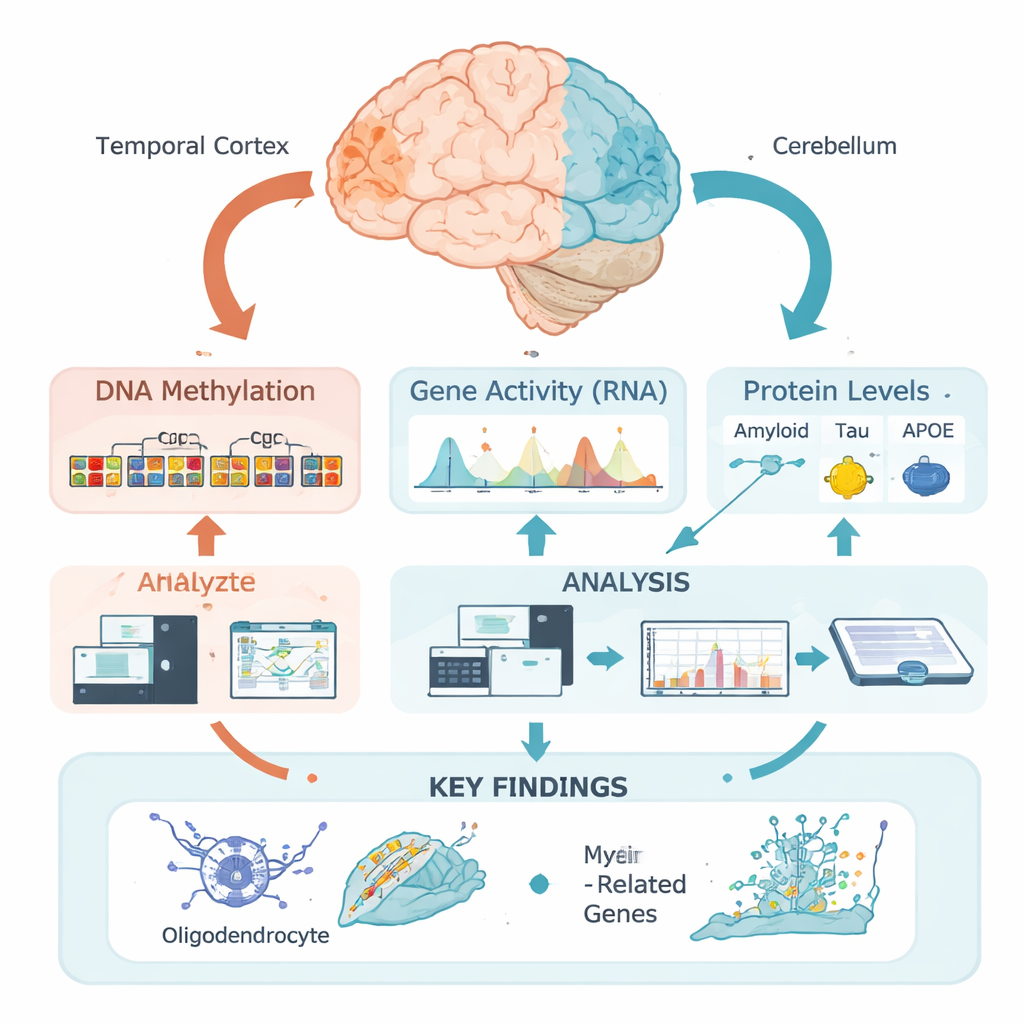
Химические метки на ДНК как скрытые переключатели
Наша ДНК несёт базовые инструкции по построению и функционированию клеток мозга, но эти инструкции регулируются эпигенетическими метками — химическими ярлыками, которые могут усиливать или ослаблять активность соседних генов без изменения генетического кода. Одна из важнейших меток — метилирование ДНК, при котором небольшие химические группы прикрепляются к определённым участкам ДНК. Вместо того чтобы изучать отдельные сайты поодиночке, команда применила новый «региональный» подход: они сгруппировали многие близко расположенные сайты в функциональные зоны на основе упаковки ДНК в височной коре, области, сильно затронутой при Альцгеймере, и в мозжечке, относительно сохраняющемся. Это позволило им спросить, где в биологическом смысле меняются паттерны метилирования в связи с признаками болезни.
Связывание меток ДНК с белками Альцгеймера
Исследователи проанализировали мозговую ткань 472 человек с посмертно подтверждённым диагнозом болезни Альцгеймера. Для каждой пробы височной коры они измеряли детальные уровни амилоида, тау и белка APOE в разных биохимических формах, а также классические микроскопические показатели амилоидных бляшек и тау-сплетений. Затем они провели эпигеномные ассоциативные исследования в масштабе всего генома, проверяя, соотносятся ли региональные уровни метилирования ДНК с этими измерениями. Поразительно, что почти все сильные ассоциации связывались не с амилоидом, а с тау — особенно с общим растворимым тау и с мембраносвязанной фосфорилированной (химически модифицированной) формой, которая, как полагают, обладает особой токсичностью.
Сильный сигнал в клетках «проводки» мозга
Многие области ДНК, связанные с тау, располагались в «активных» участках генома, влияющих на соседние гены. Сопоставив данные о метилировании с измерениями активности генов в тех же образцах, команда показала, что эти регионы часто контролируют гены, используемые олигодендроцитами — клетками, которые обвивают нервные волокна изолирующим миелином, позволяя электрическим сигналам распространяться быстро и надёжно. В этот набор попали ключевые гены, связанные с миелином, такие как MBP, MAG и MYRF, а также ген риска Альцгеймера BIN1 и более новый кандидат LDB3. Более высокие уровни токсичного фосфорилированного тау, как правило, совпадали с повышенным метилированием в этих регионах и пониженной экспрессией соответствующих генов олигодендроцитов и миелина, тогда как более «безвредный» пул растворимого общего тау проявлял противоположную картину.
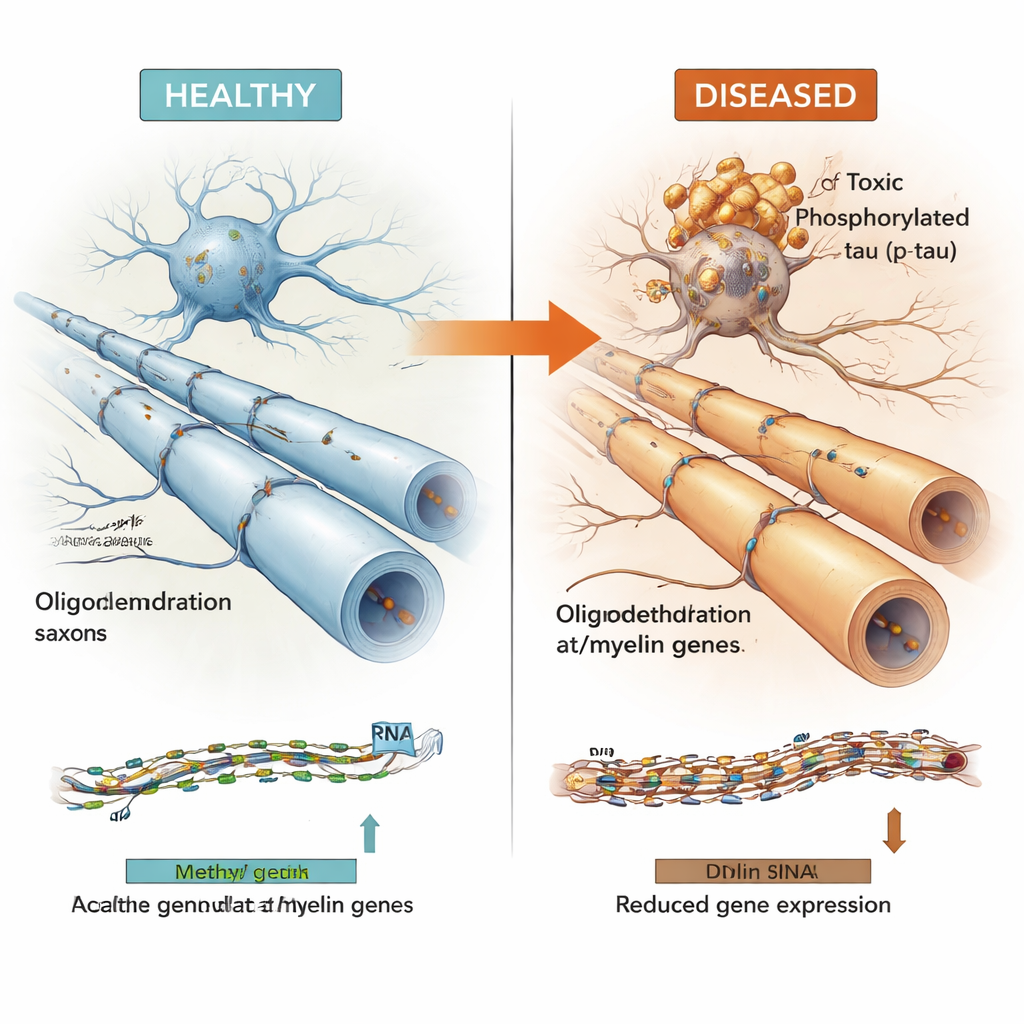
Паттерн, наблюдаемый при нескольких заболеваниях мозга
Чтобы проверить надёжность и общность этих находок, авторы изучили крупные независимые наборы данных из других коллекций мозгов при Альцгеймере и из мозгов, поражённых первичными «тауопатиями», такими как прогрессирующий супрануклеарный паралич и болезнь Пика. Несмотря на то что эти когорты измерялись разными технологиями и часто в разных областях мозга, многие те же регионы ДНК и гены олигодендроцитов демонстрировали согласованное поведение: уровни их метилирования коррелировали с нагрузкой тау-сплетений, а их экспрессия была снижена в больных мозгах и в исследованиях на уровне одиночных клеток, сосредоточенных на олигодендроцитах. Важно, что эти паттерны вряд ли объясняются только генетикой или общим снижением числа клеток, что указывает на подлинный эпигенетический сдвиг в функционировании олигодендроцитов.
Что это значит для понимания болезни Альцгеймера
В целом результаты поддерживают модель, в которой рост уровней вредного тау тесно связан с эпигенетическими изменениями в олигодендроцитах, подавляющими гены, связанные с миелином, что может ослаблять «проводку» мозга и способствовать когнитивному снижению. По-прежнему неясно, что возникает первым — накопление тау или нарушение этих миелиновых генов — но тесные, повторяющиеся ассоциации на тысячах образцов и при нескольких заболеваниях указывают на общий механизм. Сопоставив эти ДНК‑переключатели и объединив их в публичный «Мультиомный атлас», работа выделяет олигодендроциты и их эпигенетическую регуляцию как перспективные мишени для будущих терапий, направленных на стабилизацию мозговых цепей, а не только на нейроны или амилоидные бляшки.
Цитирование: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Ключевые слова: болезнь Альцгеймера, белок тау, метилирование ДНК, олигодендроциты, миелин