Clear Sky Science · ru
Структурные основы передачи сигналов и модуляции человеческого цинк‑активируемого канала (ZAC)
Как следовый металл помогает нервным клеткам общаться
Цинк наиболее известен как питательное вещество в мультивитаминах, но в организме этот металл также действует как быстрый химический посредник в мозге. Описанное здесь исследование раскрывает на атомном уровне, как малоизвестный белок — цинк‑активируемый канал (ZAC) — обнаруживает цинк снаружи клетки и преобразует этот сигнал в электрический ответ. Понимание этого особого «врата» в клеточной мембране может прояснить, как цинк формирует активность мозга и подсказать новые способы тонкой настройки нервных сигналов в норме и при заболеваниях.
Особые ворота для цинковых сигналов
Многие быстрые сообщения между нервными клетками передаются хорошо знакомыми химическими веществами, такими как серотонин или ацетилхолин, которые открывают кольцевые каналы в мембране. ZAC — дальний родственник этих рецепторов, но вместо органического лиганда он включается ионами металлов, такими как цинк, медь и протоны. ZAC присутствует во многих тканях человека, включая мозг, но отсутствует у стандартных лабораторных животных, таких как мыши и крысы, что замедляло прогресс. В этой работе применена высокоразрешающая криоэлектронная микроскопия, чтобы зафиксировать несколько трехмерных снимков человеческого ZAC: в состоянии покоя, с связанным цинком и с двумя разными препаратами, которые закрывают канал. В совокупности эти структуры показывают, где именно цинк садится на вершине канала, как проходят ионы и как блокаторы зажимают ворота или застревают их в не проводящем состоянии.
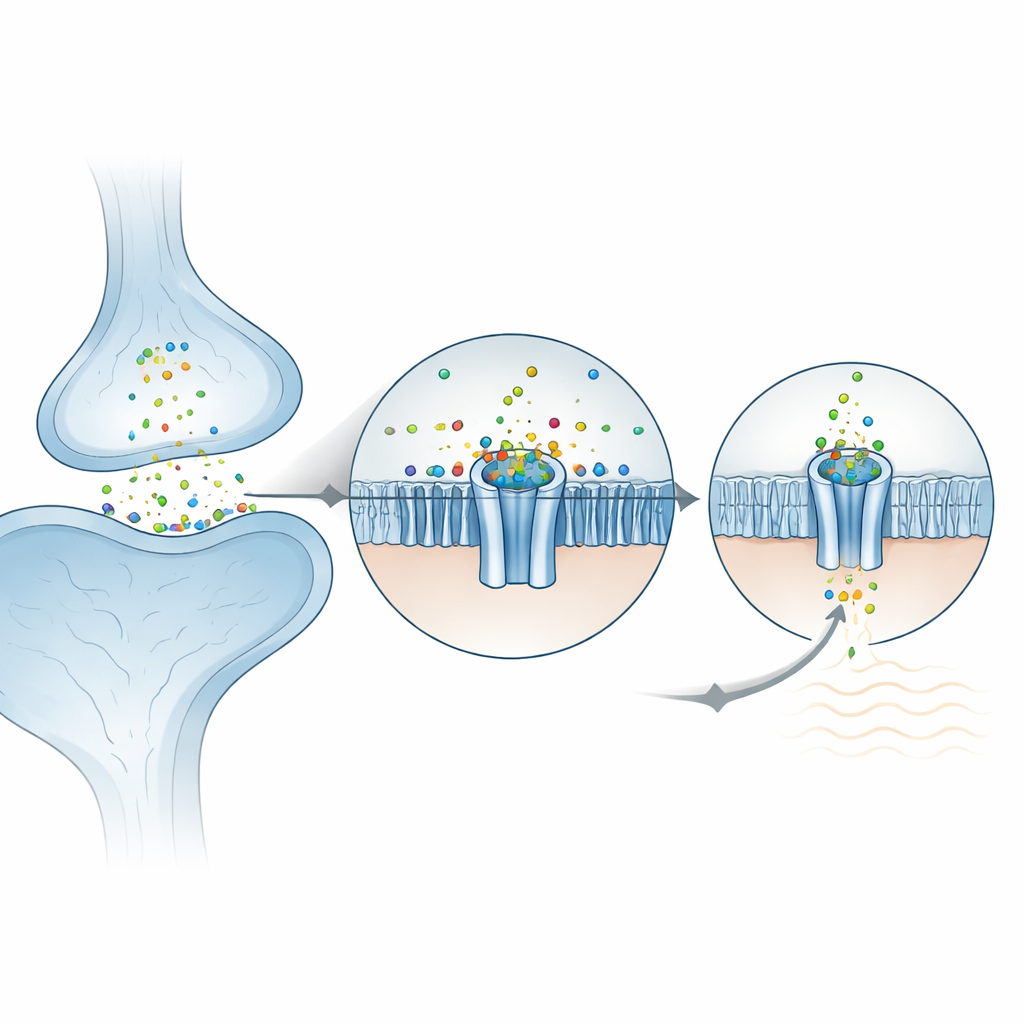
Как цинк фиксируется в канале
На наружной поверхности клетки ZAC состоит из пяти идентичных субъединиц, образующих розетку. Исследователи обнаружили, что ионы цинка располагаются в пяти эквивалентных карманах, каждый из которых находится между двумя соседними субъединицами во внешней доменной области. Удивительно, но цинк не удерживается обычными «захватчиками» — аминокислотами, которые часто связывают металлы (такими как гистидин или цистеин). Вместо этого он поддерживается главным образом двумя ароматическими боковыми цепями в форме кольца, которые стабилизируют положительный ион посредством так называемых катион–π взаимодействий. Когда эти ключевые остатки были мутированы в яйцах лягушки для электрических записей, канал перестал реагировать на цинк, что подтвердило их центральную роль. Окружающая среда уже предорганизована, что помогает объяснить заметную спонтанную активность ZAC даже без цинка: белок находится близко к стадию перехода между закрытым и открытым состоянием, и цинк лишь сдвигает баланс.
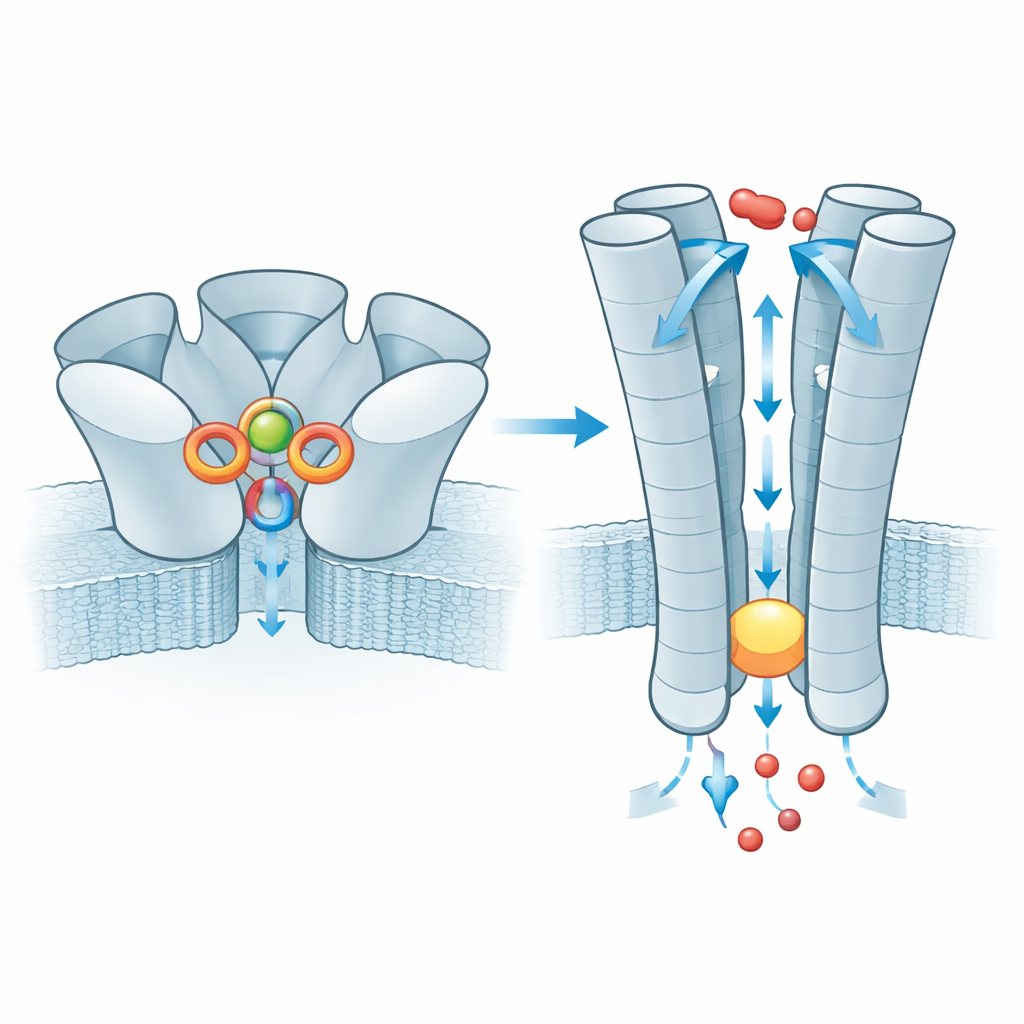
Путь для ионов и распространённый генетический вариант
После связывания цинка эффект передаётся вниз к части ZAC, пронизывающей мембрану, где пять внутренних спиралей формируют пору. В состоянии покоя эта трубка сужается у кольца лейциновых остатков, образуя гидрофобную пробку, блокирующую прохождение ионов. При связывании цинка пробка расширяется как раз настолько, чтобы пропускать мелкие положительные ионы, такие как натрий и калий, в то время как заряженная внутренняя поверхность поры помогает селектировать эти ионы. Команда также изучила очень распространённый вариант человека, в котором одна аминокислота (треонин) заменена на аланин в короткой петле над пробкой. Это небольшое изменение ослабляет сеть взаимодействий между соседними субъединицами, которые обычно передают сигнал о связывании цинка к затвору, и электрические измерения показывают, что каналы из этого варианта пропускают значительно меньшие токи. Следовательно, вариант действует как менее эффективный преобразователь сигнала, хотя его влияние на физиологию человека остаётся неизвестным.
Как два препарата заглушают канал
Помимо цинка, исследование также рассматривает, как два антагониста, TTFB и d‑тубокурарин (d‑TC), выключают ZAC. TTFB — специально созданная небольшая молекула, которая, как оказалось, встраивается глубоко в мембранную область, просачиваясь между двумя спиралями, формирующими пору, чуть выше затвора. Там она взаимодействует с плотным гидрофобным карманом и близлежащими полярными остатками, эффективно распоряжаясь спиралями так, что те не могут перейти в полностью открытое проводящее состояние. d‑TC, более старый препарат, когда‑то использовавшийся как миорелаксант, действует шире. Одна молекула d‑TC связывается в том же наружном кармане, который обычно занимает цинк, имитируя положительный заряд цинка, но блокируя его нормальное связывание. Вторая молекула d‑TC располагается в начале самой поры, физически закупоривая тоннель. Вместе эти связи запирают ZAC в десенситизированной, не проводящей конформации, в то время как форма белка остаётся относительно открытой.
Что означают эти результаты для цинка и здоровья
Эта структурная работа показывает в ясных молекулярных деталях, что ZAC является истинным сенсором цинка, используя необычную ароматическую «колыбель» для обнаружения металла в том же типе участка, где другие члены семейства связывают нейромедиаторы. Также определены конкретные сети взаимодействий, которые регулируют, насколько легко канал открывается и закрывается, и нанесены на карту два различных сайта связывания лекарств, которые либо клином прижимают затвор, либо заклинивают пору. Для неспециалистов ключевое послание таково: цинк — не просто статичный нутриент, а активный сигнальный агент, и ZAC — один из его специализированных приёмников. По мере того как учёные ищут роли ZAC в организме человека и при неврологических расстройствах, связанных с дисбалансом цинка, эти атомные чертежи дают дорожную карту для разработки более точных молекул, способных модулировать этот канал и, возможно, исправлять нарушенную цинковую сигнализацию.
Цитирование: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Ключевые слова: цинковая сигнализация, ионные каналы, управляемые лигандами, нейронаука, крио-ЭМ структура, модуляция канала