Clear Sky Science · ru
Пальмитоилирование ASCT2, регулируемое осью JNK1–ZDHHC14, организует метаболизм глутамина и прогрессирование НМРЛ
Подпитывая огонь рака легкого
Многие быстрорастущие раки легкого зависят от глутамина — распространённой аминокислоты, служащей ключевым топливом и строительным блоком. В этом исследовании показано, как опухолевые клетки тонко настраивают крупный «вентиль» для глутамина на своей поверхности и как нарушение этой системы управления может замедлить рост опухоли. Понимание этого скрытого регулятора поступления топлива помогает объяснить, почему некоторые опухоли трудно «голодить», и указывает на новые комбинации препаратов, которые могут более эффективно перекрывать их энергетический поток.
Клеточные ворота для глутамина
Глутамин поступает в клетки в основном через белковый транспортер ASCT2, расположенный в наружной мембране и переносящий глутамин внутрь. Немелкоклеточный рак легкого (НМРЛ), наиболее распространённая форма рака легкого, часто сильно зависит от глутамина для поддержания быстрого деления и выживания. Высокий уровень ASCT2 в опухолях связан с агрессивным течением болезни и худшим прогнозом для пациентов. Вместе с тем сам ASCT2 постоянно синтезируется, модифицируется и разрушается, что ставит вопрос: что определяет, сколько этого «привратника» остаётся на поверхности клетки в каждый конкретный момент?
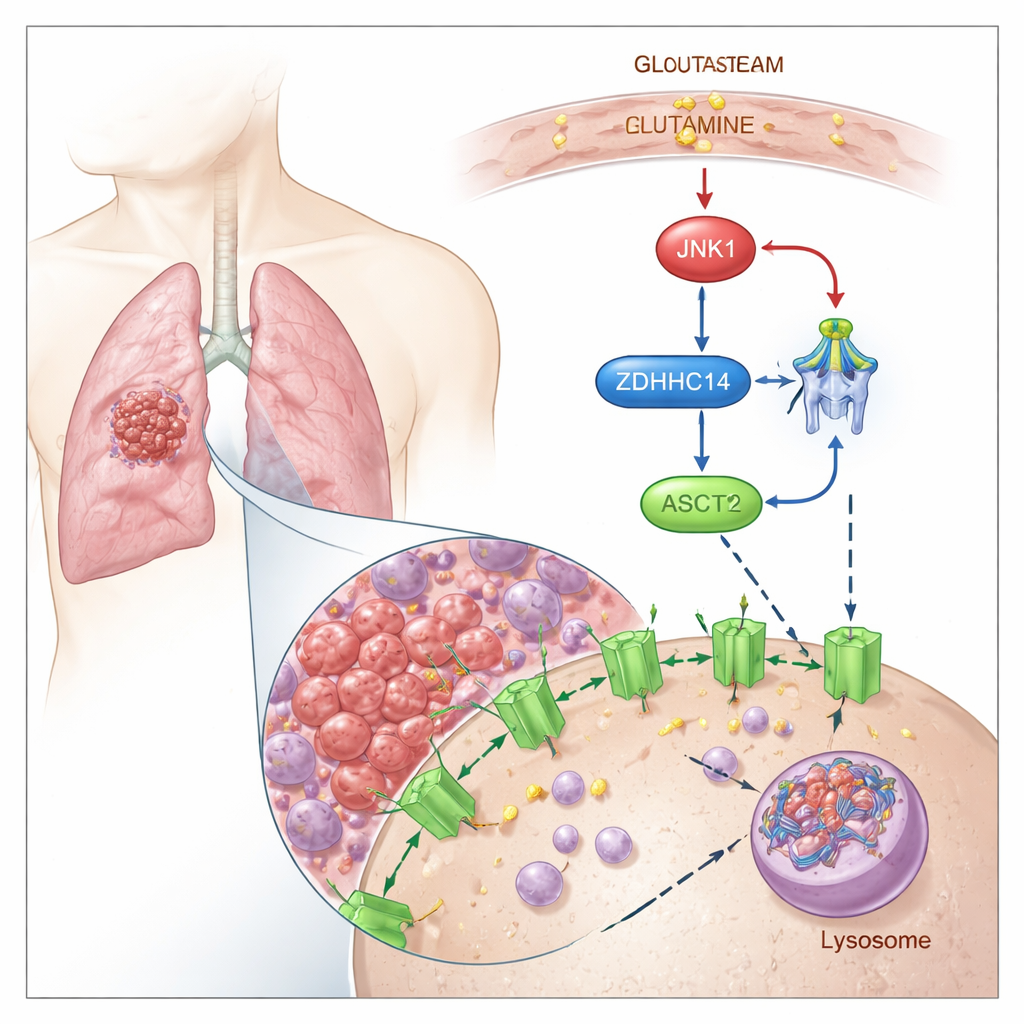
Метка ASCT2 для разрушения
Исследователи показали, что ASCT2 контролируется химической «меткой» — пальмитоилированием, при котором к определённым цистеиновым остаткам белка присоединяется жирная кислота. Они обнаружили, что фермент ZDHHC14 добавляет этот липидный ярлык к двум консервативным сайтам на ASCT2 (Cys39 и Cys48). После метки ASCT2 перенаправляется с клеточной поверхности в центры переработки — лизосомы, где он разрушается. Блокирование пальмитоилирования препятствует маркировке и деградации ASCT2, что приводит к повышению уровня белка ASCT2 и усилению поглощения глутамина без изменения активности гена.
Противоположный фермент, защищающий ворота
Противоположную функцию по отношению к ZDHHC14 выполняет другой фермент — ABHD17B, удаляющий жирный ярлык с ASCT2. При активности ABHD17B ASCT2 менее пальмитоилирован, более стабилен и с большей вероятностью возвращается на поверхность клетки, а не направляется в лизосому. Это постоянное назначение и снятие метки действует как тонко настроенный регулятор потока глутамина: ZDHHC14 направляет ASCT2 на разрушение, тогда как ABHD17B спасает его и поддерживает транспорт глутамина. В клетках рака легкого сдвиг баланса в сторону уменьшения пальмитоилирования увеличивает поглощение глутамина и способствует росту опухоли в культурах и у мышей.
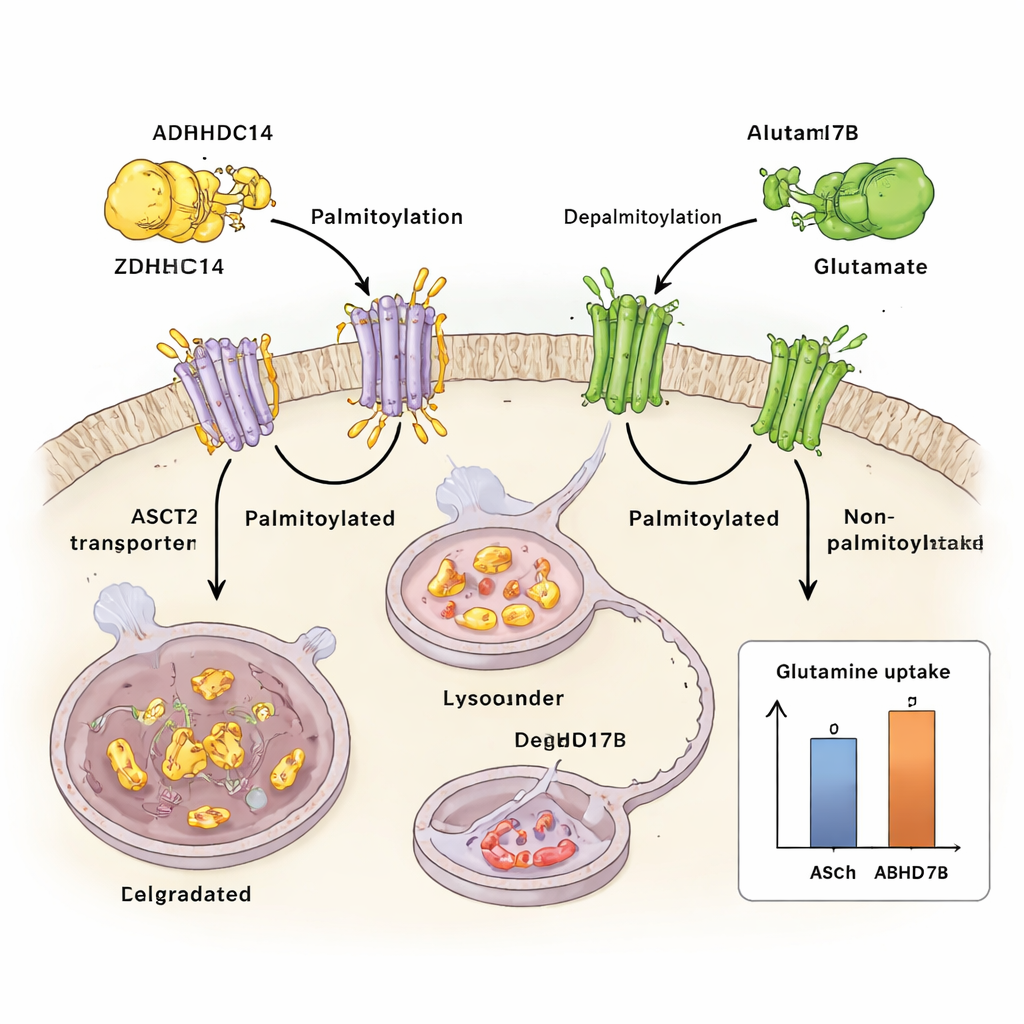
Как нутриентный стресс перенастраивает систему
Далее команда изучила, что происходит, когда опухолевые клетки испытывают недостаток глутамина. При дефиците глутамина включается чувствительный к стрессу сигнальный белок JNK1. JNK1 физически связывается с ZDHHC14 и фосфорилирует его в конкретном сайте (Thr440), помечая ZDHHC14 для собственной лизосомной деградации. По мере снижения уровня ZDHHC14 ASCT2 получает меньше пальмитоилирования, избегает разрушения и накапливается на поверхности клетки — как раз тогда, когда клетке важно максимально захватывать ограниченный глутамин. Мутация в этом одном сайте, чувствительном к JNK1, стабилизирует ZDHHC14, восстанавливает маркировку ASCT2 и уменьшает поглощение глутамина, подчёркивая, насколько плотно нутриентный стресс интегрирован в этот контур управления.
От механизма к терапии
Поскольку ASCT2 настолько важен для метаболизма опухолей, разрабатываются препараты, блокирующие его, например экспериментальное соединение V9302, как потенциал лечения рака. В этом исследовании показано, что сигнальная каскада JNK1 может противодействовать разрушению ASCT2, фактически защищая «ворота» глутамина. В клеточных и мышиных моделях НМРЛ комбинирование ингибитора JNK с V9302 сильнее снижало поглощение глутамина, рост опухолевых клеток и размер опухоли, чем любой из препаратов по отдельности. Образцы пациентов и общедоступные наборы данных дополнительно показывают, что низкий уровень ZDHHC14 и высокий уровень ASCT2 часто встречаются при НМРЛ и связаны с худшей выживаемостью, что указывает на то, что этот молекулярный профиль может помочь выявить пациентов, наиболее вероятно отзывчивых на таргетирование этого пути.
Что это значит для пациентов
Проще говоря, эта работа показывает, что некоторые раки легкого регулируют своё «любимое» топливо, настраивая молекулярный клапан на поверхности. Троица участников — JNK1, ZDHHC14 и ABHD17B — решает, будет ли транспортер ASCT2 отмечен для разрушения или оставлен открытым. Когда глутамина мало, система сдвигается в сторону сохранения ASCT2 и поддержания потока топлива, что помогает опухолям выживать в тяжёлых условиях. Совместное блокирование ASCT2 и защитного пути JNK позволило более эффективно «голодать» раковые клетки в лабораторных и животных моделях. Хотя необходимы дополнительные исследования, ось фосфорилирование–пальмитоилирование предлагает перспективный подход для терапий, направленных на перекрытие питательных жизнеобеспечений глутамина-зависимых опухолей легкого.
Цитирование: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Ключевые слова: метаболизм глутамина, немелкоклеточный рак легкого, транспортер ASCT2, пальмитоилирование белков, JNK-сигнализация