Clear Sky Science · ru
Молекулярные механизмы и возможные терапевтические последствия взаимосвязи между метилированием ДНК и перестройкой метаболизма при раке щитовидной железы
Почему это исследование важно за пределами лаборатории
Рак щитовидной железы — одно из наиболее быстро распространяющихся злокачественных заболеваний в мире. Хотя многие случаи поддаются лечению, самые агрессивные формы часто теряют чувствительность к радиоактивному йоду, основному виду терапии, оставляя пациентов с ограниченными вариантами лечения. В этом обзоре объясняется, как два невидимых внутри клетки фактора — химические метки на ДНК и изменения в том, как опухолевые клетки используют топливо — действуют совместно, стимулируя рост рака щитовидной железы и устойчивость к лечению. Понимание этого скрытого взаимодействия может открыть путь к более точным и стойким методам лечения.
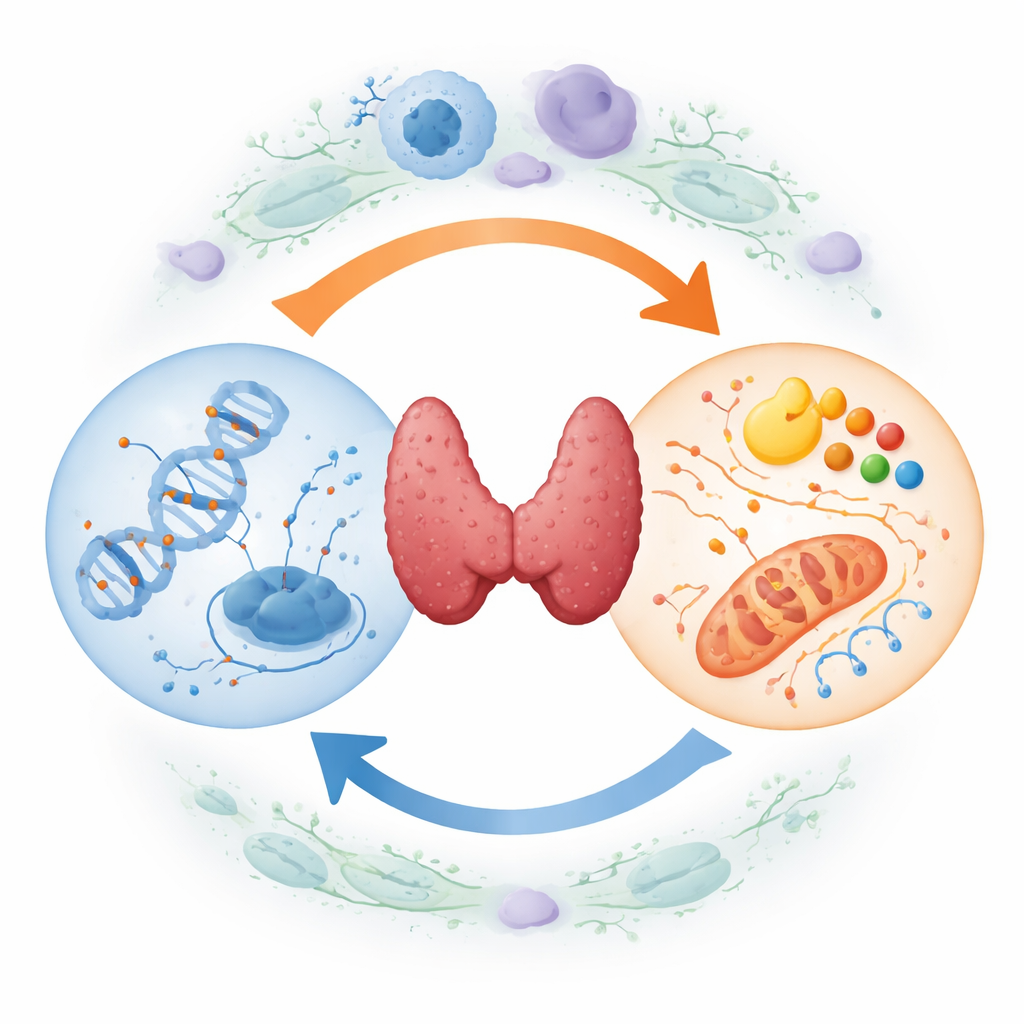
Как раковые клетки переписывают руководство по инструкции
Каждая клетка несёт одинаковую ДНК, но химические метки, называемые метильными группами, могут включать или выключать гены без изменения самого генетического кода. При раке щитовидной железы эта «верстка» ДНК сильно искажается. Большие участки генома теряют метки, что может дестабилизировать хромосомы, тогда как ключевые тормоза роста и гены, отвечающие за функцию щитовидной железы, становятся чрезмерно метилированными и выключаются. Сюда входят супрессоры опухолей и щитовидно-специфические гены, которые обычно помогают клеткам захватывать йод. В результате получается своего рода инструкция, в которой многие разделы безопасности закрыты, что способствует неконтролируемому росту и утрате нормальной идентичности щитовидной ткани.
Как раковые клетки перенастраивают свои топливные линии
Одновременно опухолевые клетки щитовидной железы перестраивают способы получения и использования энергии. Вместо того чтобы в основном эффективно сжигать топливо в митохондриях, они опираются на быстрый, но менее эффективный разбор сахаров, создающий кислые побочные продукты, которые помогают им уклоняться от иммунного надзора. Они также усиливают синтез и расщепление липидов, а аминокислоты, такие как серин и глутамин, перенаправляются на поддержку быстрого деления. Эти изменения не случайны: ими управляют сигнальные пути, запускающие рак, и они создают гибкую метаболическую сеть, позволяющую клеткам опухоли выживать при низком содержании кислорода, сопротивляться лекарствам и размножаться в новых местах.
Двусторонний обмен между метками ДНК и метаболизмом клетки
Ключевая идея статьи в том, что метилирование ДНК и использование топлива не существуют по отдельности — они образуют самоусиливающийся цикл. С одной стороны, изменённый метаболизм опухолевых клеток генерирует специфические малые молекулы, которые служат переключателями для ферментов, ставящих или снимающих метильные метки с ДНК. При изменении уровней этих молекул геном может сдвигаться к большей или меньшей метилированности в чувствительных участках. С другой стороны, метилирование ДНК может прямо подавлять или усиливать экспрессию генов, контролирующих утилизацию сахаров, обращение с жирами и транспорт аминокислот. Со временем этот двунаправленный трафик закрепляет состояние, благоприятное для рака, при котором аномальные метки ДНК и искажённый метаболизм постоянно усиливают друг друга.
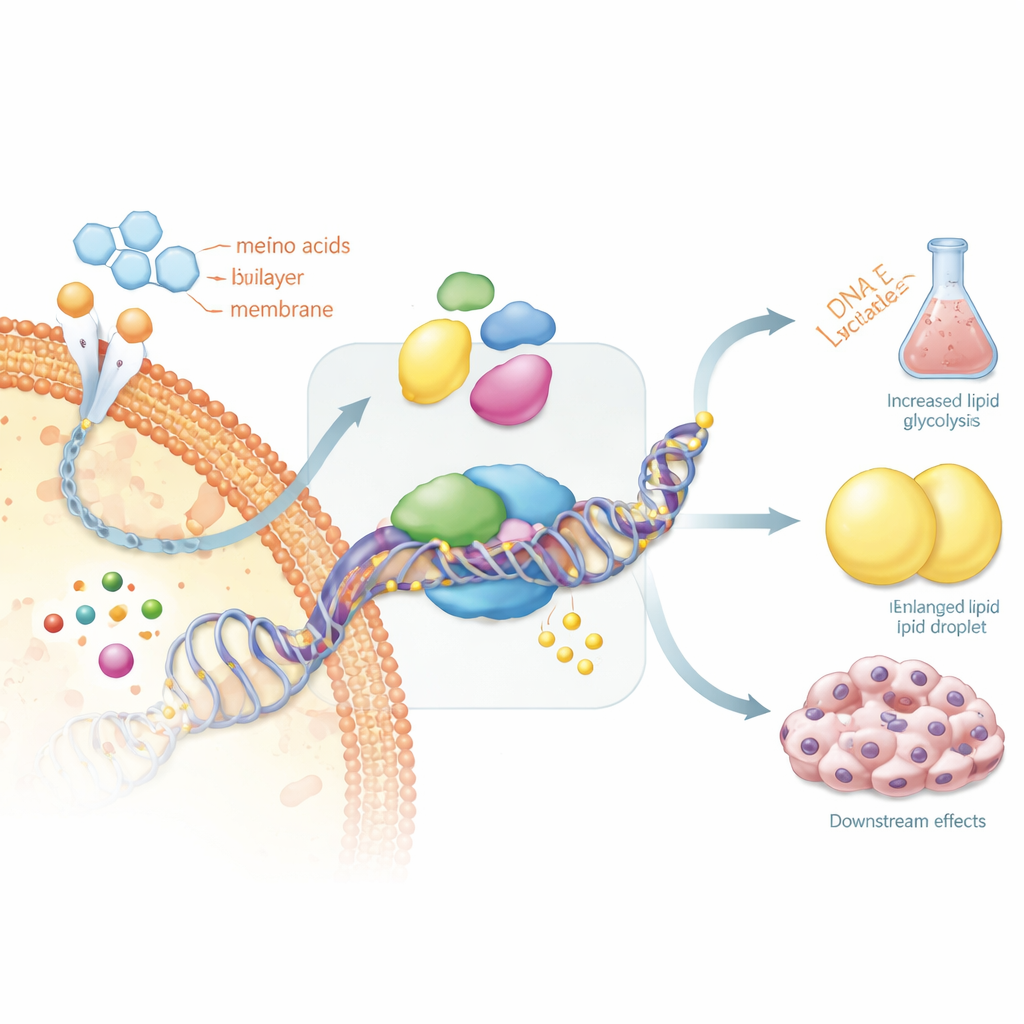
Почему некоторые раки щитовидной железы перестают захватывать йод
Этот петлевой механизм имеет очень практические последствия для пациентов. Терапия радиоактивным йодом эффективна только если опухолевые клетки сохраняют молекулярный аппарат для захвата йода. В обзоре подчёркивается, что ключевые щитовидные гены, отвечающие за это, включая рецептор тиреотропного гормона и натрий-йодный транспортер, часто выключаются из-за интенсивного метилирования их регуляторных областей. После этого клетки «забывают», что они — щитовидная ткань, и перестают поглощать йод, что делает стандартную терапию неэффективной. Авторы предлагают, что аккуратное обращение этих меток ДНК или блокирование метаболических путей, которые их поддерживают, может вновь пробудить захват йода и восстановить чувствительность к лечению.
Новые идеи лечения на основе интегрированного взгляда
Рассмотрение рака щитовидной железы как болезни оси «метилирование ДНК — метаболизм» ведёт к новым терапевтическим стратегиям. Вместо опоры на одиночные препараты авторы выступают за комбинационные подходы, которые одновременно атакуют несколько звеньев петли — эпигенетические препараты, ослабляющие вредные метки ДНК; метаболические препараты, перекрывающие ключевые каналы топлива; и сигнально-блокирующие агенты, приглушающие основные онкогенные пути. Добавление современных иммуннотерапий и передовых систем доставки лекарств, таких как «умные» наночастицы, может дополнительно смещать равновесие, перестраивая иммунную среду опухоли и уменьшая побочные эффекты. Ранние лабораторные и клинические данные указывают, что такие координированные атаки могут замедлить прогрессирование заболевания, восстановить захват радиоактивного йода у некоторых пациентов и отсрочить развитие резистентности.
Что это означает для будущего ухода
Для неспециалиста вывод таков: агрессивные формы рака щитовидной железы, вероятно, не вылечиваются одним «волшебным» средством, а требуют понимания и нарушения порочного круга между метками ДНК и метаболизмом клеток. Тщательно картируя эту ось и отслеживая соответствующие изменения в крови и образцах опухоли, врачи смогут в будущем подбирать пациентам индивидуальные комбинации эпигенетических, метаболических, таргетных и иммунотерапий. При успехе такой интегрированный подход может превратить сегодняшние наиболее упорные формы рака щитовидной железы в снова поддающиеся лечению состояния — и, возможно, помешать им стать столь агрессивными изначально.
Цитирование: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
Ключевые слова: рак щитовидной железы, метилирование ДНК, метаболизм рака, резистентность к радиоактивному йоду, таргетная терапия