Clear Sky Science · ru
Ингибирование HSP27 активирует взаимодействие XBP1s/CerS1, которое запускает DRP1‑опосредованную митофагию, тем самым защищая от гибели клеток и способствуя литическому циклу KSHV в клетках первичной эмптсионной лимфомы
Когда клеточный стресс становится двуострым мечом
Наши клетки выживают при повседневных повреждениях, включая аварийные программы, которые восстанавливают ущерб и поддерживают жизнеспособность. Однако клетки рака могут присвоить эти же программы, чтобы размножаться и скрывать внутри себя вирусы. В этой статье рассматривается, как блокирование одного белка, защищающего от стресса, в редкой лимфоме не только подтолкнуло опухолевые клетки к смерти, но и предоставило спрятанному в них вирусу окно для активации и размножения. Понимание этого хрупкого баланса может помочь в разработке терапий, убивающих рак и лишающих вирус возможности распространяться.
Скрытый вирус в агрессивной лимфоме
Первичная эмптсионная лимфома — это высокоагрессивный рак В‑клеток, разновидности лейкоцитов. У большинства таких опухолевых клеток присутствует дремлющий пассажир: вирус, связанный с саркомой Капоши (KSHV). В латентном состоянии вирус продуцирует лишь несколько белков и прячется в геноме хозяина. Определённые стрессы могут вывести его в активную, литическую фазу, когда он копирует себя и производит новые вирусные частицы, обычно убивая при этом клетку‑хозяина. Сами опухолевые клетки зависят от нескольких систем ответа на стресс, включая так называемые белки теплового шока и ответ на накопление неправильно свёрнутых белков, которые помогают справляться с дефектными белками, нарушенным липидным обменом и повреждениями митохондрий — энергообразующих органелл. 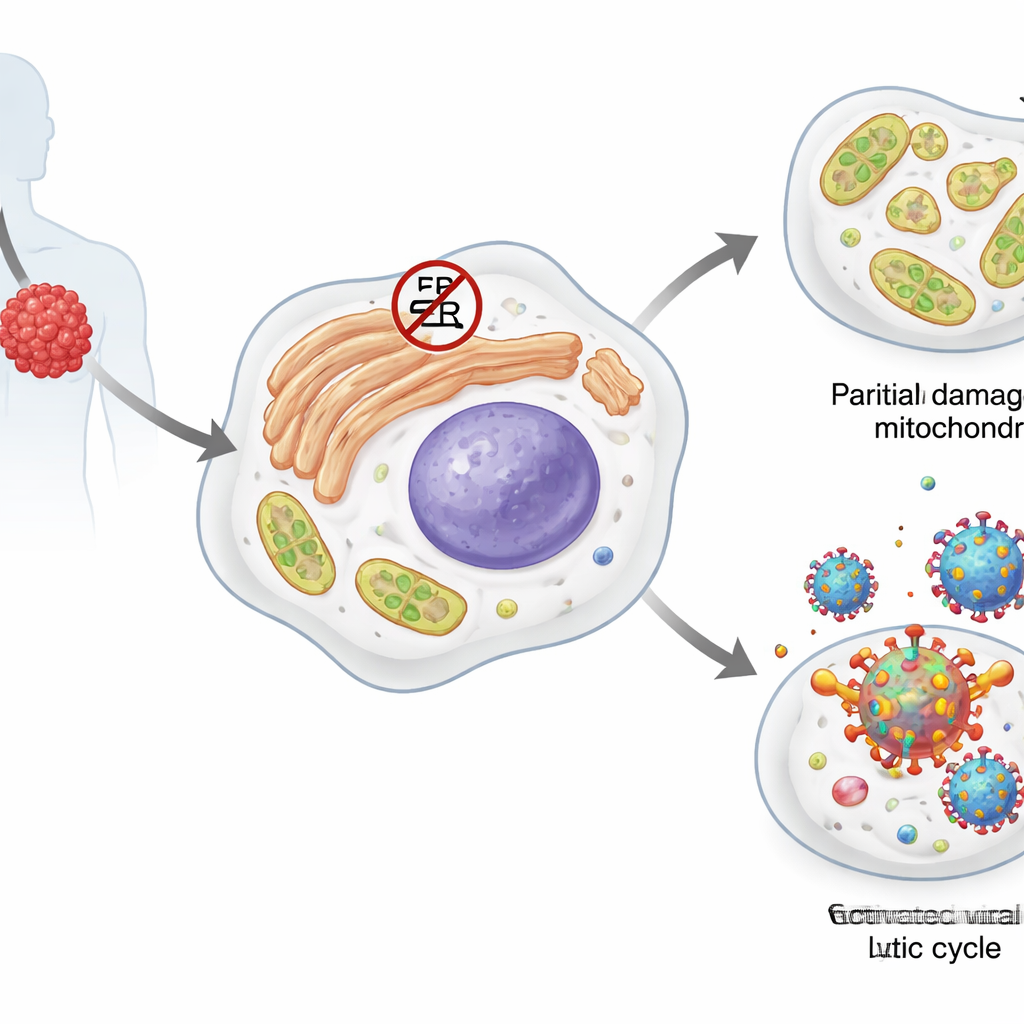
Блокирование клеточного телохранителя
Исследователи сосредоточились на HSP27, небольшом белке теплового шока, известном своей способностью защищать клетки от стресса. С помощью химического ингибитора J2 или с помощью заглушения гена малыми РНК они снизили активность HSP27 в лимфомных клетках, выращиваемых в культуре. Это уменьшило выживаемость клеток и вызвало интенсивный стрессовый сигнал в внутренней мембранной сети — эндоплазматическом ретикулуме. Маркеры этого ответа, включая факторы, защищающие и способствующие смерти, повысились, и был активирован ключевой переключатель XBP1s. Одновременно в клетках усилились признаки программируемой смерти, что подтверждает: лишение HSP27 подталкивает их к критической грани между выживанием и гибелью.
Петля стресса, которая взаимодействует с липидами клетки
Стресс в эндоплазматическом ретикулуме тесно переплетён с тем, как клетки управляют липидами. Команда обнаружила, что блокирование HSP27 повышает уровни CerS1 — фермента, синтезирующего определённый липид C18‑церамид. Когда они химически блокировали XBP1s, рост CerS1 исчезал, что показывает: XBP1s способствует включению гена CerS1 при этих условиях. Поразительно, что ингибирование CerS1 в свою очередь снижало XBP1s, выявляя положительную обратную связь: каждый фактор поддерживает другой. Это молекулярное «пожатие рук» не только перестраивает липидный метаболизм, но и усиливает способность клетки адаптироваться к стрессу эндоплазматического ретикулума, даже когда сигналы смерти накапливаются.
Митохондрии перерабатываются вместо того, чтобы быть уничтоженными
Стресс в одной части клетки часто переходит на митохондрии — крошечные энергетические станции. После блокирования HSP27 лимфомные клетки вырабатывали больше активных форм кислорода, что указывает на митохондриальные нарушения, и повышали уровни DRP1 — белка, который рассекает митохондрии на более мелкие фрагменты. Авторы показали, что петля XBP1s–CerS1 отвечала за повышение DRP1. Это, в свою очередь, запускало митофагию — процесс контроля качества, при котором повреждённые митохондрии оборачиваются мембранами и направляются в «центры утилизации» клетки, лизосомы. С помощью флуоресцентных красителей и белковых маркеров они подтвердили селективное удаление митохондрий. При химическом или генетическом блокировании DRP1 митофагия уменьшалась, и клетки погибали легче, что означает: переработка митохондрий на самом деле помогала стрессующимся опухолевым клеткам выживать.
Предоставляя вирусу время для побега
Та же митофагия, которая защищала опухолевые клетки, также приносила пользу KSHV. Активация XBP1s, накопление C18‑церамида и усиление митохондриального дробления ранее связывали с пробуждением этого вируса. Здесь, при ингибировании HSP27, больше клеток экспрессировали ранние и поздние вирусные белки — явные признаки литической репликации. Блокирование DRP1 и, следовательно, митофагии, снижало эту вирусную реактивацию. Авторы предполагают, что слегка продлевая выживание клеток под стрессом, митофагия даёт KSHV время завершить цикл репликации и покинуть умирающую клетку, потенциально инфицируя новые мишени и способствуя прогрессии рака.
Что это значит для будущих лечений
Для неспециалиста ключевое послание таково: HSP27 выступает центральным регулятором того, как лимфомные клетки справляются со стрессом, как они утилизируют повреждённые митохондрии и когда связанный с раком вирус решает проснуться. Выключение HSP27 запускает цепочку событий, которая одновременно подтачивает выживание клетки и, парадоксально, временно защищает её через митофагию, позволяя KSHV реплицироваться. С терапевтической точки зрения сочетание ингибирования HSP27 с препаратами, блокирующими DRP1‑опосредованную митофагию, могло бы ускорить гибель опухолевых клеток и ограничить шансы вируса на распространение, предложив двунаправленную стратегию против этой смертоносной лимфомы.
Цитирование: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Ключевые слова: первичная эмптсионная лимфома, вирус саркомы Капоши, ответ на клеточный стресс, митофагия, тепловой шоковый белок HSP27