Clear Sky Science · ru
Ось AdipoR1–AMPK подавляет рак молочной железы во многих молекулярных подтипах посредством мультимодальных путей гибели клеток, включая ферроптоз и апоптоз
Почему жировые клетки важны для рака молочной железы
Большинство из нас считает жировую ткань пассивным хранилищем энергии, но жировые клетки — активные «фабрики», которые выпускают гормоны и сигнальные молекулы в кровоток. В этом исследовании изучается, как один из таких жировых сигналов, действующий через молекулу AdipoR1 на клетках рака молочной железы, может замедлять рост опухоли. Работа важна тем, что указывает на новый способ лечения многих форм рака молочной железы, опирающийся на коммуникацию между жировой тканью и опухолями и потенциально усиливающий эффект существующих препаратов.
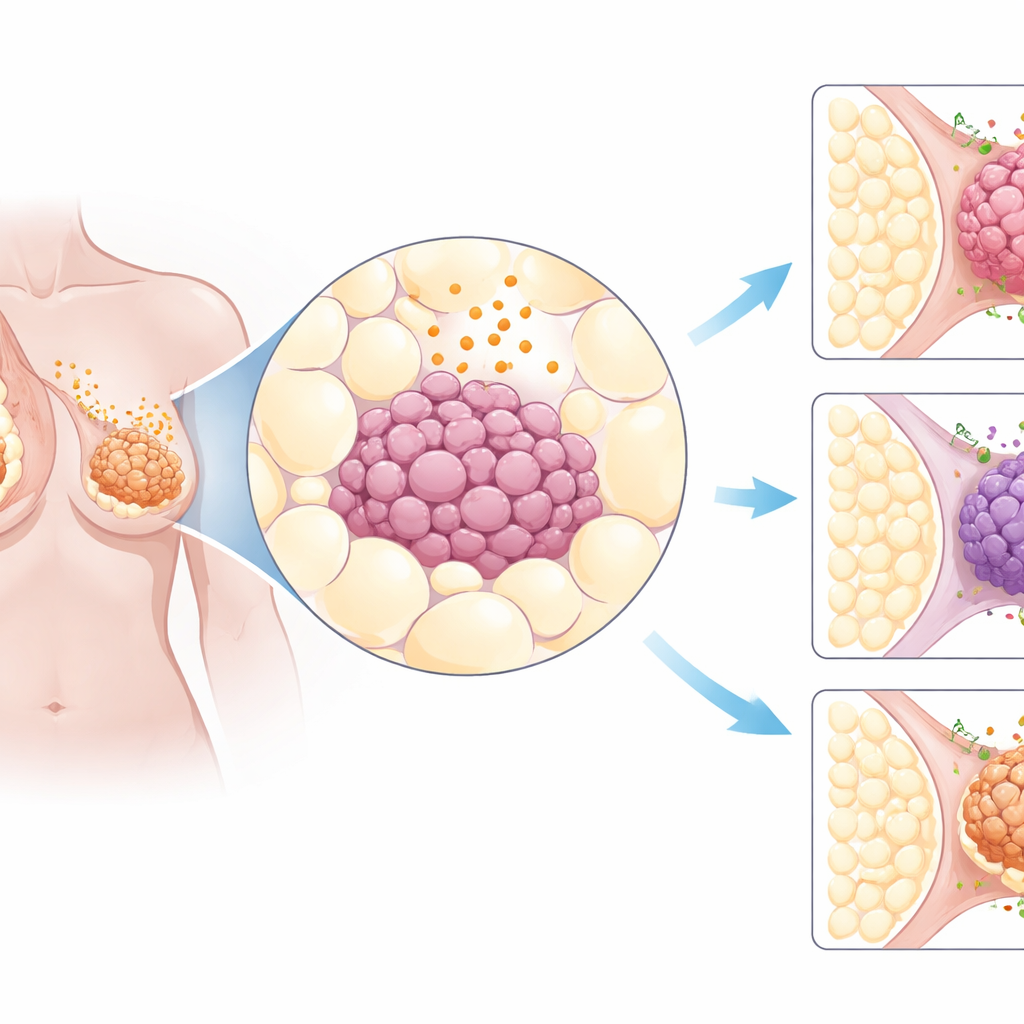
Исследование множества видов рака
Исследователи начали с анализа крупных публичных онкологических баз данных, содержащих генетическую информацию из тысяч опухолей пациентов. Они сосредоточились примерно на тридцати нескольких генах, вовлечённых в сигналы, исходящие из жировой ткани, и на структурах клетки, принимающих эти сигналы. Сравнивая опухоли из 31 органа со здоровой тканью, они обнаружили одну заметную закономерность: изменения, связанные с жировыми сигналами, были особенно сильны в раке молочной железы. В частности, рецептор AdipoR1 часто обнаруживался в повышенных уровнях в опухолях молочной железы, независимо от того, гормонозависимые они, HER2‑положительные или более агрессивного тройного‑негативного типа. Образцы тканей более чем из 600 опухолей молочной железы подтвердили широкое присутствие белка AdipoR1 в раковых клетках.
Тестирование препарата, имитирующего жировой сигнал, на раковых клетках
Чтобы понять, что делает AdipoR1 внутри опухолей, команда обратилась к линиям клеток рака молочной железы, выращенным в лаборатории и представляющим несколько распространённых подтипов. Они лечили эти клетки AdipoRon — небольшой молекулой, активирующей AdipoR1. AdipoRon быстро включал известный клеточный датчик энергии AMPK, что доказывало прохождение сигнала. С увеличением дозы AdipoRon клетки делились медленнее, перемещались меньше в тестах на «заживление» ран, и многие проходили программируемую самоуничтожение. Когда исследователи целенаправленно снижали уровни AdipoR1 в клетках, эффект AdipoRon значительно ослабевал, тогда как повышение уровня рецептора делало препарат более эффективным — что связывает наблюдаемый эффект напрямую с этим рецептором.
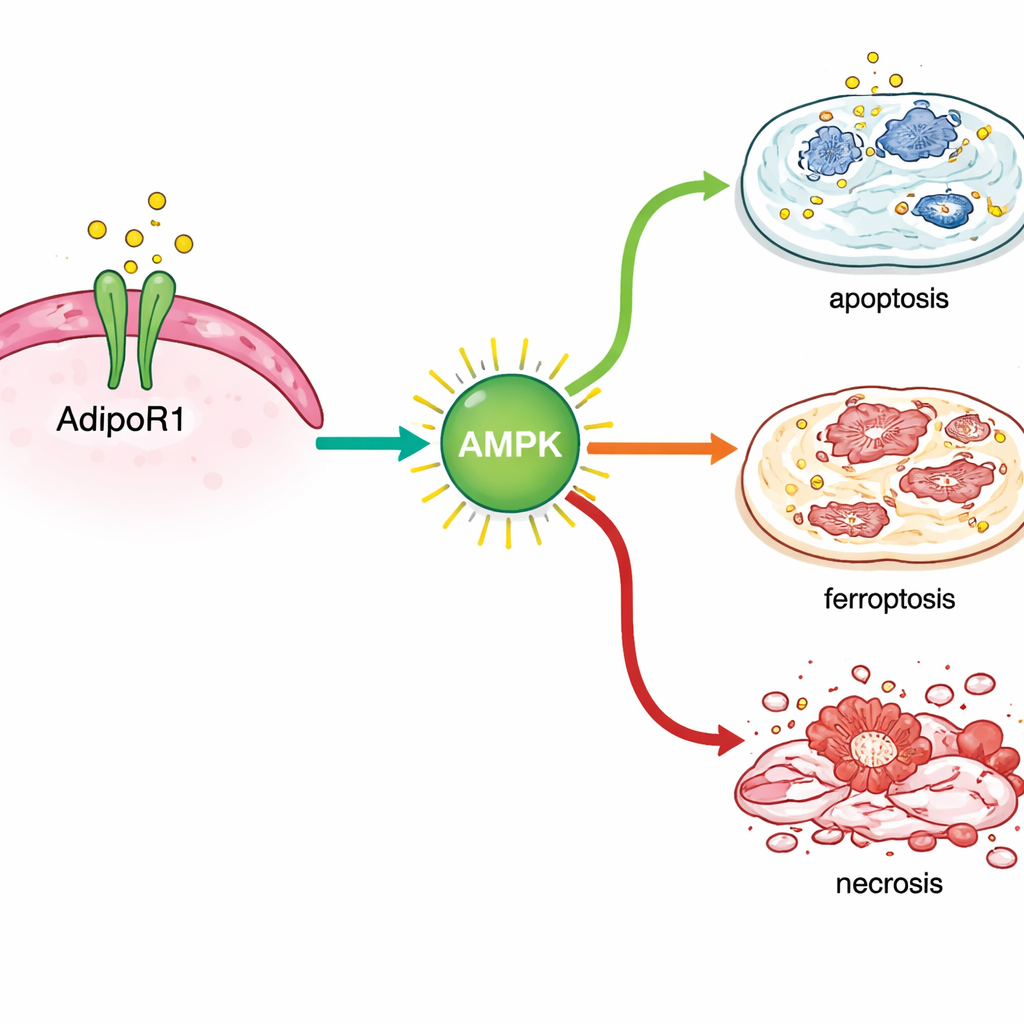
Несколько путей ведут клетки к гибели
Анализ активности генов после лечения показал, что AdipoRon включал стресс‑реакции внутри клеток рака молочной железы. Он активировал гены, связанные со стандартными программируемыми путями гибели клеток, а также те, что участвуют в недавно признанной форме железозависимой гибели — ферроптозе. Ключевые маркеры этого процесса возросли как на уровне РНК, так и на уровне белка, особенно в гормон‑чувствительных клетках молочной железы, а химические измерения повреждённой липидной составляющей клеток подтверждали это наблюдение. Одновременно AdipoRon снижал уровни белков, которые обычно помогают клеткам выживать, включая участники репарации ДНК (BRCA1 и BRCA2), эстрогеновый рецептор, стимулирующий рост во многих опухолях, и TROP2 — поверхностный молекулярный маркер, связанный с агрессивным поведением.
Взаимодействие с текущими методами лечения
Команда затем проверила, может ли активация AdipoR1 дополнять стандартные препараты. В гормон‑чувствительных клетках молочной железы сочетание AdipoRon с тамоксifenом вызвало более сильное подавление роста, чем любой из препаратов по‑отдельности. В тройно‑негативных линиях AdipoRon усиливал эффект общих химиопрепаратов, таких как паклитаксел и доxorубицин. При переходе к исследованиям на мышах с гормон‑чувствительными опухолями молочной железы препарат давали перорально. У животных из группы лечения опухоли росли медленнее и содержали большие зоны мёртвых клеток при гистологическом обследовании. Важно, что в ходе лечения у мышей не наблюдалось явных побочных эффектов в поведении, весе или состоянии печени.
Что это может значить для пациентов
В совокупности результаты указывают, что включение AdipoR1 в клетках рака молочной железы задействует несколько перекрывающихся путей гибели клеток и ослабляет ключевые системы выживания, и что этот подход действует в разных генетических вариантах болезни. Вместо того чтобы заменять существующие терапии, препараты, нацеленные на AdipoR1, такие как AdipoRon, могли бы служить дополнением, делающим опухоли более уязвимыми к гормональной терапии, химиотерапии или будущим таргетным агентам. Прежде чем этот подход попадёт в клинику, потребуется разработать более мощные и селективные активаторы AdipoR1, выяснить, у каких пациентов опухоли сильнее экспрессируют этот рецептор, и тщательно оценить безопасность. Тем не менее работа подаёт интересную идею: сигналы нашей собственной жировой ткани могут быть перенаправлены, чтобы помогать в борьбе с раком молочной железы, а не подпитывать его.
Цитирование: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Ключевые слова: рак молочной железы, адипокины, AdipoR1, пути гибели клеток, метаболизм рака