Clear Sky Science · ru
Роль липидных рафтов в опосредованной FGFR2c онкогенной сигнализации с участием канала TRPA1 в клетках аденокарциномы панкреатического протока
Почему маленькие островки в мембранах клеток имеют значение
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что его клетки особенно склонны отсоединяться от первичной опухоли и вторгаться в окружающие ткани. В этом исследовании рассматриваются крошечные «островки» на внешней оболочке раковых клеток, состоящие из холестерина и липидов, и ставится простой, но важный вопрос: помогают ли эти островки включать сигналы роста, которые делают рак поджелудочной более агрессивным, и можно ли замедлить процесс, нарушив их целостность?
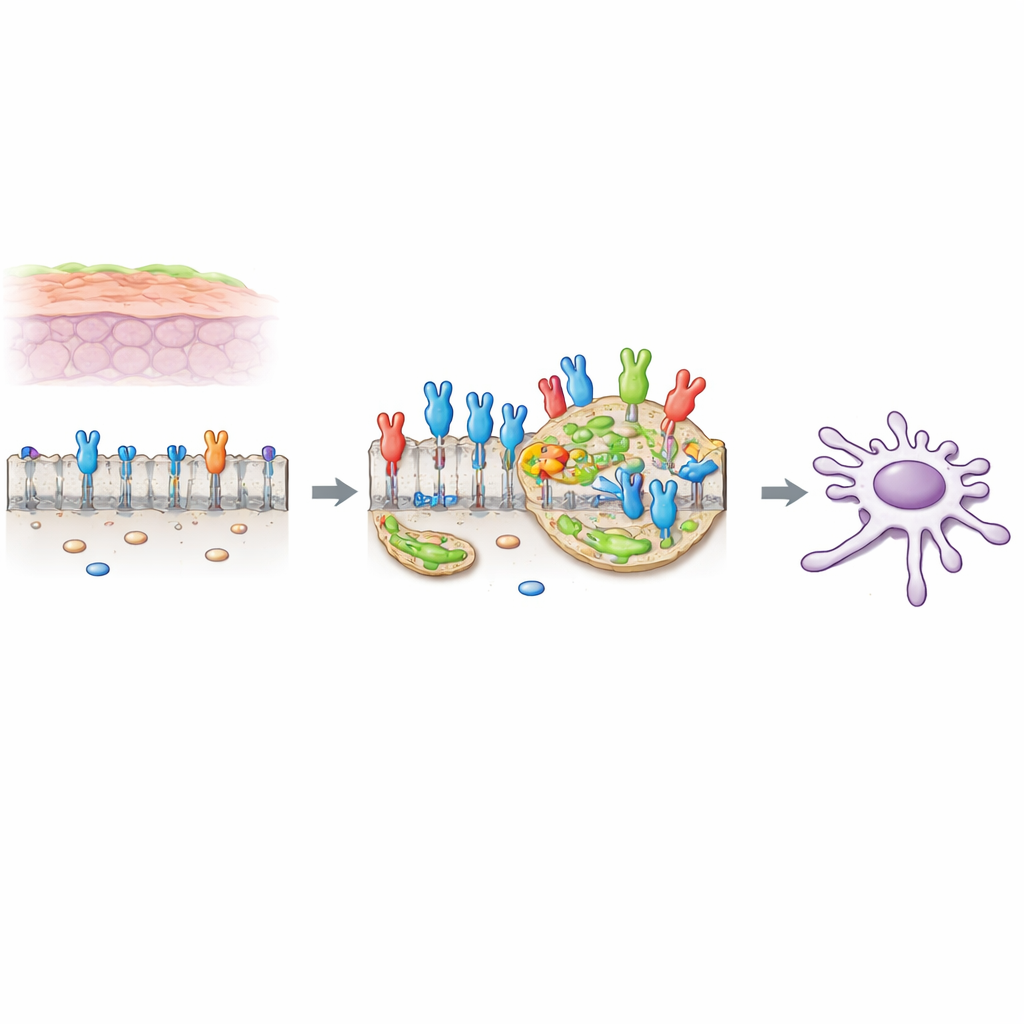
Ракопродвигающий переключатель на поверхности клетки
Многие клетки несут на своей поверхности «выключатели», которые реагируют на сигналы роста. Один из таких переключателей, называемый FGFR2c, — вариант рецептора, обычно встречающийся в более подвижных клетках, — оказывается аномально обильным в клетках аденокарциномы панкреатического протока (PDAC). Когда этот рецептор активируется своим внеклеточным лигандом, он запускает изменения, известные как эпителиально-мезенхимальный переход (EMT), которые делают клетки менее прикрепленными и более подвижными и инвазивными. Ранее авторы показали, что в клетках PDAC FGFR2c активирует каскад внутриклеточных посредников с участием белка PKCε и нескольких классических путей роста, усиливая выживание клеток, их подвижность и инвазию.
Холестериновые островки как усилители сигналов
Внешняя мембрана клетки не однородна. В ней есть небольшие холестерин-содержащие участки, называемые липидными рафтами, которые служат миниатюрными платформами, где сигнальные молекулы могут собираться и взаимодействовать эффективнее. Исследователи обнаружили, что при активации FGFR2c большее количество рецептора перемещается в эти липидные рафты. С помощью флуоресцентных маркеров и биохимической фракционизации они показали, что активированный FGFR2c концентрируется в этих участках, тогда как его распределение вне рафтов изменяется от равномерного до пятнистого, что соответствует кластеризации рецепторов на этих «островках».
Разрушение островков ослабляет раковые свойства
Чтобы проверить, являются ли эти липидные островки необходимыми для ракообразующих эффектов FGFR2c, команда использовала соединение (метил-β-циклодекстрин), которое избирательно удаляет холестерин из мембраны и дестабилизирует липидные рафты без гибели клеток. В клетках PDAC с высоким уровнем FGFR2c нарушение рафтов сильно снижало активацию ключевых сигнальных молекул ниже рецептора и подавляло программу EMT: уровень генов и белков, связанных с подвижным и инвазивным фенотипом, уменьшался, а эпителиальные черты частично восстанавливались. То же лечение снижало уровни белков, связанных с инвазией, таких как MCL-1, SRC и матрично-разрушающие ферменты, и уменьшало способность раковых клеток перемещаться и проникать в гель, имитирующий окружающую ткань. Клетки с очень низким уровнем FGFR2c почти не реагировали, что подчеркивает центральную роль взаимодействия рецептора и рафтов в этих опухолях.
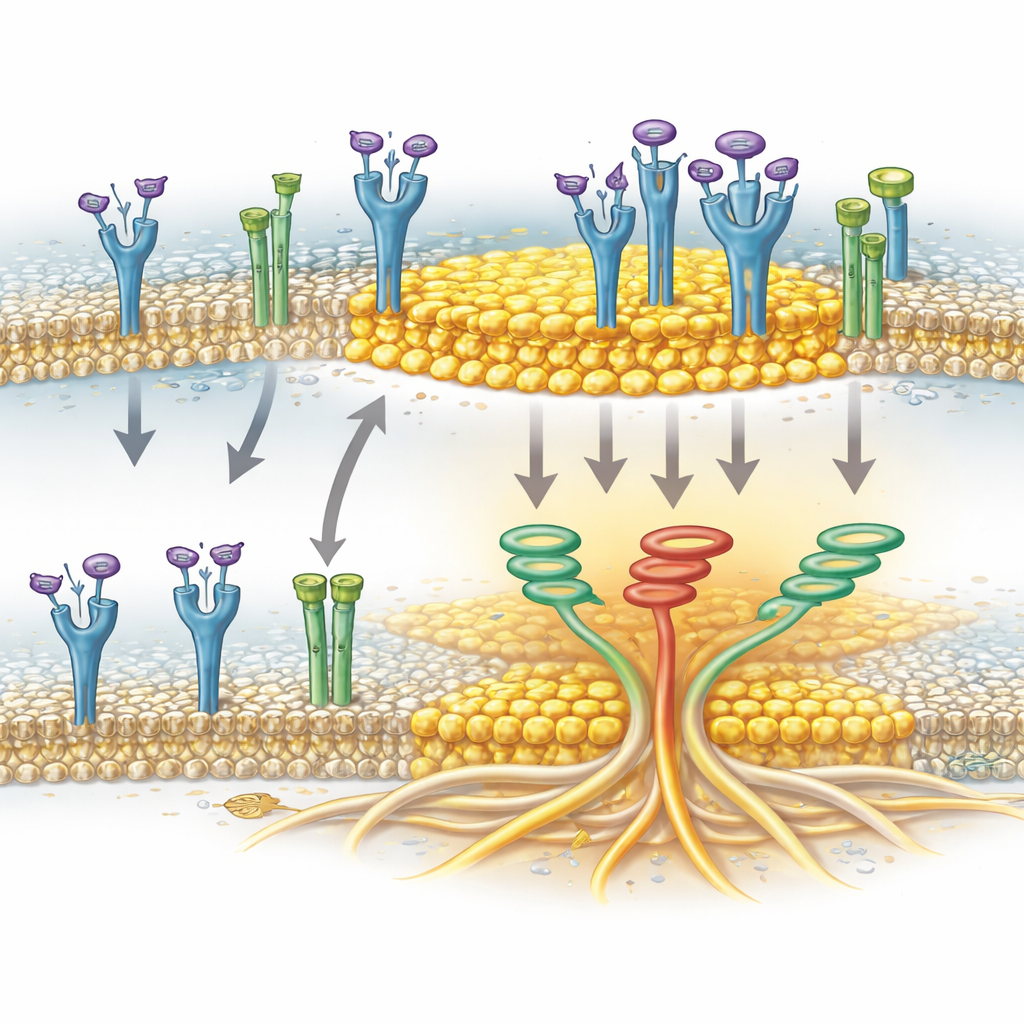
Ионный канал как помощник кластеризации
Исследование также выявляет неожиданный вспомогательный компонент: TRPA1, каналовый белок, известный в основном по роли в ощущении раздражителей и окислительного стресса в нервной системе. В клетках рака поджелудочной TRPA1 присутствует на мембране и может локализоваться в липидных рафтах. Авторы показали, что TRPA1 физически ассоциирует с FGFR2c при активации рецептора и что эта ассоциация совпадает с обогащением FGFR2c в рафтовых фракциях. При снижении уровня TRPA1 активированный FGFR2c переставал эффективно накапливаться в областях рафтов, хотя сами рафты оставались целыми. Это указывает на то, что TRPA1 не просто пассивный пассажир, а активно помогает «сопровождать» или стабилизировать FGFR2c в этих холестерин-насыщенных платформах, где рецептор эффективнее запускает инвазивную сигнальную сеть.
Что это значит для будущих терапий
В совокупности работа создает картину, в которой FGFR2c, TRPA1 и липидные рафты образуют кооперативный комплекс, усиливающий инвазивные свойства клеток рака поджелудочной железы. FGFR2c обеспечивает ростовой сигнал, липидные рафты дают физическую сцену для сборки сигнальных комплексов, а TRPA1 помогает вывести рецептор на эту сцену. Для неспециалиста ключевая мысль заключается в том, что опасность опухоли определяется не только самими онкогенными молекулами, но и крошечными мембранными ландшафтами, которые они занимают. Нацеливание на FGFR2c, TRPA1 или на стабильность этих холестериновых «островков» — по отдельности или в комбинации — в будущем может позволить точнее ослаблять инвазивный механизм клеток рака поджелудочной железы, действуя более выборочно в отношении опухоли.
Цитирование: Mancini, V., Manganelli, V., Garofalo, T. et al. Role of lipid rafts in the FGFR2c-mediated oncogenic signaling by involvement of TRPA1 channel in pancreatic ductal adenocarcinoma cells. Cell Death Dis 17, 259 (2026). https://doi.org/10.1038/s41419-026-08513-7
Ключевые слова: рак поджелудочной железы, липидные рафты, FGFR2c, канал TRPA1, инвазия клеток