Clear Sky Science · ru
Нацеливание на мутанты p53 в позиции Y220C, Y220N и Y220S с помощью низкомолекулярного стабилизатора резатапопт
Почему это важно для будущих методов лечения рака
Рак часто нейтрализует p53, белок, который иногда называют «стражем» клетки, посредством мутаций, из‑за которых он уже не может контролировать опасные клетки. Одна из таких изменений, известная как Y220C, часто встречается в солидных опухолях и стала объектом испытаний для лекарств, стремящихся восстановить нарушенную функцию p53, а не просто уничтожать клетки. В этом исследовании поставлен практический, ориентированный на пациентов вопрос: может ли многообещающее экспериментальное вещество резатапопт, уже проходящее клинические испытания для Y220C, также помогать людям с близкими, но более редкими вариантами мутаций в той же позиции p53?
Препарат, разработанный как «заплатка» для трещины в p53
Многие мутации p53 приводят к тому, что белок «раскрывается» и теряет точную форму. При мутации Y220C замена аминокислоты образует небольшую полость на поверхности белка — дефект, который химики поняли как пригодный для «заплатки» с помощью подобранных низкомолекулярных соединений для стабилизации p53. Резатапопт — одно из таких соединений, созданное на базе более ранних серий молекул, которые встраиваются в эту полость и действуют как молекулярный подпор. Авторы сосредоточили внимание на двух других мутациях в той же аминокислотной позиции, Y220S и Y220N, которые также образуют похожий карман, но еще сильнее дестабилизируют p53, чем Y220C. Если резатапопт сможет «заплатать» и эти варианты, это потенциально расширит подход прецизионной медицины для тысяч дополнительных пациентов ежегодно. 
Измерение того, насколько надежно резатапопт захватывает и укрепляет мутантный p53
Чтобы проверить это, команда очистила ДНК-связывающий центр p53 с заменой Y220C, Y220S или Y220N и подвергла каждый вариант действию резатапопта (и близких по строению аналогов). С помощью тепловых тестов они показали, что все три мутантных белка становятся более стабильными при связывании с препаратом: Y220C и Y220S фактически возвращают устойчивость, сравнимую с дикой формой, тогда как Y220N восстановилась лишь частично. Вторая методика, измеряющая тепло, выделяющееся при связывании, объяснила причину: резатапопт сильно сцепляется с Y220C (порядка нескольких десятков наномоляр), несколько слабее — с Y220S и еще слабее — с Y220N, хотя все значения попадают в диапазоны, которые считаются перспективными для медицинской химии.
Наблюдение молекулярной «заплатки» на атомном уровне
Структуры высокой разрешающей способности, полученные методом рентгеновской кристаллографии, дали визуальное объяснение. Во всех трех мутантах резатапопт располагается в образованном мутацией углублении в сохраненной ориентации: его центральный каркас заполняет полость, один конец проникает глубоко в карман с кластером атомов фтора, а другой контактирует с рядом расположенной петлей белка. Препарат образует сеть контактов, включая стратегически расположенный атом фтора, взаимодействующий с каркасом белка. В случае Y220S эти взаимодействия сохраняются с лишь незначительными смещениями, что позволяет добиться сильной стабилизации. Для Y220N же связывание заставляет боковую цепь аспарагина размещаться в более гидрофобном ядре белка в энергетически неблагоприятной конформации, и некоторые контакты с фторированным «якорем» препарата теряются. Такая напряженная посадка объясняет и более слабое связывание, и неполное восстановление устойчивости. 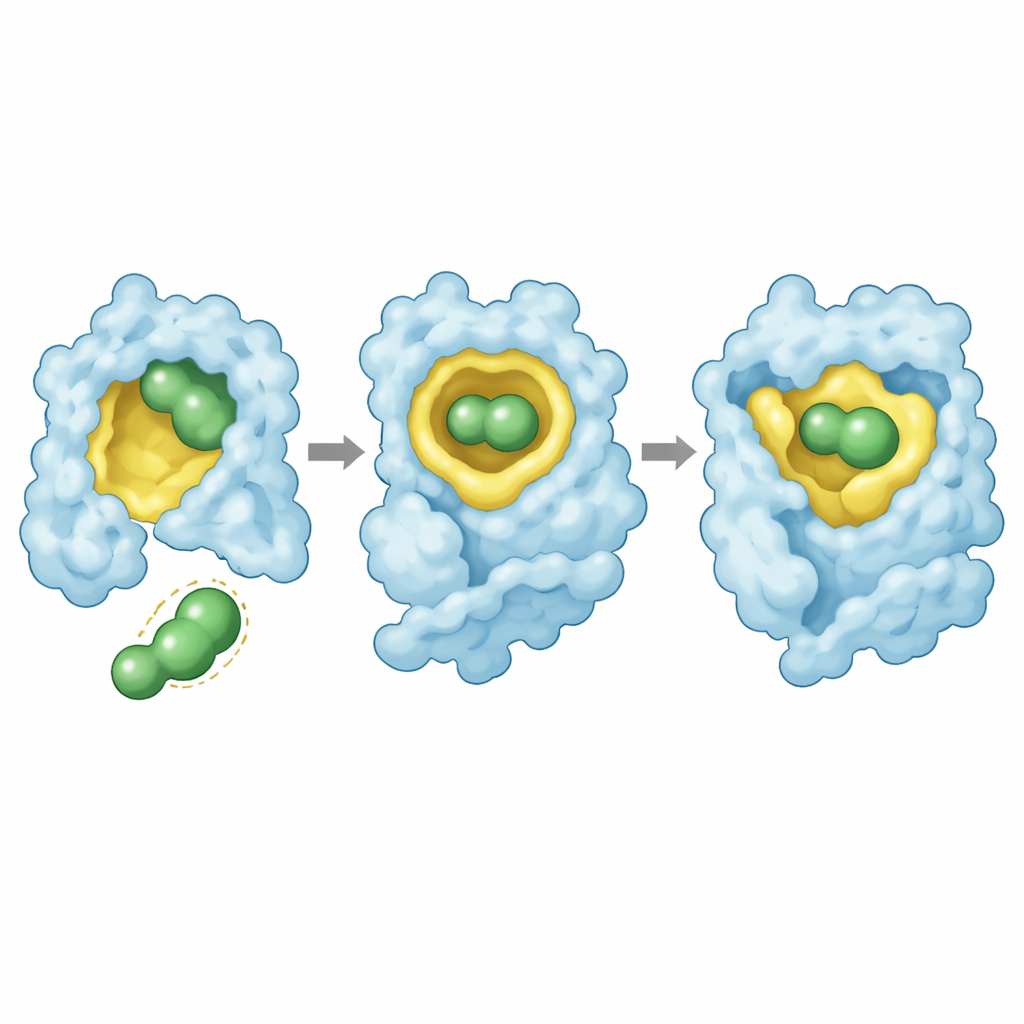
От починки белка до поведения клетки
Ключевой тест — восстановит ли такая стабилизация защитную роль p53 в живых клетках. Исследователи генетически модифицировали клетки рака легкого, лишенные естественного p53, чтобы они экспрессировали варианты Y220C, Y220S, Y220N или Y220H. При обработке резатапоптом клетки с Y220C демонстрировали мощную активацию классических целевых генов p53, отвечающих за остановку клеточного цикла и запуск программ гибели клетки. Клетки с Y220S показали очень схожую картину — восстановление свернутой активной формы p53, сильную активацию генов, замедление пролиферации и усиление гибели клеток — но лишь при концентрациях препарата более чем в десять раз выше, чем для Y220C. Клетки с Y220N, напротив, при переносимых дозах не продемонстрировали явной активации целевых генов и в основном оставались в неправильно свернутом состоянии, хотя незначительные поздние эффекты на рост намекают на лишь частичное функциональное восстановление.
Что это значит для пациентов и дальнейшей разработки препаратов
Для людей с опухолями, несущими мутацию Y220S, эти результаты осторожно обнадеживают: в принципе резатапопт может восстановить защитные функции p53, но для этого требуются существенно более высокие дозы, которые может быть трудно безопасно реализовать у пациентов. Для Y220N нынешнее соединение, по-видимому, недостаточно, чтобы полностью исправить p53 в реалистичных условиях. Тем не менее структурные чертежи, представленные в этой работе, показывают, почему текущая конструкция работает хуже, и как будущие молекулы можно изменить, чтобы взаимодействовать со всеми тремя вариантами боковых цепей, не вынуждая их занимать неблагоприятные позиции. Иными словами, создание по-настоящему «пан‑Y220» препарата для восстановления p53 выглядит сложной, но достижимой задачей и могло бы умеренно расширить число пациентов, которые могли бы получить пользу от этого нового подхода — ремонта, а не замены — собственного опухолевого супрессора организма.
Цитирование: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Ключевые слова: реактивация p53, резатапопт, мутация Y220C, прецизионная медицина при раке, стабилизация белка