Clear Sky Science · ru
Дебубиквитинирование OTUD4 стабилизирует EGFR и активирует путь PI3K/AKT, способствуя инвазивности тройного‑негативного рака молочной железы
Почему это исследование важно для рака молочной железы
Тройной‑негативный рак молочной железы — одна из самых труднолечимых форм рака молочной железы, поскольку в ней отсутствуют обычные гормональные и ростовые маркеры, на которые нацелены многие препараты. В этом исследовании обнаружена скрытая «защитная» молекула, которая помогает раковым клеткам поддерживать включенным мощный переключатель роста. Поняв эту незаметную систему поддержки, учёные могут найти новые способы прервать сигналы, приводящие к росту и распространению опухоли.
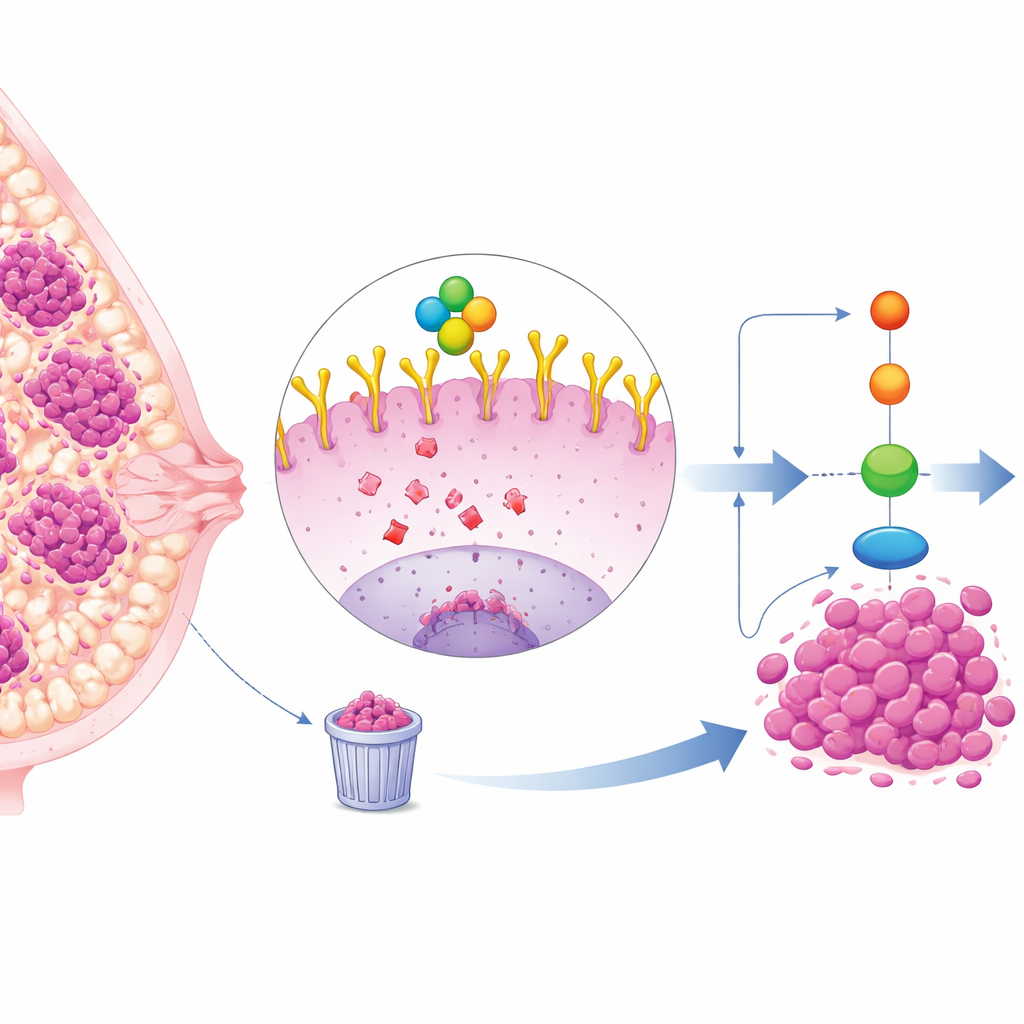
Трудноизлечимый подтип рака молочной железы
Тройной‑негативный рак молочной железы (TNBC) составляет примерно четверть случаев рака молочной железы и обычно растёт и метастазирует быстрее, чем другие подтипы. Поскольку клетки TNBC не несут рецепторов эстрогена, прогестерона или HER2, стандартные таргетные терапии менее эффективны, и в основном остаются химиотерапия и хирургия. Однако многие опухоли TNBC демонстрируют высокий уровень белка на поверхности клетки EGFR, который действует как антенна для приёма сигналов роста и выживания. Высокий уровень EGFR связан с плохим прогнозом, но препараты, прямо блокирующие EGFR, в клинике показали разочаровывающие результаты, что указывает на более глубокие уровни регуляции.
Нахождение скрытого помощника роста опухоли
Исследователи сосредоточили внимание на OTUD4 — ферменте, который снимает с белков маленькие метки, называемые убиквитином. Эти метки часто служат сигналами утилизации, помечая белки для разрушения, поэтому их удаление может стабилизировать и защитить помеченный белок. Используя крупные онкологические базы данных и образцы тканей пациентов, команда показала, что OTUD4 присутствует в повышенных количествах в опухолях TNBC и в клеточных линиях по сравнению с нормальной тканью молочной железы. У пациентов с опухолями, содержащими больше OTUD4, наблюдалась худшая выживаемость, что указывает на то, что OTUD4 ведёт себя как онкоген — ген, способствующий прогрессированию рака.
Как OTUD4 делает раковые клетки более агрессивными
Чтобы проверить роль OTUD4 в клетках TNBC, учёные понизили его уровень в двух широко изучаемых клеточных линиях TNBC. При уменьшении OTUD4 клетки росли медленнее, образовывали меньше колоний и были менее подвижны в тестах заживления ран и Transwell, что свидетельствует о снижении агрессивности. При увеличении уровня OTUD4 наблюдалось противоположное: клетки пролиферировали быстрее и активнее мигрировали, что подтверждает идею о том, что OTUD4 стимулирует злокачественное поведение. В экспериментах на мышах опухоли, сформированные из клеток с дефицитом OTUD4, росли медленнее и демонстрировали уменьшенные маркеры деления клеток и сигналы роста, подтверждая эти эффекты in vivo.
Молекулярный щит, защищающий EGFR
Изучая механизм, команда использовала скрининг взаимодействий белок‑белок и биохимические тесты, чтобы идентифицировать EGFR как прямого партнёра по связыванию OTUD4. Они обнаружили, что OTUD4 прикрепляется к определённому участку EGFR и удаляет K48‑связанные цепочки убиквитина — тип метки, который обычно помечает белки для разрушения клеточным «перерабатывающим» аппаратом. При снижении OTUD4 EGFR разлагался быстрее, хотя активность его гена оставалась неизменной, что показывает, что OTUD4 действует после синтеза EGFR, а не на уровне ДНК или РНК. Блокирование системы утилизации белков восстанавливало уровни EGFR, подчёркивая, что ключевой этап — защита от разрушения. При стабильно высоком уровне EGFR на поверхности клетки важный внутриклеточный сигнальный маршрут, путь PI3K/AKT/mTOR, остаётся включённым, стимулируя рост и выживание клеток.
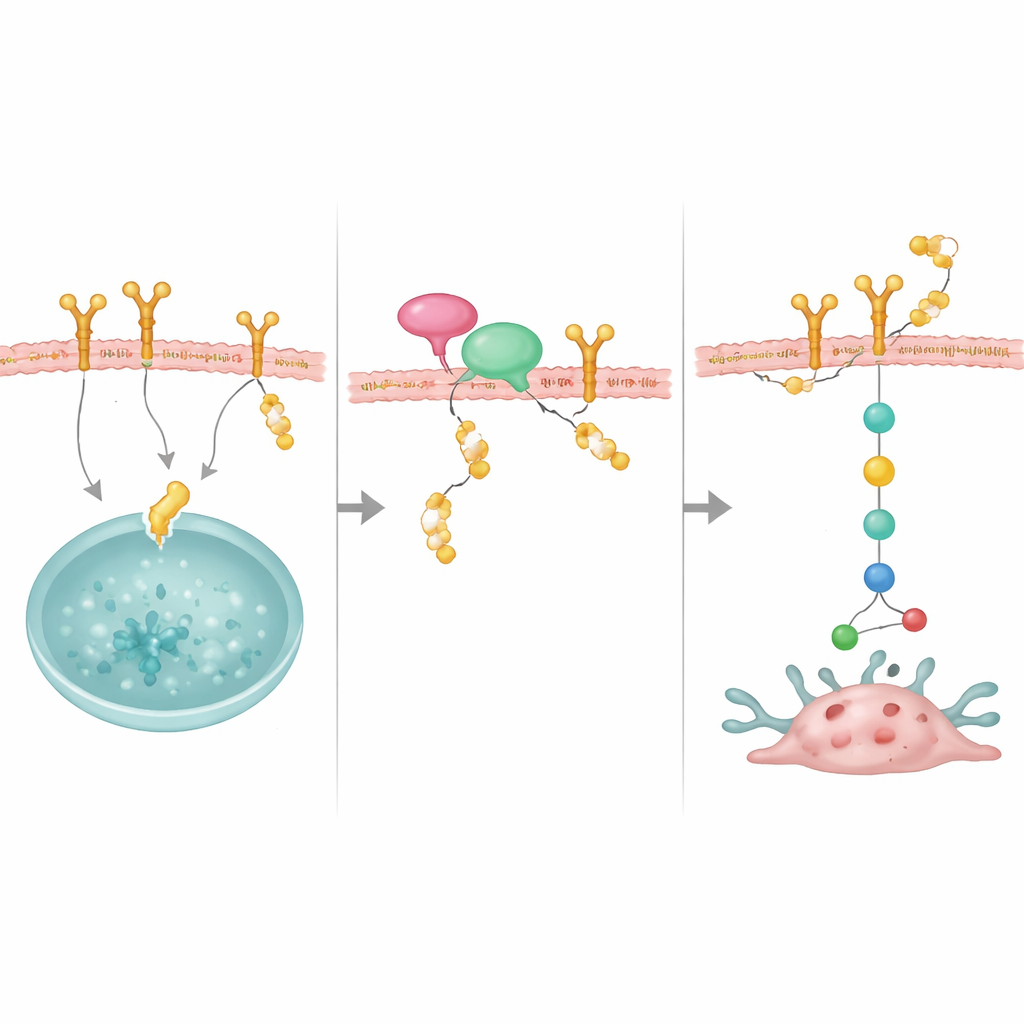
Адаптор, который приводит защитника к его цели
В исследовании также выявили важного партнёра — NRP1, мембранный белок, ранее связанный с агрессивными формами рака молочной железы. NRP1 связывается и с OTUD4, и с EGFR и способствует привлечению OTUD4 в позицию, где он может спасти EGFR от разрушения. При снижении NRP1 EGFR становился менее стабильным, а его сигналы роста ослабевали, хотя уровни OTUD4 не изменялись. Переизбыток OTUD4 частично компенсировал потерю NRP1, что указывает на то, что NRP1 действует как док‑платформа, рекрутируя OTUD4 к EGFR. Вместе эти молекулы образуют стабилизирующий комплекс, который поддерживает высокий уровень EGFR на поверхности клетки.
Что это значит для будущего лечения
Раскрывая, как OTUD4 и NRP1 совместно защищают EGFR от разрушения, это исследование выявляет новую точку контроля ключевого сигнала роста в тройном‑негативном раке молочной железы. Вместо попыток блокировать активность EGFR на его активном участке будущие терапии могут быть направлены на нарушение защитной функции OTUD4 или его рекрутирования NRP1, что снизит уровни EGFR и ослабит путь PI3K/AKT, питающий рост опухоли. Хотя потребуется дополнительная работа для поиска безопасных и эффективных ингибиторов OTUD4 и для выяснения возможных путей ускользания, которые могут использовать раковые клетки, эти результаты открывают перспективные направления для более точных терапий против этого сложного подтипа рака молочной железы.
Цитирование: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Ключевые слова: тройной‑негативный рак молочной железы, сигнализация EGFR, OTUD4, путь PI3K AKT, распад белка