Clear Sky Science · ru
Дегидрогеназа короткоцепочечных ацил-КоА запускает деметилирование и утечку митохондриальной ДНК, подпитывая антитуморный иммунитет при колоректальном раке
Почему наши собственные клетки иногда прячут рак от иммунной системы
Колоректальный рак — одна из самых смертоносных опухолей в мире, отчасти потому что иммунная система часто не признаёт и не атакует его. В этом исследовании выявлена неожиданная связь между тем, как раковые клетки «сжигают» жиры, как их крошечные электростанции (митохондрии) обращаются со своей ДНК и узнаёт ли иммунная система о наличии опухоли. Проследив эту цепочку событий, исследователи также выделили старое природное соединение, гиперицин, как потенциальный способ вновь пробудить иммунную атаку при колоректальном раке.
Отсутствующий митохондриальный «страж» в опухолях кишечника
Команда начала с поиска в крупных наборах данных человека и мыши генов метаболизма, устойчиво изменяющихся при колоректальном раке. Выделился один фермент: дегидрогеназа короткоцепочечных ацил-КоА (ACADS), которая обычно помогает митохондриям расщеплять короткие жирные кислоты. В образцах пациентов и в нескольких моделях на мышах уровень ACADS был заметно снижен в опухолевой ткани по сравнению с близлежащей здоровой слизистой. При снижении ACADS в клетках колоректального рака мышей опухоли росли быстрее и становились более агрессивными; повышение уровня ACADS замедляло рост опухолей. Мыши, у которых специально в эпителии кишечника отсутствовал ACADS, развивали больше и более крупные опухоли в химической модели рака, связанного с колитом, что подтверждает идею о том, что ACADS действует как супрессор опухолей в кишечнике.
Как опухоли приглушают сигналы тревоги для иммунитета
Эти эффекты на рост нельзя было объяснить только скоростью деления раковых клеток в культуре — она менялась мало. Вместо этого потеря ACADS стимулировала рост опухолей только у животных с целой иммунной системой, что указывает на изменения в микросреде опухоли. Анализ отдельных клеток в образцах человеческого колоректального рака показал, что опухоли с низким уровнем ACADS окружены большим числом опухолевых и подавляющих иммунных клеток — таких как миелоидные клетки-подавители, определённые макрофаги и регуляторные Т-клетки — и меньшим количеством полезных эффекторных Т-клеток и естественных киллеров. Этот профиль указывает на «иммуносупрессивный квартал», который укрывает опухоль от атаки. 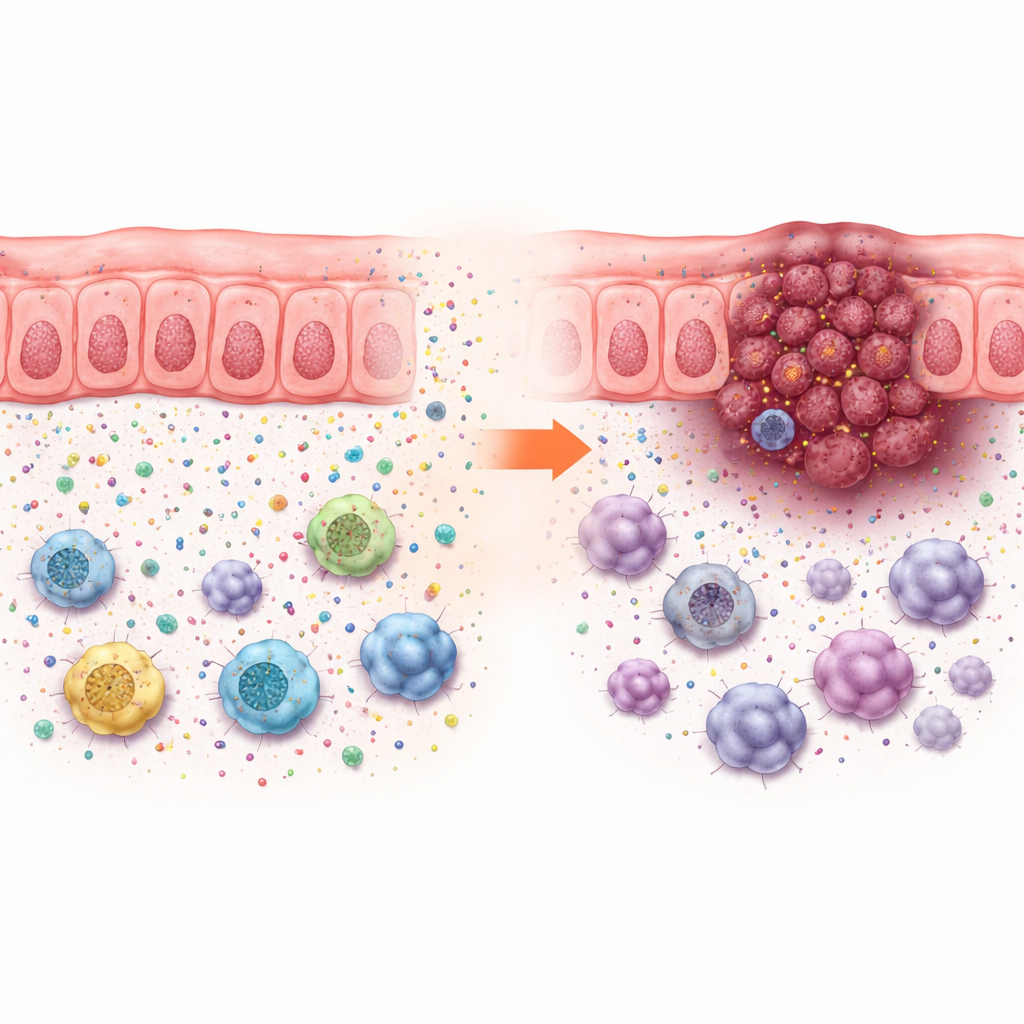
Утечка митохондриальной ДНК как скрытый триггер
Что связывает фермент, расщепляющий жиры, с чувствителем ДНК иммунной системы? Ответ — в митохондриальной ДНК (мтДНК). При стрессе фрагменты мтДНК могут просачиваться из митохондрий в цитоплазму, где cGAS распознаёт их как сигнал опасности. Исследователи показали, что клетки рака с дефицитом ACADS имели меньше мтДНК именно в этой компартменте, хотя общий уровень мтДНК оставался неизменным. Блокирование утечки мтДНК в клетках с высоким ACADS выключало cGAS–STING, что подтвердило, что именно эти сбежавшие фрагменты ДНК являются критической сигнализацией. Удивительно, что классические факторы митохондриального стресса — такие как реактивные формы кислорода, всплески кальция и значительные изменения формы митохондрий — не могли полностью объяснить разницу. Вместо этого исследование указывает на «ворота» в митохондриальной мембране и, что более важно, на химические метки на самой мтДНК. 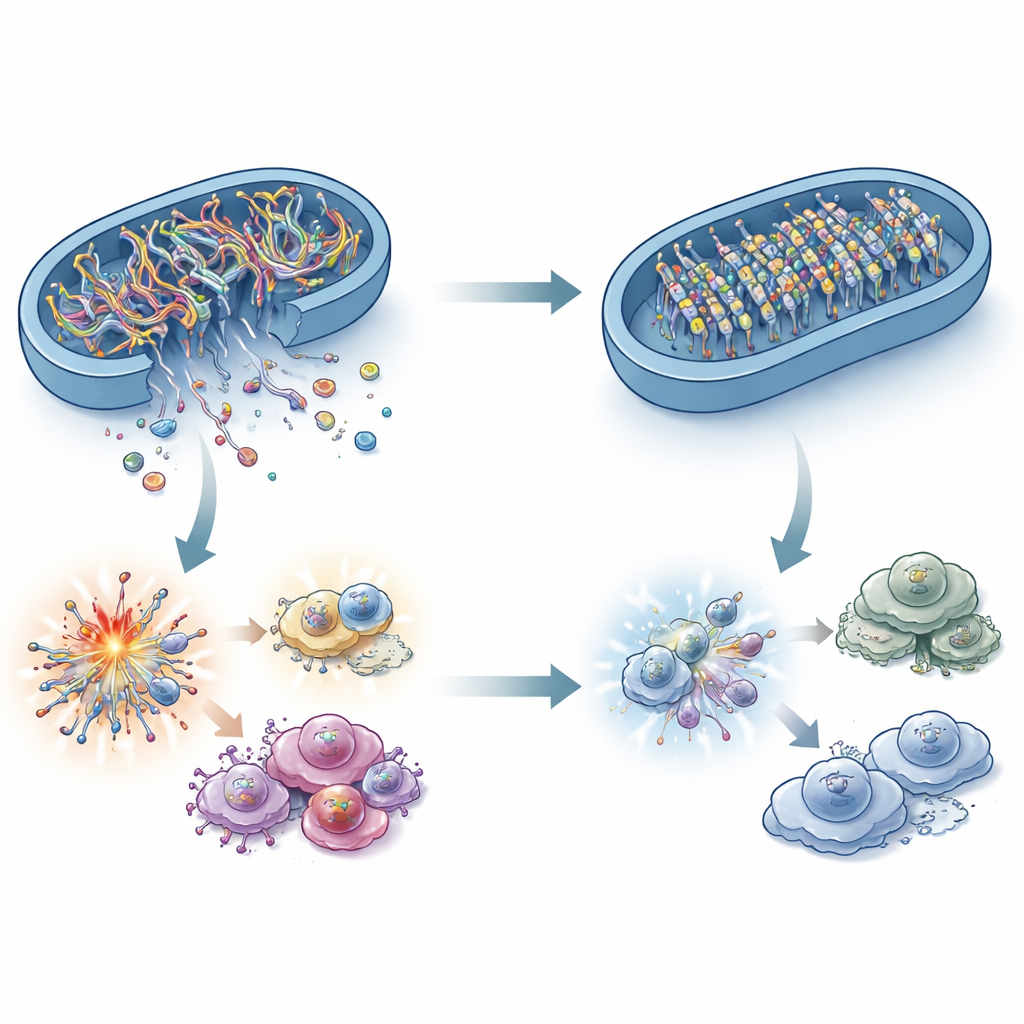
Партнёр по метилированию ДНК, который запирает сигнал тревоги
Через скрининг белковых взаимодействий было обнаружено, что ACADS ассоциируется с формой фермента метилирования ДНК DNMT1, локализующейся в митохондриях. При утрате ACADS этот митохондриальный DNMT1 накапливался, добавляя дополнительные метильные группы на мтДНК. Эти метки делают мтДНК более стабильной и менее склонной к разрывам и утечке. Перегрузка клеток митохондриальным DNMT1 уменьшала уход мтДНК, подавляла сигнализацию cGAS–STING и ускоряла рост опухолей, тогда как блокирование DNMT1 препаратом децитабином восстанавливало утечку мтДНК и замедляло рост опухолей с дефицитом ACADS. Образцы пациентов отражали эти выводы: низкий ACADS коррелировал с высоким митохондриальным DNMT1, ослабленной сигнализацией STING, меньшим числом эффекторных Т-клеток, большим количеством подавляющих иммунных клеток и худшим прогнозом ответа на ингибиторы контрольных точек иммунитета.
Пробуждение иммунной защиты старым соединением
Чтобы выяснить, можно ли использовать этот путь в терапевтических целях, исследователи провели компьютерный скрининг в поисках молекул, связывающихся с ACADS. Они выделили гиперицин, природный пигмент, ранее тестировавшийся как светочувствительная терапия при некоторых кожных лимфомах. В клетках колоректального рака гиперицин повышал уровень ACADS, снижал митохондриальный DNMT1, увеличивал утечку мтДНК и реактивировал сигнализацию cGAS–STING — изменения, зависящие от наличия ACADS. В моделях опухолей на мышах и в краткосрочных культурах человеческих опухолей лечение гиперицином уменьшало размер опухолей или смещало иммунный состав в сторону более активного, обогащённого Т-клетками состояния. Хотя необходимы дополнительные исследования перед клиническим применением, эти результаты предполагают, что фармакологическое «включение» ACADS может помочь превратить «холодную», иммуносупрессивную опухоль в ту, которая лучше отвечает на иммунотерапию.
Что это значит для пациентов и будущих лечений
Проще говоря, эта работа показывает, что некоторые колоректальные раки растут отчасти потому, что они заглушают митохондриальный фермент, который обычно способствует утечке крошечных фрагментов ДНК в цитоплазму, где они служат сигналами для вызова иммунной системы. Позволив партнёру по метилированию ДНК «запереть» эту митохондриальную ДНК на месте, опухоли с дефицитом ACADS скрывают эти сигналы и избегают иммунного распознавания. Восстановление активности ACADS, например с помощью препаратов, подобных гиперицину, может вновь открыть этот митохондриальный сигнал тревоги, усилить антитуморный иммунитет и улучшить ответы на существующие иммунотерапии. ACADS, митохондриальный DNMT1 и активность пути STING могут поэтому служить полезными биомаркерами и мишенями в поиске более эффективных методов лечения колоректального рака.
Цитирование: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Ключевые слова: колоректальный рак, tumor immunity, митохондриальная ДНК, липидный метаболизм, путь cGAS-STING