Clear Sky Science · ru
Нацеливание на белок fused in sarcoma (FUS): новая анттисмысловая стратегия лечения идиопатического лёгочного фиброза
Почему здесь важно рубцевание лёгких
Идиопатический лёгочный фиброз (ИЛФ) — непрекращающееся заболевание лёгких, при котором тонкие воздушные мешочки постепенно превращаются в жёсткую рубцовую ткань, из‑за чего каждый вдох даётся с трудом. Современные препараты могут замедлить образование этих рубцов, но не способны остановить или обратить процесс. В этом исследовании изучают новую мишень — белок FUS, который помогает клеткам обрабатывать свои генетические сообщения, и тестируют, получится ли выключить его с помощью созданной нитевидной молекулы, схожей с ДНК, чтобы успокоить процесс фиброзирования и помочь повреждённым лёгким восстановиться.
Клеточный регулятор трафика, вышедший из строя
FUS — это белок, который обычно находится в ядре клетки и помогает управлять тем, как РНК — рабочая копия наших генов — обрабатывается и используется. При заболеваниях мозга, таких как БАС, FUS может вести себя ненадлежащим образом: покидать ядро, собираться в кластеры в цитоплазме и нарушать нормальные функции клетки. Авторы задали вопрос, не вызывает ли похожее нарушение образование рубцов при ИЛФ. Они изучали лёгочные фибробласты — клетки соединительной ткани, откладывающие рубцовое вещество — от пациентов с ИЛФ и от здоровых доноров. В клетках пациентов с ИЛФ общий уровень FUS был выше и, что важно, значительно больше FUS обнаруживалось в цитоплазме по сравнению со здоровыми клетками. С помощью высокоразрешающей электронной микроскопии они подтвердили, что этот белок аномально накоплен за пределами ядра, что указывает на возможное искажение его обычного контроля над РНК в фиброзных лёгких. 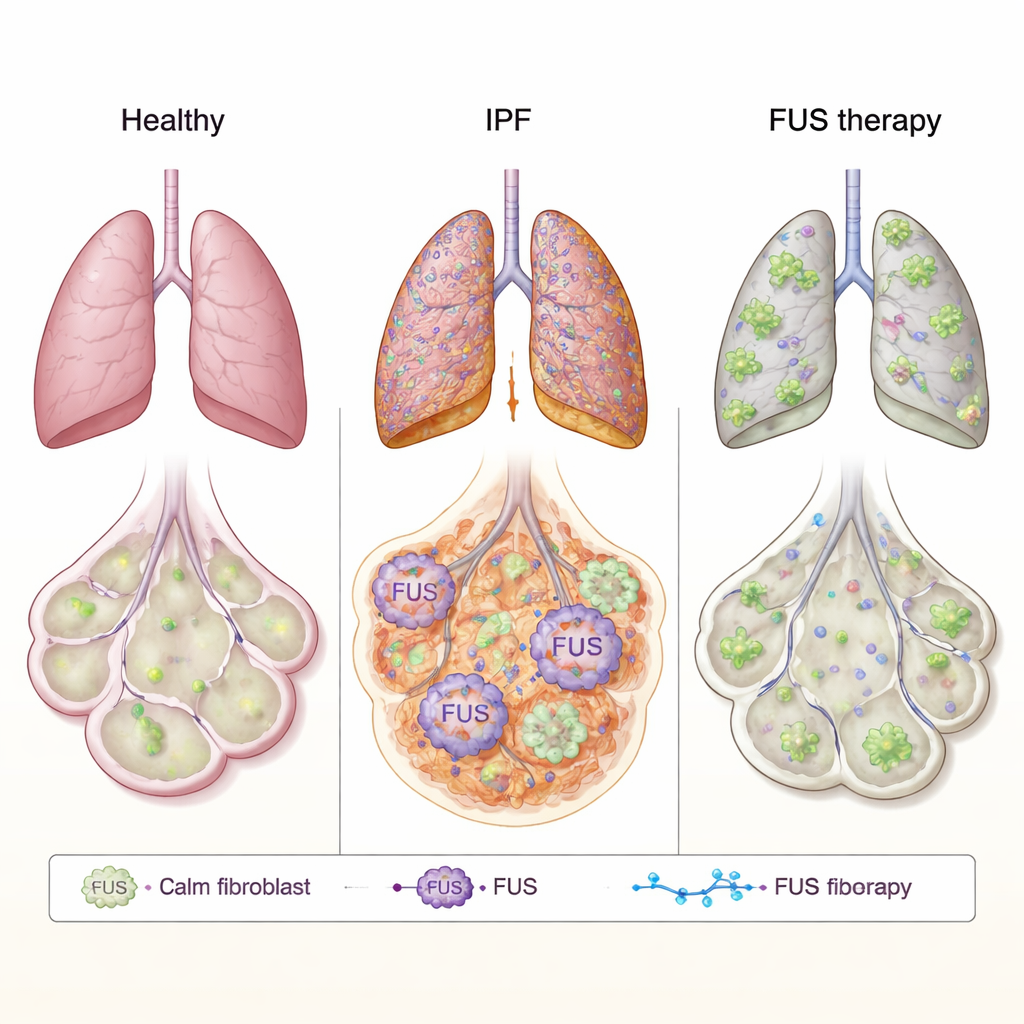
Как FUS подпитывает клетки‑рубцеобразователи
Чтобы понять, что делает этот «непослушный» белок, исследователи увеличивали экспрессию FUS в здоровых фибробластах и уменьшали её в клетках ИЛФ. Избыток FUS заставлял здоровые клетки делиться быстрее, тогда как снижение FUS в фибробластах ИЛФ замедляло их рост и движение — два поведения, ключевых для формирования рубцов. Команда затем использовала методику, которая «замораживает» комплексы белок–РНК и считывает, какие РНК связаны с FUS. В фибробластах ИЛФ FUS оказался прикреплённым к множеству генетических сообщений, продвигающих фиброз, включая те, что кодируют коллаген, факторы роста вроде TGF‑β и провоспалительные сигналы. Проще говоря, FUS функционировал как узловая точка, связывающая целую сеть пролонгирующих рубцевание сообщений.
Подавление сигнала прицельным препаратом
В исследовании протестировали антисмысловой олигонуклеотид ION363 — короткую химически модифицированную нитку, спроектированную для связывания РНК FUS и запуска её разрушения. При обработке фибробластов ИЛФ ION363 уровень FUS снижался, клетки замедляли пролиферацию и миграцию, а ключевые гены, участвующие в образовании рубца, затухали. Важно, что эффект не зависел от гибели клеток или принуждения их к старению; вместо этого наблюдалась перенастройка их поведения. Когда то же лечение применили к тонким срезам лёгочной ткани ИЛФ, поддерживаемым живыми в лаборатории, большие группы генов, связанных с внеклеточным матриксом, воспалением и аномальной эпителиальной выстилкой, были понижены, в то время как гены, ассоциированные с нормальным синтезом сурфактанта и функцией альвеол, усилились. Лечение также уменьшало окрашивание коллагена и увеличивало маркеры функциональных поверхностных клеток лёгкого, что предполагает смещение от рубцевания в сторону восстановления.
Помощь в восстановлении повреждённых альвеол
Поскольку клетки выстилки альвеол типа II критически важны для восстановления лёгких, исследователи создали трёхмерные «альвеолосферы» из клеток пациентов, чтобы имитировать миниатюрные лёгочные единицы. В культурах от пациентов с ИЛФ такие структуры обычно выживают плохо. При лечении ION363 формировалось больше альвеолосфер, они росли крупнее и демонстрировали повышенную лизосомную активность — признак активного обновления. Детальное окрашивание показало больше клеток с маркёрами зрелых газообменных клеток, что говорит о том, что подавление FUS не только успокаивает фибробласты, но и стимулирует повреждённый эпителий перестроить более здоровую поверхность. 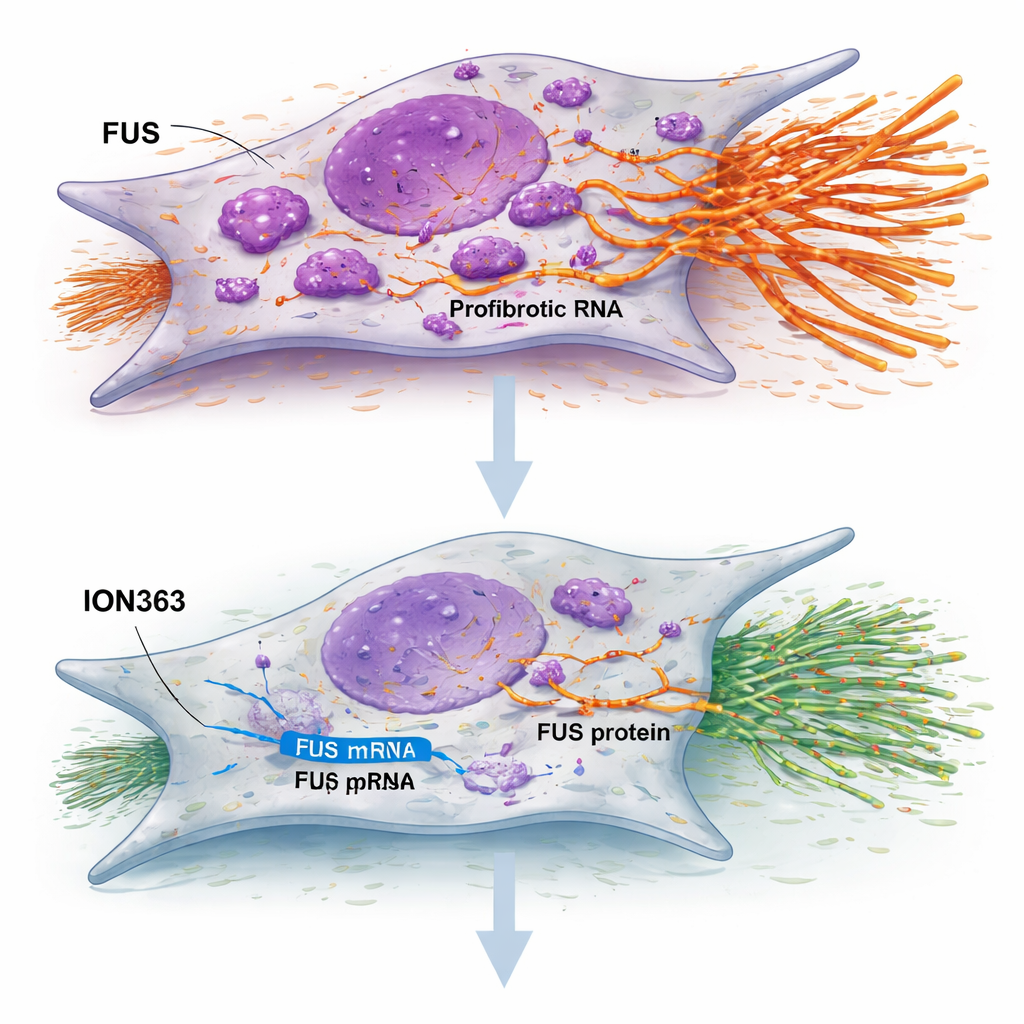
Что это может значить для пациентов
В сумме работа изображает FUS как главный переключатель при ИЛФ, связывающий гиперактивные рубцеобразующие фибробласты с нарушенным восстановлением тонких воздушных мешочков. Путём уменьшения активности FUS с помощью прицельного антисмыслового препарата исследователи смогли сократить профибротические генные программы, ослабить накопление коллагена и стимулировать регенерацию в моделях лёгких, полученных от пациентов. Хотя этот подход всё ещё находится на лабораторной стадии и потребует тщательной проверки на животных моделях и в клинических испытаниях, он даёт надежду на то, что ИЛФ в будущем можно будет лечить не только замедлением рубцевания, но и прямой перестройкой клеточных программ, контролирующих повреждение и восстановление лёгких.
Цитирование: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Ключевые слова: идиопатический лёгочный фиброз, антисмысловой олигонуклеотид, белок FUS, лёгочный фиброз, восстановление альвеол