Clear Sky Science · ru
Частичная усечённость C‑концевого домена PTCH1 в раке стимулирует опухолеобразование через неклассическую активацию петли GLI–PI3K
Почему небольшая белковая модификация имеет значение при раке толстой кишки
Рак толстой кишки обычно развивается вследствие медленного накопления генетических ошибок. В этом исследовании подробно рассмотрена неожиданно малая модификация белка на поверхности клетки — PTCH1 — и показано, как усечение части его «хвоста» может ускорять рост раковых клеток, облегчать их распространение и потенциально вызывать устойчивость к некоторым существующим препаратам. Понимание этого скрытого переключателя роста может открыть путь к новым, более точным методам лечения для подгруппы пациентов.
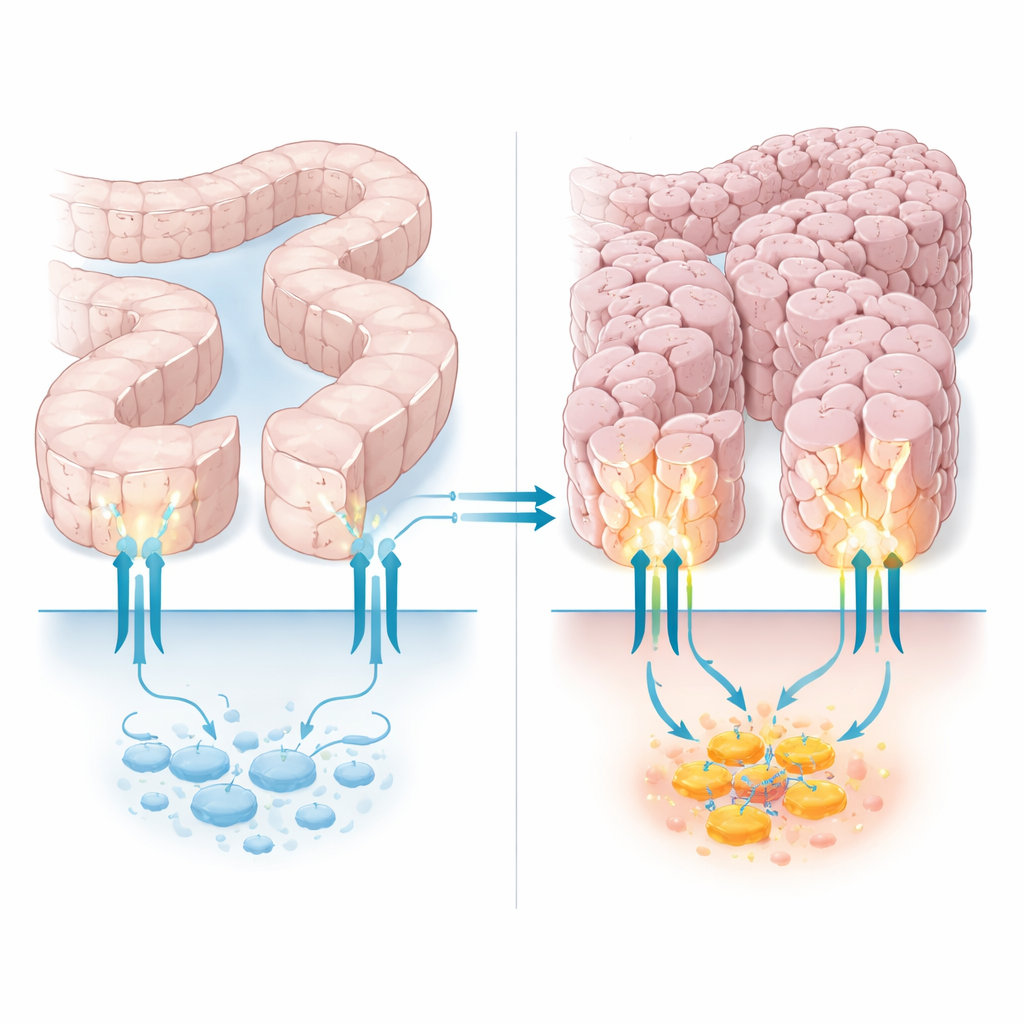
«Шлюз» клетки с незаметной дополнительной функцией
PTCH1 хорошо известен как «шлюз» пути Hedgehog, линии связи, которой клетки пользуются в онтогенезе и при восстановлении тканей. В классической роли PTCH1 сдерживает партнёра Smoothened и таким образом регулирует семейство контролёров ДНК — белков GLI. Но у PTCH1 также есть длинный, гибкий хвост, который располагается внутри клетки и служит площадкой для связывания других белков, влияющих на гибель клеток, переработку компонентов клетки и не только. Ранее было показано, что в некоторых опухолях кишечника, желудка и матки встречаются мутации, укорочивающие этот внутренний хвост. Эти мутации не нарушали классический переключатель Hedgehog, но повышали выживаемость раковых клеток в стрессовых условиях, что указывало на то, что сегмент хвоста тихо вносит вклад в противоопухолевую функцию PTCH1.
Создание модифицированных раковых клеток для проверки эффекта
Чтобы выяснить, что на самом деле делают эти мутации, исследователи использовали редактирование генома CRISPR/Cas9 для воссоздания их в клеточной линии рака толстой кишки. Они сравнили два отредактированных клона, каждый с разным усечением хвоста PTCH1, с генетически совпадающими клетками с нормальным PTCH1. Мутантные клетки делились быстрее, образовывали значительно больше колоний и успешно росли даже без прикрепления — поведение, связанное со способностью к метастазированию. При имлантации мышам клетки с усечённым хвостом формировали гораздо большие опухоли за несколько недель и содержали больше делящихся клеток. Важно, что у отредактированных клеток всё ещё синтезировался PTCH1 и сохранялась его основная роль «шлюза», что показывает: повышенная агрессивность связана с утратой специализированных внутриклеточных функций хвоста, а не с полной потерей PTCH1.
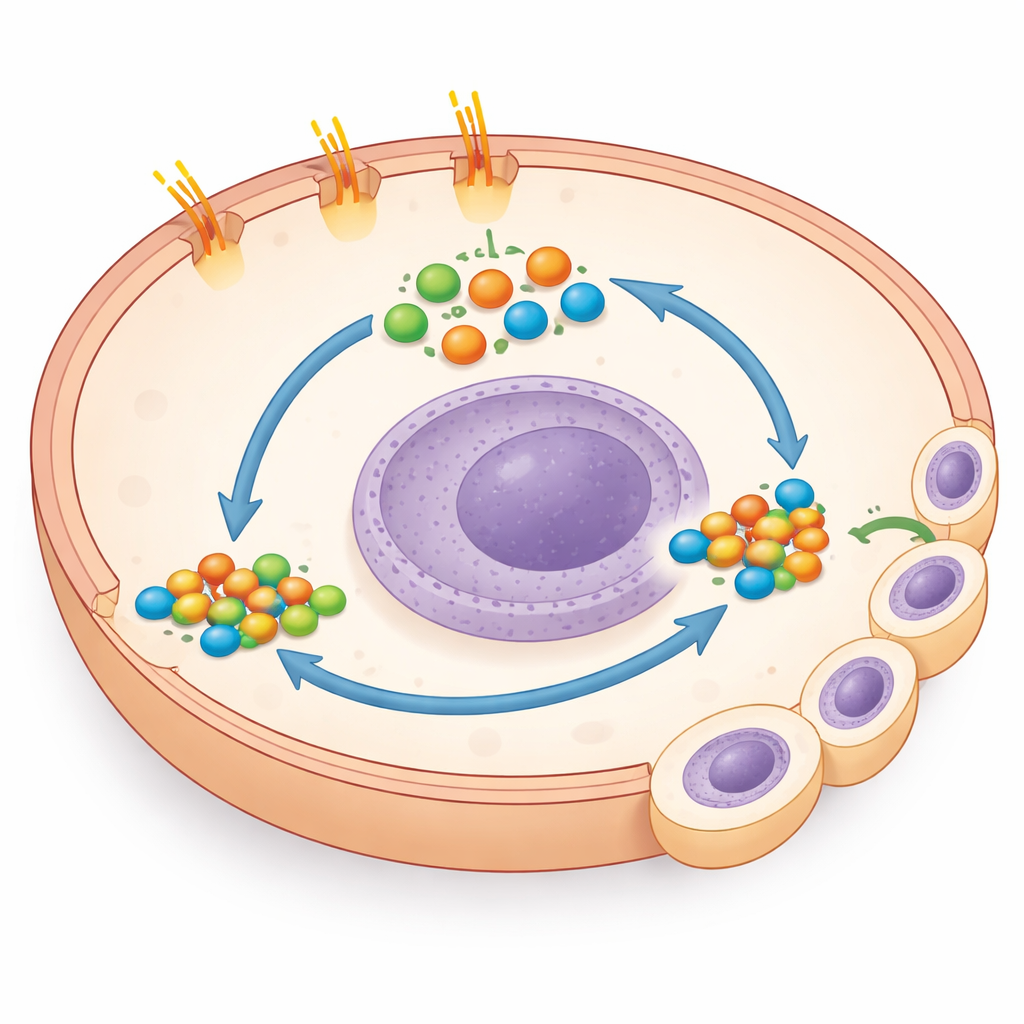
Неожиданный обходной путь к мощному переключателю роста
Изучая молекулярные механизмы, команда обнаружила неожиданное явление: в клетках с усечённым хвостом резко повысились уровни GLI1 и GLI2 — ключевых драйверов генетических программ роста и выживания. Обычно активность GLI растёт при включении Smoothened, но блокирование Smoothened здесь не влияло на ситуацию. Вместо этого прямое подавление GLI малой молекулой или уменьшение уровня GLI1 генетическими методами резко снижало рост мутантных клеток в культурах и в дополнительных линиях клеток рака толстой кишки, которые естественно несут мутации хвоста PTCH1. Это показало, что потеря хвоста активирует GLI по «неклассическому» пути, минуя обычный переключатель Hedgehog, и что раковые клетки сильно зависят от этого обходного механизма для своего агрессивного поведения.
Активируются многочисленные ростовые цепи, но доминирует одна петля
Секвенирование РНК выявило тысячи генов с изменённой активностью при усечении хвоста PTCH1. Многие из них принадлежат известным онкогенным цепям, включая контролируемые рецептором эпидермального фактора роста (EGFR), Ras и сигнальными системами, регулирующими метаболизм и стволовые свойства клеток. Мутантные клетки демонстрировали повышенную активность EGFR и его лигандов, а также усиление двух основных нисходящих путей: MAPK и PI3K/Akt. Тем не менее блокада EGFR или его ветви MAPK лишь частично замедляла мутантные клетки. Напротив, низкие дозы ингибиторов PI3K существенно ограничивали их рост и образование колоний и снижали уровни GLI1, указывая на PI3K/Akt как критического партнёра в этом новом механизме активации GLI.
Самоподдерживающаяся петля, питающая рост опухоли
Дальнейшие эксперименты выявили цикл обратной связи: усечение хвоста PTCH1 повышает активность GLI; GLI, в свою очередь, поддерживает высокий уровень сигнальной активности PI3K/Akt; а PI3K/Akt способствует стабилизации и активации GLI. Нарушение либо GLI, либо PI3K разрушало эту петлю и лишало мутантные клетки преимущества в росте, тогда как простое усиление PI3K/Akt не могло компенсировать прямую блокаду GLI. Также наблюдалось подавление активности PKA — фермента, который обычно метит белки GLI для инактивации, что, вероятно, ещё сильнее смещает баланс в пользу программ, управляемых GLI.
Что это может значить для будущего лечения
Для пациентов главный вывод таков: в некоторых раках толстой кишки есть мутации хвоста PTCH1, которые незаметно подключают положительную петлю обратной связи GLI–PI3K, помогая опухолям расти и обходить препараты, нацеленные на более знакомый переключатель Hedgehog или путь EGFR–MAPK. Такие опухоли могут особенно чувствительно реагировать на лечение, направленное на прямое подавление GLI или на PI3K/Akt. Работа указывает, что секвенирование PTCH1 в опухолях толстой кишки — особенно справа расположенных опухолях, где такие мутации встречаются чаще — может помочь выявить пациентов, которые выиграют от стратегий, нацеленных на PI3K или GLI, превратив тонкую модификацию белка в полезный терапевтический маркер.
Цитирование: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Ключевые слова: рак толстой кишки, Hedgehog‑сигнализация, мутации PTCH1, транскрипционные факторы GLI, путь PI3K–Akt