Clear Sky Science · pt
Tecnologias de sensoriamento multimodal para bios vigilância de HPAI em sistemas de produção avícola
Por que a gripe aviária nas fazendas importa para todos
A influenza aviária altamente patogênica, frequentemente chamada de HPAI ou gripe das aves, deixou de ser apenas um problema para galinhas em fazendas distantes. Ondas recentes da cepa H5N1 dizimaram mais de 168 milhões de aves nos Estados Unidos, elevaram bruscamente os preços dos ovos e até se espalharam para bovinos leiteiros e pessoas. Este artigo de revisão explica como novas tecnologias “inteligentes” de sensoriamento — ouvir sons dos animais, amostrar o ar do galpão e realizar testes genéticos rápidos no local — podem detectar surtos mais cedo, proteger o abastecimento de alimentos e reduzir o risco de que um vírus influenza perigoso se adapte para se disseminar facilmente entre humanos.
A ameaça crescente nas fazendas e nas pessoas
Nos últimos anos, um novo ramo do vírus H5N1 (clado 2.3.4.4b) espalhou-se amplamente pela avicultura dos EUA e, mais recentemente, por rebanhos leiteiros. Cada surto força os produtores a abater lotes inteiros, gerando prejuízos superiores a 1,4 bilhão de dólares e provocando quedas súbitas no fornecimento de ovos e carne. Ao mesmo tempo, mais de 70 infecções humanas foram registradas nos Estados Unidos, principalmente entre trabalhadores de baixa renda que lidam com animais infectados e frequentemente têm acesso limitado a serviços de saúde. Mapas e dados de vigilância mostram que ondas de H5N1 em aves frequentemente se sobrepõem aos picos sazonais de gripe em pessoas durante o inverno, criando um cenário de risco compartilhado na interface animal–humano. Essa sobreposição torna especialmente importante monitorar o que acontece em galpões e pastagens, além do que ocorre nas clínicas.
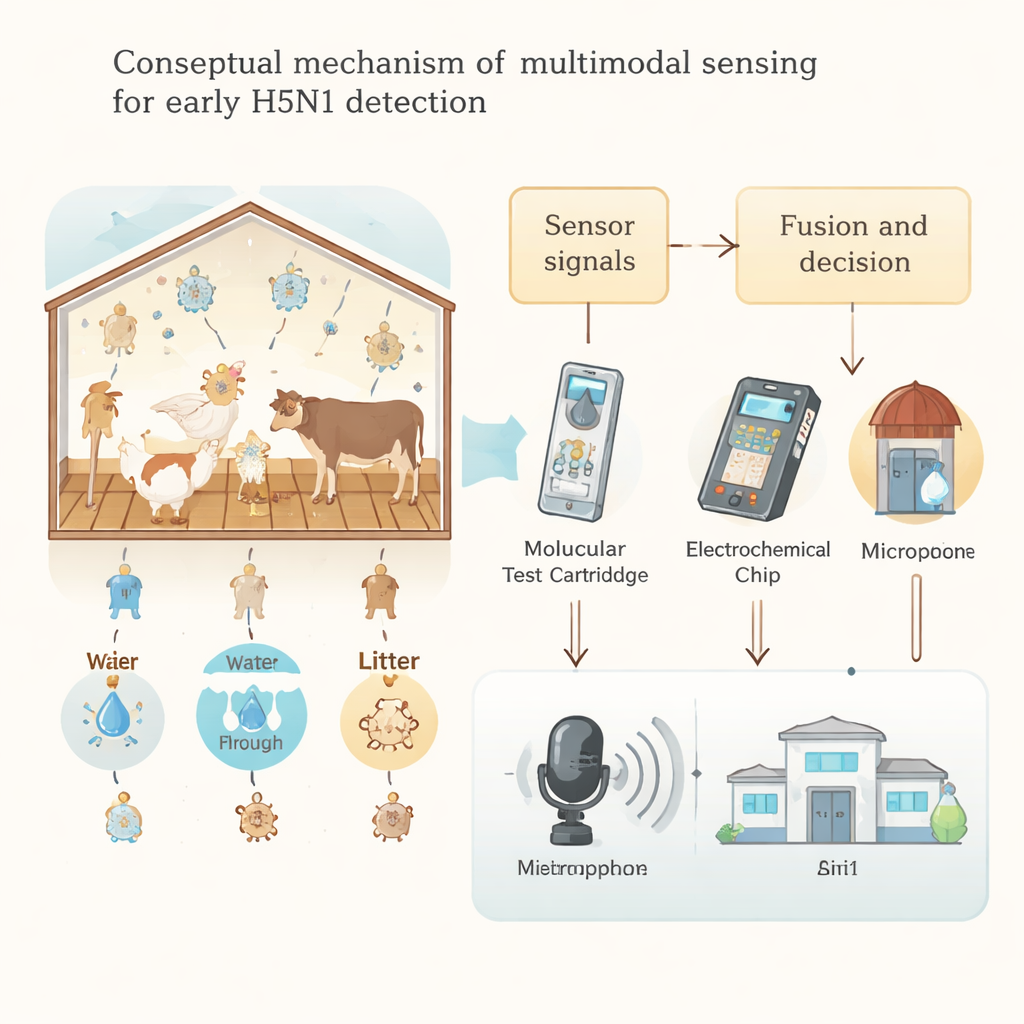
Como esse vírus funciona e por que se espalha tão facilmente
Os vírus da influenza aviária são partículas pequenas e envelopadas que carregam seu material genético em oito segmentos de RNA separados. Duas proteínas de superfície, hemaglutinina (H) e neuraminidase (N), originam rótulos familiares como H5N1 ou H3N2 e determinam quais espécies o vírus pode infectar e quão grave a doença pode ser. Cepas de baixa patogenicidade permanecem majoritariamente no trato intestinal e respiratório das aves e muitas vezes causam poucos sinais visíveis. Em contraste, cepas altamente patogênicas como a H5N1 atual têm um “sítio de clivagem” especial na proteína H que permite ao vírus multiplicar-se por todo o corpo, levando à morte súbita em até 90–100% das aves afetadas. O genoma segmentado também facilita que vírus influenza de diferentes hospedeiros troquem fragmentos e evoluam, razão pela qual infecções entre espécies — em bovinos, felinos ou animais selvagens — são tão preocupantes: cada novo hospedeiro é uma oportunidade para o vírus mudar.
Limites da biossegurança e dos testes atuais
Empresas avícolas já seguem regras rígidas de biossegurança, incluindo controle de acesso, desinfecção e inspeções visuais de saúde. Ainda assim, grandes surtos de HPAI ocorreram mesmo em fazendas que cumprem esses padrões. Uma razão é a velocidade: a vigilância tradicional depende de notar aves doentes, coletar swabs e enviá-los a um laboratório distante para testes por PCR, processo que pode levar dois ou três dias. Como a H5N1 pode dizimar um lote em cerca de 48 horas, esse atraso abre uma janela para que o vírus se espalhe pelos galpões e entre fazendas. Amostrar aves suficientes em lotes gigantes também é difícil, e protocolos rotineiros raramente testam poeira, água ou superfícies onde o vírus pode persistir sem ser notado. Como resultado, infecções iniciais, casos leves e baixos níveis de contaminação frequentemente passam despercebidos.
Ouvir, cheirar e ver: novas maneiras de detectar surtos
Os autores defendem que as fazendas precisam de sensoriamento multimodal — múltiplas formas complementares de vigiar problemas. No lado direcionado estão ferramentas que procuram diretamente o vírus ou seus componentes: métodos portáteis que amplificam RNA viral a temperatura única, testes programáveis baseados em CRISPR que entregam resultados em menos de uma hora, e biossensores eletroquímicos e ópticos compactos que podem detectar proteínas virais no ar, na água ou em swabs. No lado não direcionado estão métodos que buscam sinais gerais de doença sem identificar qual microrganismo é responsável, como câmeras térmicas que detectam febre, lasers que leem impressões químicas da poeira do galpão e sistemas de microfones que aprendem os padrões sonoros de lotes saudáveis e doentes. Por exemplo, modelos de deep learning podem detectar mudanças sutis nas vocalizações de frangos um a dois dias antes da doença se tornar óbvia, enquanto métodos avançados de espalhamento de luz podem distinguir moléculas relacionadas ao vírus em aerossóis misturados à poeira comum do galpão.
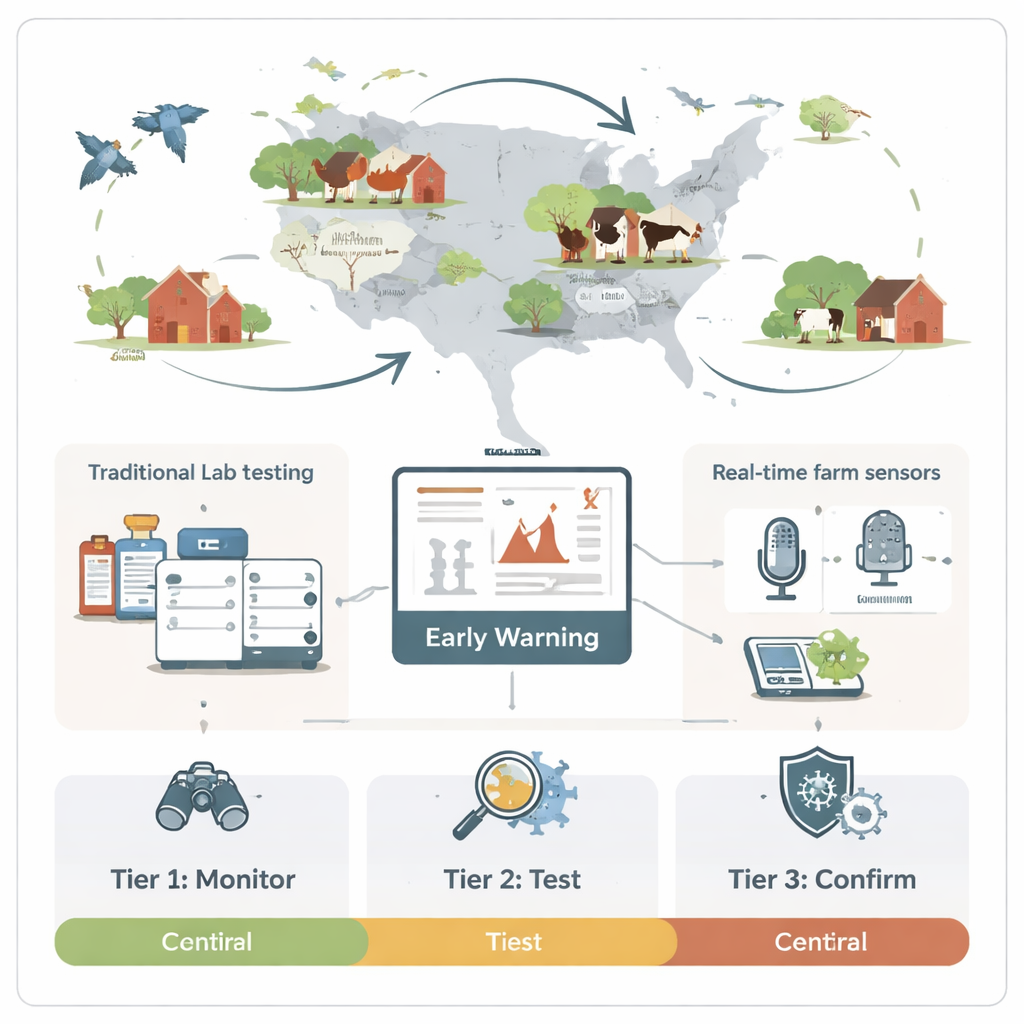
Construindo um sistema de alerta precoce em níveis
Em vez de usar todas as ferramentas em todos os lugares, a revisão propõe um sistema em três níveis. No Nível 1, sensores de baixo custo operam continuamente em segundo plano, detectando tosses anormais, monitorando partículas no ar ou escaneando poeira em busca de assinaturas químicas suspeitas. Se esses alarmes amplos ultrapassarem um limiar, entra o Nível 2: testes moleculares rápidos no local e biossensores verificam amostras direcionadas, como concentrações de ar ou swabs, tipicamente em 30–60 minutos. Somente quando esses exames mais rápidos indicam perigo real começa o Nível 3, com testes confirmatórios de laboratório como painéis PCR completos ou isolamento viral que levam um dia ou mais. Essa abordagem em etapas equilibra velocidade e confiabilidade, reduzindo pânico por falsos alarmes enquanto ainda ganha um tempo precioso em comparação com esperar que aves morram ou trabalhadores adoeçam visivelmente.
O que isso significa para segurança alimentar e da saúde
Em termos simples, o artigo conclui que combater a gripe aviária moderna exige que as fazendas se comportem mais como fábricas inteligentes e menos como galpões isolados. Ao combinar ouvidos (monitoramento acústico), narizes (sensores químicos e moleculares) e cérebros (algoritmos de fusão de dados) por meio dos setores animal, ambiental e de saúde humana, a agricultura pode passar de reagir a desastres para antecipá‑los. A detecção mais precoce significa menos abates em massa, preços mais estáveis para ovos, carne e leite, e menores chances de que a H5N1 adquira as mutações certas para iniciar uma pandemia humana. Ainda há obstáculos — custo das tecnologias, necessidade de treinamento de trabalhadores e o desafio de combinar dados ruidosos de sensores muito diferentes —, mas o sensoriamento multimodal oferece um caminho realista para fazendas mais seguras e uma vigilância One Health mais robusta para todos.
Citação: Ali, M.A., Ataei Kachouei, M., Jacobs, L. et al. Multimodal sensing technologies for HPAI biosurveillance in poultry production systems. npj Biosensing 3, 11 (2026). https://doi.org/10.1038/s44328-025-00075-6
Palavras-chave: influenza aviária, biossensores, vigilância em fazendas, diagnósticos CRISPR, monitoramento acústico