Clear Sky Science · pt
Percepções em célula única sobre a heterogeneidade trofoblástica e a disfunção adaptativa na restrição seletiva do crescimento fetal
Quando um dos gêmeos fica para trás
Para pais que esperam gêmeos, é profundamente preocupante quando um bebê deixa de crescer tão bem quanto o outro, apesar de compartilharem o mesmo útero e placenta. Essa condição, chamada restrição seletiva do crescimento fetal, não só ameaça a saúde do gêmeo menor antes do parto, como também pode moldar o desenvolvimento a longo prazo. Este estudo utiliza análise de ponta em célula única para examinar o interior da placenta compartilhada nessas gestações, revelando como mudanças sutis em tipos específicos de células placentárias e nas respostas imunes podem desequilibrar o crescimento saudável e levar a uma escassez perigosa.
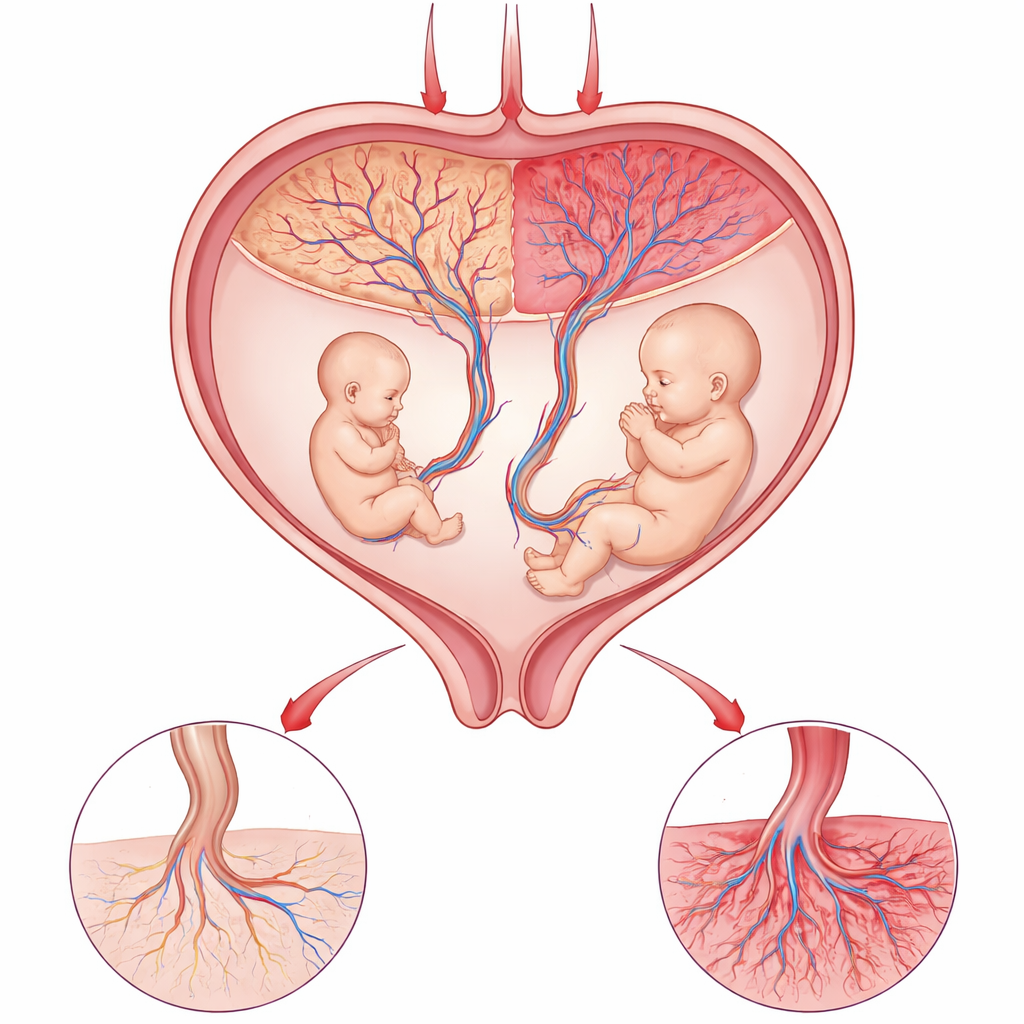
O delicado ato de equilíbrio da placenta
A placenta é a linha de vida entre mãe e bebê, fornecendo oxigênio e nutrientes enquanto remove resíduos. Em certas gestações de gêmeos idênticos, ambos compartilham uma única placenta, mas ocupam territórios diferentes dentro dela. Quando um gêmeo se torna muito menor que o outro, os médicos sabem que algo falhou localmente nesse órgão compartilhado. Como os gêmeos têm a mesma mãe e genes quase idênticos, eles oferecem um experimento natural poderoso: quaisquer diferenças marcantes no crescimento provavelmente advêm de como suas respectivas partes da placenta estão funcionando, em vez de diferenças nos próprios bebês.
Ampliando para as células placentárias individuais
Os pesquisadores coletaram amostras placentárias de três gestações nas quais um dos gêmeos estava significativamente menor que o outro. Usando sequenciamento de RNA em célula única — um método que lê a atividade de milhares de genes em células individuais — eles perfilaram mais de 175.000 células das diferentes regiões placentárias. Isso permitiu classificar as células em tipos distintos, incluindo células de suporte, células vasculares e vários tipos de células imunes. O foco recaiu sobre um grupo-chave chamado citotrofoblastos vilosos, uma camada de células que reveste as projeções em forma de dedo onde o sangue materno encontra a circulação fetal e que continuamente reabastece e repara a superfície da placenta.
Dois estados celulares principais: estrutura versus modo de sobrevivência
Dentro desses citotrofoblastos vilosos, a equipe descobriu dois estados maiores com papéis muito diferentes. Um grupo, marcado por uma molécula chamada TP63, atuava como zeladores estruturais: apoiavam a barreira entre mãe e bebê, mantinham conexões entre células e ajudavam a manter o tecido organizado. O outro grupo, marcado por uma enzima chamada LDHA, estava orientado para intensa produção de energia e enfrentamento de estresse, com vias associadas a mitocôndrias, estresse oxidativo e controle de qualidade proteica aumentadas. Nos territórios placentários dos gêmeos menores, as células protetoras TP63 estavam reduzidas, enquanto as células LDHA, dirigidas pelo estresse, expandiram-se e ciclaram com mais atividade. Análises computacionais de “trajetória” sugeriram que as células eram empurradas ao longo de um caminho do papel estrutural saudável rumo a um modo de sobrevivência, com menos células alcançando o estado totalmente fundido que normalmente mantém uma superfície de troca lisa e eficiente.
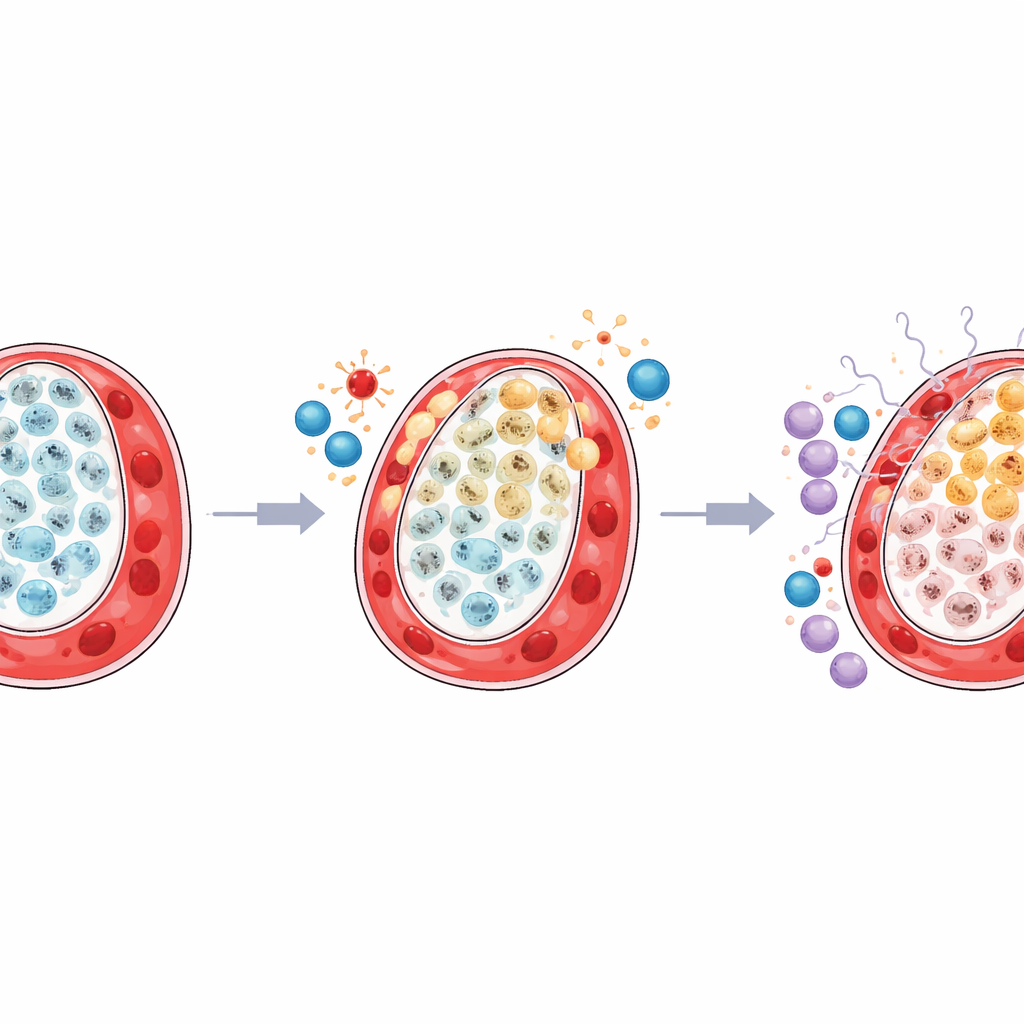
Um vizinhança inflamada ao redor das células estressadas
O estudo também identificou que o ambiente imune ao redor, no território placentário do gêmeo menor, foi remodelado de forma prejudicial. Um tipo útil de macrófago residente, conhecido como células de Hofbauer, que normalmente apoia a saúde tecidual e regula o metabolismo, estava reduzido. Ao mesmo tempo, certas células natural killer, preparadas para respostas antivirais e inflamatórias, tornaram-se mais abundantes e mais ativas. O mapeamento detalhado dos sinais trocados entre as células mostrou que os trofoblastos do tipo LDHA, sob estresse, interagiam mais fortemente com células imunes por meio de vias impulsionadas por interferon e moléculas de alarme relacionadas. Enquanto isso, a comunicação entre as células estruturais TP63 e as células estromais e vasculares de suporte enfraqueceu, sugerindo que tanto o suporte físico quanto a regulação imune calma estavam sendo perdidos.
Quebra tripla que limita o crescimento fetal
Em conjunto, o trabalho descreve de forma clara e acessível o que dá errado na placenta quando um gêmeo fica para trás. Células de suporte estrutural que mantêm a superfície de troca compacta e ordenada são exauridas, células estressadas e famintas por energia assumem o lugar, e o sistema imune desloca-se para um estado mais inflamatório. Esses três fios — perda de estrutura, sobrecarga metabólica e inflamação crônica — reforçam-se mutuamente e gradualmente comprometem a capacidade da placenta de fornecer oxigênio e nutrientes suficientes ao bebê menor. Ao identificar precisamente os tipos celulares e as vias de sinalização envolvidas, este estudo oferece um roteiro para testes e tratamentos futuros voltados a detectar problemas placentários mais cedo e, talvez, orientar essas células de volta a um equilíbrio mais saudável.
Citação: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Palavras-chave: placenta, gravidez de gêmeos, restrição do crescimento fetal, sequenciamento de RNA em célula única, células trofoblásticas