Clear Sky Science · pt
Interrupção da homeostase de neutrófilos está associada a alterações funcionais nas mitocôndrias de pacientes criticamente enfermos com COVID-19
Por que isto importa para pacientes com COVID-19
A maioria das pessoas já sabe que a COVID-19 é mais do que uma infecção pulmonar, mas a forma exata como o vírus transforma as defesas do próprio corpo ainda está sendo desvendada. Este estudo examina de perto os neutrófilos, um tipo comum de glóbulo branco, em pacientes com COVID-19 em estado crítico na unidade de terapia intensiva. Ao analisar como essas células vivem, morrem e usam suas pequenas “usinas de energia” internas (mitocôndrias), os pesquisadores revelam um padrão de neutrófilos persistentes e hiperativos que pode ajudar a explicar a inflamação contínua, lesão vascular e dano a órgãos na doença grave.
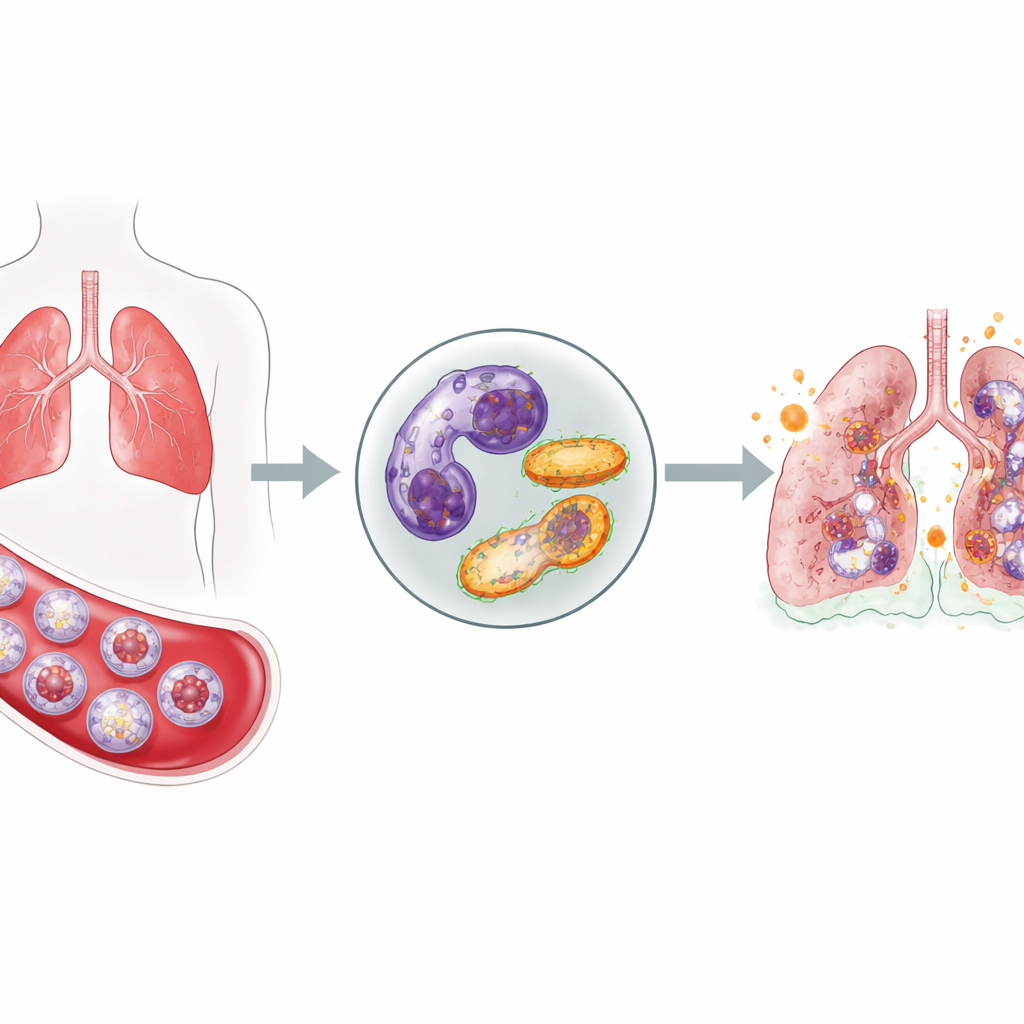
Células da linha de frente que não se retiram
Neutrófilos estão entre os primeiros a responder à infecção: eles entram na corrente sanguínea, migram para os tecidos e liberam moléculas tóxicas para matar microrganismos invasores. Normalmente, após cumprir sua função, eles se autodestruem silenciosamente e são removidos, o que evita danos ao tecido saudável. Em pacientes criticamente enfermos com COVID-19, a equipe observou um quadro muito diferente. Em comparação com voluntários saudáveis, esses pacientes apresentaram um aumento de neutrófilos no sangue e, importante, muitos eram células imaturas que haviam sido liberadas rapidamente da medula óssea. Ao mesmo tempo, vários testes mostraram que menos neutrófilos estavam passando pela morte celular programada habitual, sugerindo que essas células agressivas persistem por mais tempo do que deveriam.
Sinais genéticos sutis, mas um padrão claro de sobrevivência
Os pesquisadores também analisaram pequenas moléculas regulatórias chamadas microRNAs em neutrófilos de sobreviventes e não sobreviventes da terapia intensiva. Alguns desses microRNAs estavam alterados de maneiras que, teoricamente, apontam para vias perturbadas que controlam a morte celular e o equilíbrio de cálcio. No entanto, quando mediram marcadores diretos de morte celular, não observaram diferenças marcantes entre sobreviventes e não sobreviventes — ambos os grupos mostraram redução semelhante da autodestruição de neutrófilos em comparação com pessoas saudáveis. Isso significa que os padrões de microRNA funcionam mais como pistas para trabalhos futuros do que como indicadores firmes de quem viverá ou morrerá, e sublinha que a falha geral dos neutrófilos em se desligar é uma característica compartilhada da COVID-19 grave.
Deslocamentos de cálcio e usinas de energia sobrecarregadas
Para entender por que os neutrófilos não morriam no tempo esperado, a equipe concentrou-se em dois sistemas intimamente ligados dentro das células: sinais de cálcio e mitocôndrias. Íons de cálcio atuam como pequenos interruptores para muitas decisões celulares, incluindo quando se autodestruir. Os pesquisadores descobriram que neutrófilos de pacientes com COVID-19 grave tinham menos cálcio livre no interior, junto com níveis reduzidos de proteínas-chave que normalmente ajudam a mover cálcio para as mitocôndrias e abrem uma válvula de segurança que pode desencadear a morte celular. Ao mesmo tempo, as próprias mitocôndrias estavam incomumente “carregadas”, com um gradiente elétrico maior através de suas membranas e aumento do consumo de oxigênio, especialmente por uma via respiratória principal. Em vez de desligarem, essas mitocôndrias hiperativas produziam mais moléculas reativas de oxigênio, que podem danificar tecidos adjacentes e alimentar a inflamação.
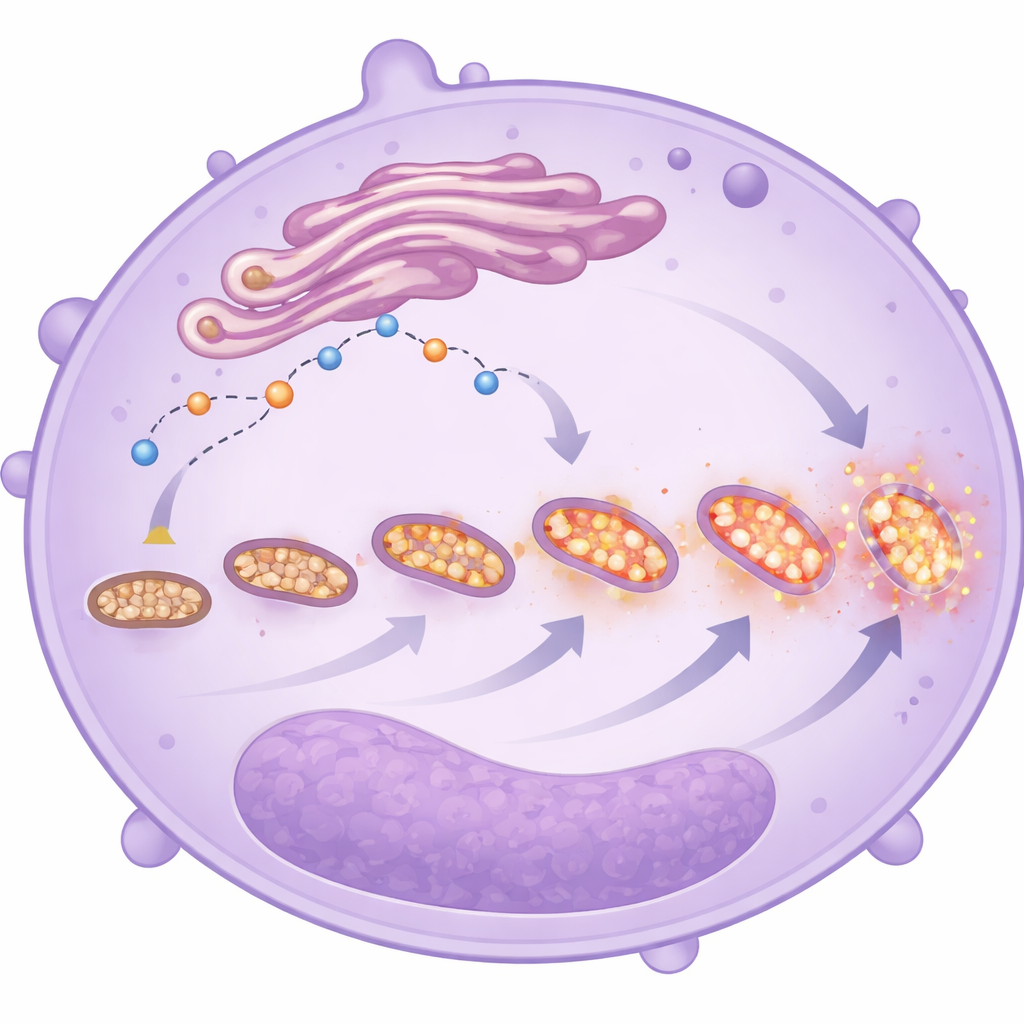
Mitocôndrias estressadas e fragmentadas
Imagens ao microscópio eletrônico e corantes fluorescentes forneceram uma visão mais próxima da forma e do comportamento dessas mitocôndrias. Em neutrófilos dos pacientes mais graves, as mitocôndrias eram mais numerosas, porém menores e mais fragmentadas — características que frequentemente indicam estresse. Essas células também mostraram níveis mais altos de espécies reativas de oxigênio mitocondriais, independentemente de o paciente ter sobrevivido ou não. Juntamente com a alteração no manuseio do cálcio e o atraso na morte celular, essas mudanças desenham um quadro de neutrófilos que mudaram sua estratégia energética: em vez de dependerem principalmente da quebra simples de açúcar, eles se apoiam mais no metabolismo mitocondrial, especialmente em células imaturas. Essa mudança pode aumentar sua capacidade de migrar, persistir e liberar moléculas danosas nos pulmões e em outros órgãos, embora o estudo não possa provar que sejam a causa direta de piores desfechos.
O que isso pode significar para cuidados futuros
Em termos práticos, o estudo sugere que, na COVID-19 crítica, os neutrófilos se tornam numerosos demais, imaturos demais e difíceis demais de desligar. Seus sinais internos de cálcio e as mitocôndrias são reprogramados de modo a mantê-los vivos e altamente ativos, produzindo rajadas de substâncias nocivas à base de oxigênio. Embora o trabalho seja observacional e não demonstre causa e efeito, ele destaca vários possíveis “botões de controle” nessas células — como reguladores do cálcio e pontos de verificação mitocondriais — que um dia poderiam ser alvo para orientar suavemente os neutrófilos de volta a um comportamento normal. Se pesquisas futuras confirmarem essas ideias, tratamentos que restaurem a adequada desligamento dos neutrófilos ou acalmem suas mitocôndrias sobrecarregadas podem ajudar a reduzir o dano colateral que essas células cruciais causam durante a COVID-19 grave e possivelmente em outras doenças críticas.
Citação: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Palavras-chave: COVID-19, neutrófilos, mitocôndrias, inflamação, doença crítica