Clear Sky Science · pt
Síntese e avaliação biológica de complexos de base de Schiff de ibuprofeno/o‑vanilina com atividades anti‑inflamatórias, antiproliferativas e anti‑SARS‑COV‑19
Por que aprimorar um analgésico familiar importa
O ibuprofeno é um dos medicamentos para dor e febre mais usados no mundo, mas o uso prolongado pode irritar o estômago e ele nunca foi projetado para combater infecções, câncer ou novos vírus. Neste estudo, químicos reengenheiraram o ibuprofeno ao ligá‑lo a uma molécula natural com aroma de baunilha e, em seguida, ao anexar diferentes metais. O resultado é uma família de novos compostos que atuam não apenas como analgésicos, mas como potenciais antibióticos, agentes anticâncer, anti‑inflamatórios e até bloqueadores de uma enzima chave do SARS‑CoV‑2, ao mesmo tempo oferecendo pistas sobre como projetar medicamentos mais inteligentes a partir de fármacos cotidianos.
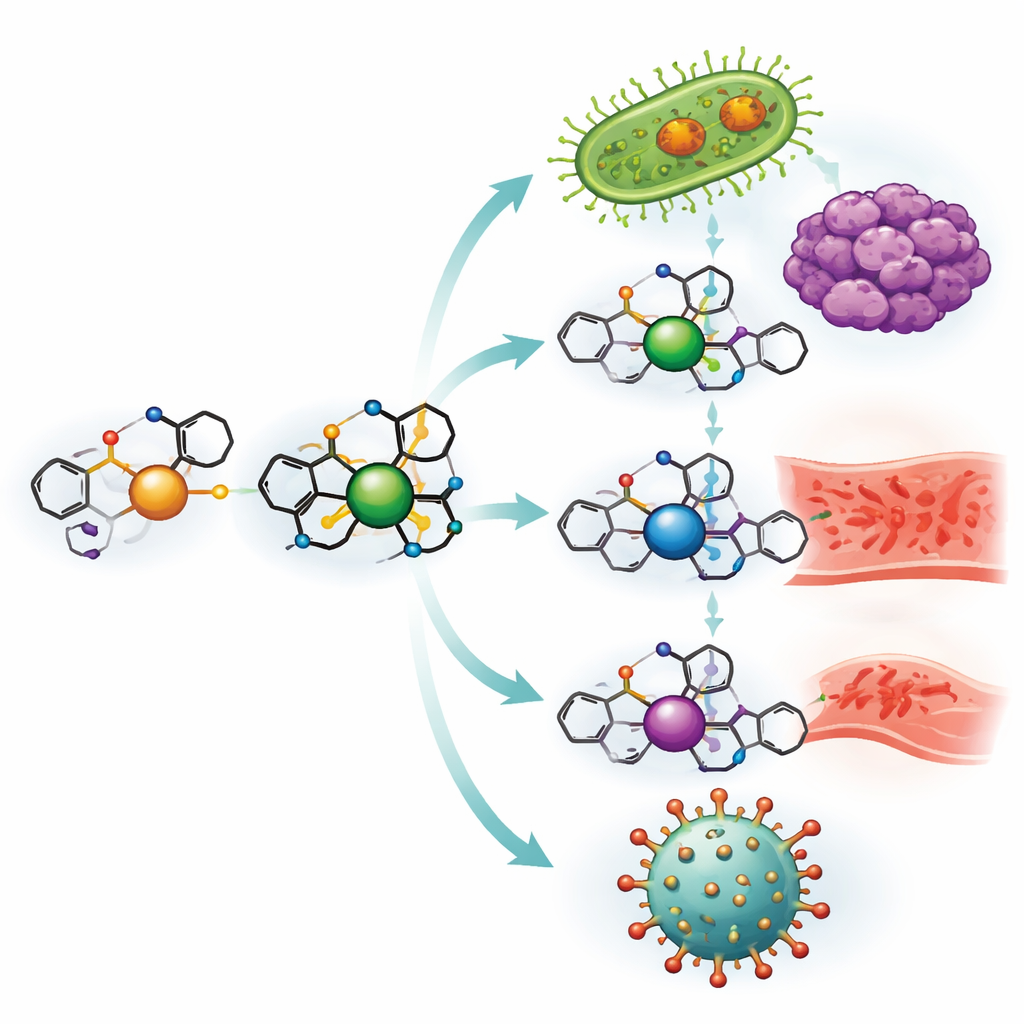
Construindo novas moléculas com aparência de fármaco a partir do ibuprofeno
A equipe começou transformando o ibuprofeno em um bloco de construção mais versátil e então ligando‑o à o‑vanilina, um parente químico próximo do composto responsável pelo sabor da baunilha. Juntos, formam um ligante do tipo “base de Schiff” — essencialmente uma garra sob medida capaz de prender íons metálicos. Esse ligante foi então combinado separadamente com sais de cobre, níquel, zinco e vanádio para produzir quatro complexos metálicos distintos. Testes laboratoriais cuidadosos, incluindo medições do comportamento de fusão, absorção de luz, propriedades magnéticas e estrutura cristalina, confirmaram como o ligante envolve cada metal e quão estáveis são os complexos resultantes, mesmo em altas temperaturas e ao longo de uma ampla faixa de acidez.
Como os complexos interagem com células e DNA
Como o efeito de um medicamento frequentemente depende de como ele encontra alvos biológicos, os pesquisadores investigaram como esses novos complexos interagem com o DNA e com células vivas. Em experimentos in vitro, o complexo de cobre em particular ligou‑se fortemente às fitas de DNA e foi capaz de danificá‑las ou “clivá‑las”, um comportamento frequentemente observado em agentes anticâncer e antibacterianos potentes. Quando testados contra linhas celulares humanas de câncer de mama, cólon e fígado, os quatro complexos foram mais tóxicos para as células cancerosas do que o próprio ligante derivado do ibuprofeno, com o complexo de cobre aproximando‑se da potência do medicamento quimioterápico vinblastina em doses semelhantes.
Combatendo germes, fungos e inflamação
Os mesmos compostos foram desafiados contra microrganismos causadores de doenças comuns, incluindo bactérias Gram‑positivas e Gram‑negativas e dois fungos problemáticos. Novamente, os complexos metálicos superaram o ligante livre, e o cobre liderou o grupo, inibindo fortemente tanto bactérias quanto fungos. Os autores interpretam isso pela teoria da “queletação”: uma vez que o metal é retido pelo ligante, sua carga fica parcialmente protegida e todo o complexo torna‑se mais lipofílico, permitindo que ele penetre nas membranas microbianas e perturbe enzimas vitais. Em um teste simples de inflamação baseado em proteína de ovo danificada pelo calor, os novos complexos também reduziram a desnaturação proteica de forma mais eficaz do que o próprio ibuprofeno, sugerindo que podem atenuar processos inflamatórios em doses menores.
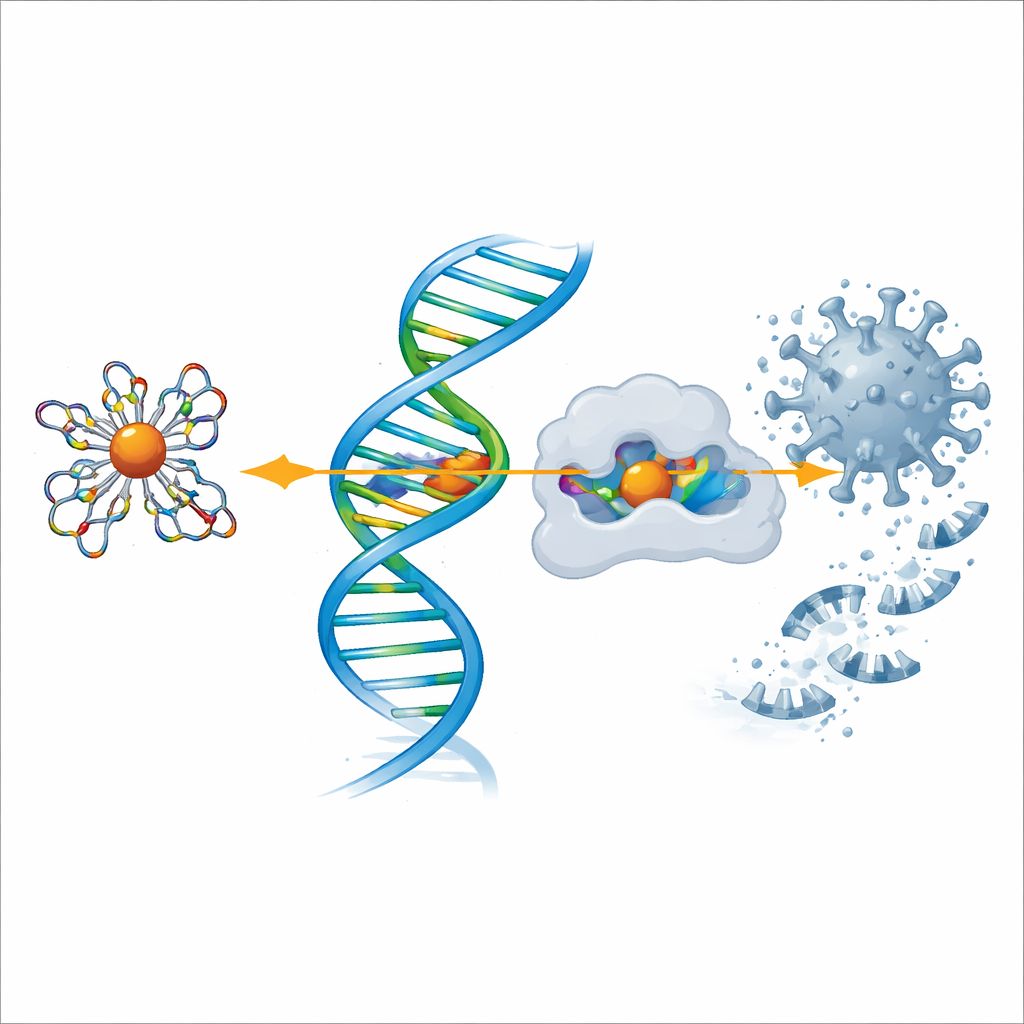
Investigações contra enzimas do COVID‑19 e da dor
Para explorar o potencial antiviral, a equipe usou modelagem computacional para encaixar o ligante e cada complexo metálico nas formas tridimensionais de duas proteínas-chave: a protease principal do SARS‑CoV‑2, que o vírus usa para clivar seus poliproteínas, e a ciclooxigenase‑2 (COX‑2), uma enzima envolvida na dor e na inflamação. As simulações mostraram que os complexos, especialmente os de cobre e zinco, se ajustaram firmemente aos bolsões ativos dessas proteínas e formaram múltiplas interações estabilizadoras. Quanto mais negativa a energia de ligação calculada, mais forte a ligação prevista, e novamente o complexo de cobre destacou‑se, seguido de perto por zinco e níquel, corroborando os achados laboratoriais sobre comportamento anti‑inflamatório e antimicrobiano.
O que isso pode significar para futuros medicamentos
Em conjunto, o trabalho mostra que um medicamento conhecido e de venda livre pode ser transformado em uma ferramenta química multifuncional ao fundi‑lo com um parceiro orgânico cuidadosamente escolhido e o íon metálico adequado. Entre os quatro metais testados, o cobre produziu o candidato mais promissor, com fortes atividades antibacteriana, antifúngica, anticâncer, anti‑inflamatória e preditas por simulação contra o SARS‑CoV‑2, enquanto níquel e zinco ofereceram efeitos ligeiramente mais moderados, mas ainda notáveis. Embora esses resultados ainda estejam em estágio de laboratório e de modelagem computacional, apontam para uma estratégia na qual medicamentos do dia a dia são “atualizados” em complexos metálicos direcionados que podem atuar em doses menores e contra uma gama mais ampla de doenças do que os fármacos originais.
Citação: Abdel-Rahman, L.H., El-ezz, D.A., Abdel-Mawgoud, AM.M. et al. Synthesis and biological evaluation of ibuprofen/o-vanillin Schiff base complexes with anti-inflammatory, anti-proliferative and anti-SARS-COV-19 activities. Sci Rep 16, 8501 (2026). https://doi.org/10.1038/s41598-026-38270-8
Palavras-chave: derivados do ibuprofeno, complexos metálicos de fármacos, agentes anticâncer, terapia antimicrobiana, protease da COVID‑19