Clear Sky Science · pt
Funcionalização assimétrica catalítica de ésteres borônicos de biciclo[1.1.0]butano viabilizada por migração 1,2 de oxigênio
Por que anéis quadrados minúsculos importam
Químicos adoram construir novos medicamentos e materiais juntando pequenas peças moleculares, como se montassem blocos de Lego. Anéis de carbono de quatro membros chamados ciclobutanos são especialmente valorizados porque concentram muita energia e forma em um espaço reduzido, o que pode alterar o comportamento de um fármaco no organismo. Este artigo descreve uma nova forma de sintetizar esses anéis com controle muito preciso, em uma configuração “de uma mão” (enantiomericamente pura), usando uma reação engenhosa que força um grupo contendo oxigênio a saltar de um átomo para outro. O trabalho abre portas para o desenho de moléculas mais complexas e precisas para aplicações farmacêuticas e materiais avançados.
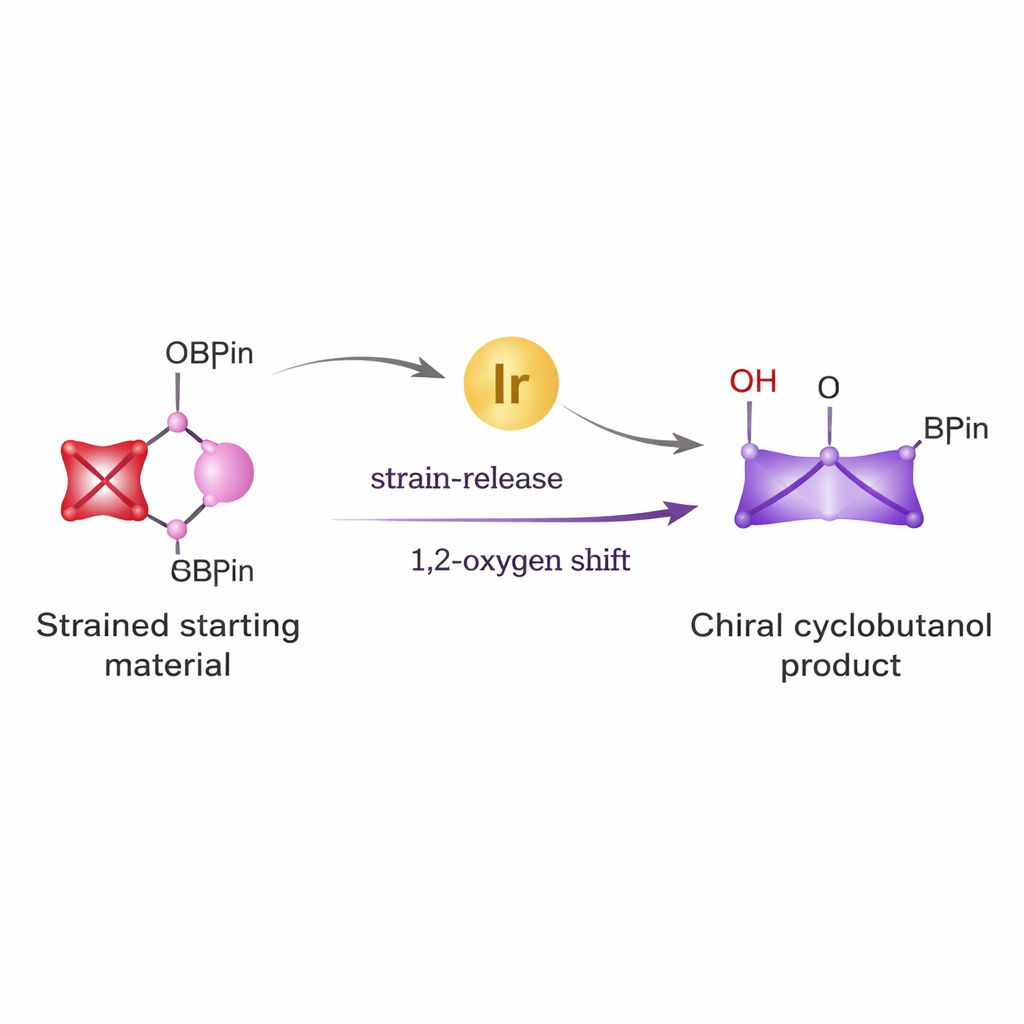
De blocos de construção simples a anéis poderosos
Ciclobutanos aparecem em diversos agentes antivirais, candidatos anticâncer e outras moléculas bioativas. Ainda assim, construí‑los com o arranjo tridimensional exato necessário para aplicações médicas tem sido difícil. Rotas tradicionais frequentemente exigem reagentes agressivos e produzem misturas de imagens especulares (enantiômeros) que são difíceis de separar. Os autores propuseram resolver esse problema combinando duas ideias poderosas: a reatividade incomum de um anel minúsculo e altamente tensionado chamado biciclo[1.1.0]butano, e a versatilidade dos ésteres borônicos, uma família bem conhecida de reagentes amplamente usada em química de acoplamento cruzado para formar ligações carbono–carbono.
Transformando uma desvantagem em nova via reacional
Em reações comuns de acoplamento catalisadas por metais, ésteres borônicos formam um complexo intermediário com um alcoóxido (uma base à base de oxigênio). Esse complexo quase sempre segue uma via consolidada chamada transmetalização, que leva diretamente à formação de novas ligações carbono–carbono ou carbono–halogênio. Essa rota “padrão” dificultou a exploração de outras possibilidades, como o deslocamento do próprio grupo oxigênio. A equipe percebeu que, se começassem a partir de um éster borônico de biciclo[1.1.0]butano, a tensão incorporada do pequeno anel poderia ser usada para sobrepor a via habitual. Ao parear esse sistema tensionado com um catalisador de irídio e um ligante quiral cuidadosamente escolhido, eles esperavam induzir a migração do oxigênio de forma controlada, enquanto o anel se abria e se recombinava em um ciclobutano.
Uma dança passo a passo guiada pela tensão
Experimentos confirmaram que essa estratégia funciona. Usando alcoóxidos de lítio preparados a partir de uma ampla variedade de álcoois — incluindo açúcares, terpenos, esteroides e álcoois alifáticos simples — os autores converteram ésteres borônicos de biciclo[1.1.0]butano em produtos cis‑ciclobutanóis com altos rendimentos e excelente controle sobre a quiralidade. O catalisador de irídio primeiro forma um complexo allyl reativo a partir de um carbonato allyl. Esse complexo então ataca o sistema tensionado do biciclo[1.1.0]butano, formando uma nova ligação carbono–carbono enquanto o anel minúsculo se abre. Crucialmente, em vez de seguir imediatamente a rota usual de transmetalização, o intermediário contendo boro sofre uma rotação sutil da ligação carbono–boro, posicionando o grupo oxigênio ligado de modo que ele possa migrar de forma limpa para um átomo de carbono vizinho. Essa migração 1,2 de oxigênio fixa a arrumação cis desejada no novo anel de ciclobutano.
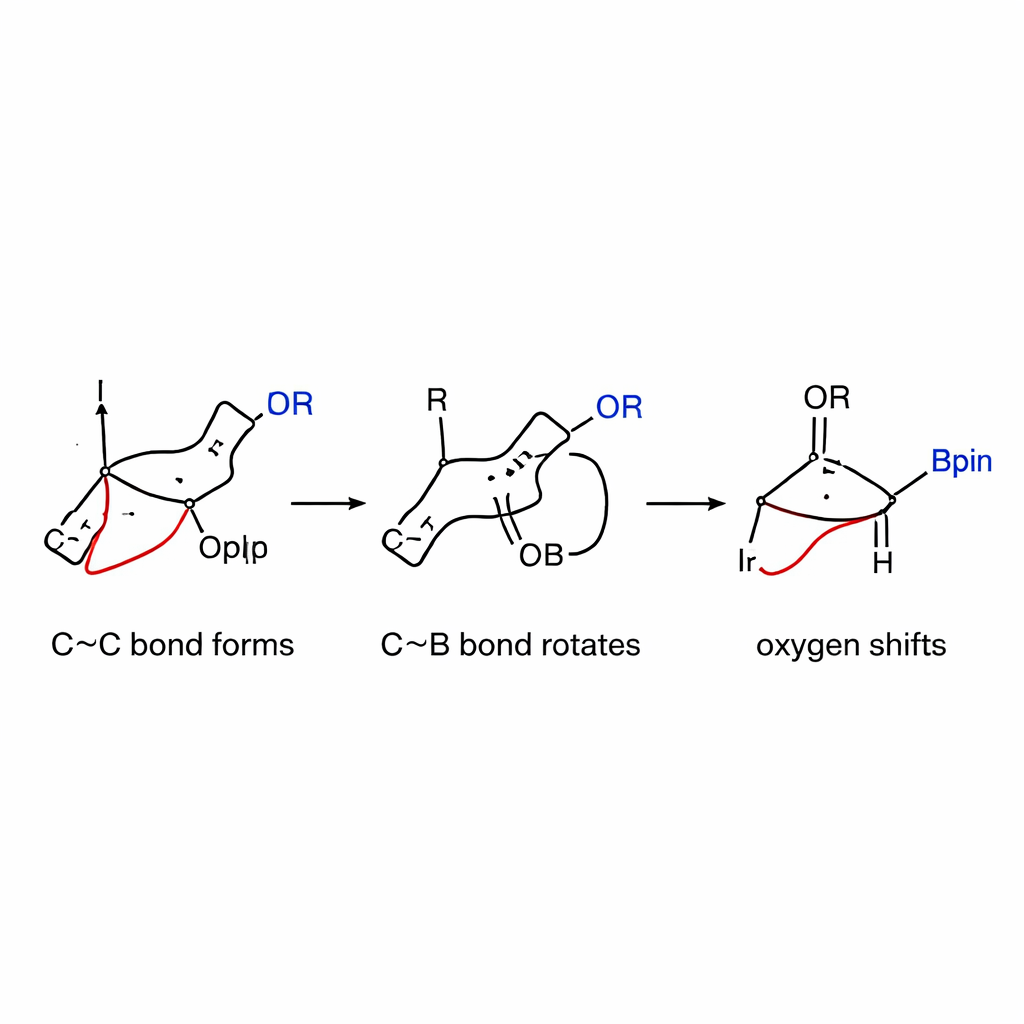
Espiando por baixo do capô do mecanismo
Para entender por que a reação é tão seletiva, os autores combinaram medições cinéticas com simulações computacionais detalhadas. Eles descobriram que o passo lento e determinante da velocidade é a formação inicial da ligação carbono–carbono entre a espécie irídio–allyl e o complexo boronato tensionado, e não a ativação anterior do carbonato allyl. Testes eletrônicos mostraram que parceiros allyl que estabilizam carga positiva reagem mais rápido, o que apoia um mecanismo em que um intermediário parcialmente carregado é formado. Cálculos adicionalmente revelaram que a rotação em torno da ligação carbono–boro — antes considerada difícil — apresenta uma barreira de energia surpreendentemente baixa nesse sistema, graças à tensão acumulada no anel. Uma vez que a rotação alinha o grupo oxigênio, o deslocamento 1,2 prossegue de forma suave e preferencial, gerando o produto cis em vez da forma trans mais comum.
Novas ferramentas para moldar futuros medicamentos
Além de provar um ponto mecanístico, a reação fornece produtos versáteis. Os ciclobutanóis retêm uma unidade de éster borônico, que pode ser transformada em muitos outros grupos funcionais usando química estabelecida. Os autores demonstraram diversas modificações em etapa tardia, como hidrogenação, oxidação, metátese de olefina e outros acoplamentos, preservando sempre a forma tridimensional precisa do anel. Em termos práticos, este trabalho transforma uma via secundária antes problemática — migração de oxigênio em complexos boronato — em uma ferramenta sintética poderosa. Ao aproveitar a tensão do anel e um catalisador de irídio finamente ajustado, os pesquisadores fornecem aos químicos um método confiável para construir ciclobutanos quirais e complexos que podem desempenhar papéis chave em medicamentos de próxima geração e materiais moleculares avançados.
Citação: Zhu, XY., Ji, CL., Dong, TG. et al. Catalytic asymmetric functionalization of bicyclo[1.1.0]butane boronic esters enabled by 1,2-oxygen migration. Nat Commun 17, 1941 (2026). https://doi.org/10.1038/s41467-026-69860-9
Palavras-chave: ciclobutano, química organoborônica, catálise assimétrica, biciclobutano, migração de oxigênio