Clear Sky Science · pt
Macrófagos CD19+ associados ao tumor induzem microambiente imunossupressor no carcinoma hepatocelular
Por que os defensores do corpo às vezes ajudam o câncer de fígado
O câncer de fígado é um dos mais letais do mundo, em parte porque os tumores podem transformar o próprio sistema imune do organismo contra si. Este estudo revela um subconjunto surpreendente de células imunes dentro de tumores hepáticos que, em vez de combater o câncer, ajudam ativamente a escondê‑lo e a promovê‑lo. Entender quem são essas células “traidoras” e como agem abre caminhos para tornar a imunoterapia mais eficaz em pessoas com carcinoma hepatocelular, a forma mais comum de câncer de fígado.
Um grupo especial de células imunes dentro dos tumores
Os autores concentraram‑se em macrófagos associados ao tumor, células imunes que normalmente engolfam germes e detritos, mas frequentemente se corrompem dentro dos cânceres. Ao analisar amostras de tumores hepáticos de muitos pacientes, descobriram um subgrupo distinto de macrófagos que expressam uma molécula de superfície chamada CD19, geralmente encontrada em células B e não em macrófagos. Esses macrófagos CD19‑positivos eram muito mais abundantes nos tumores do fígado do que no tecido hepático saudável próximo ou no sangue, e também estavam enriquecidos em vários outros cânceres sólidos. Análises de célula única confirmaram que essas células são macrófagos verdadeiros com um perfil único de genes e proteínas, e não células B mal identificadas.
Como essas células moldam um ambiente favorável ao tumor
Pacientes cujos tumores continham muitos macrófagos CD19‑positivos tendiam a ter cânceres maiores, mais agressivos e sobrevivência mais curta. Amostras tumorais ricas nessas células apresentaram menos células T CD8 capazes de matar o câncer e mais células T reguladoras, um padrão típico de um ambiente altamente imunossupressor. Em modelos murinos, adicionar macrófagos CD19‑positivos a células de câncer de fígado fez os tumores crescerem mais rápido e reduziu a presença de células T benéficas, ao mesmo tempo que aumentou outros tipos de células mieloides supressoras. Importante, quando os pesquisadores usaram células T geneticamente modificadas que reconhecem CD19 para eliminar seletivamente esses macrófagos, os tumores hepáticos encolheram mesmo em camundongos sem células B normais, identificando os próprios macrófagos como alvos terapêuticos.
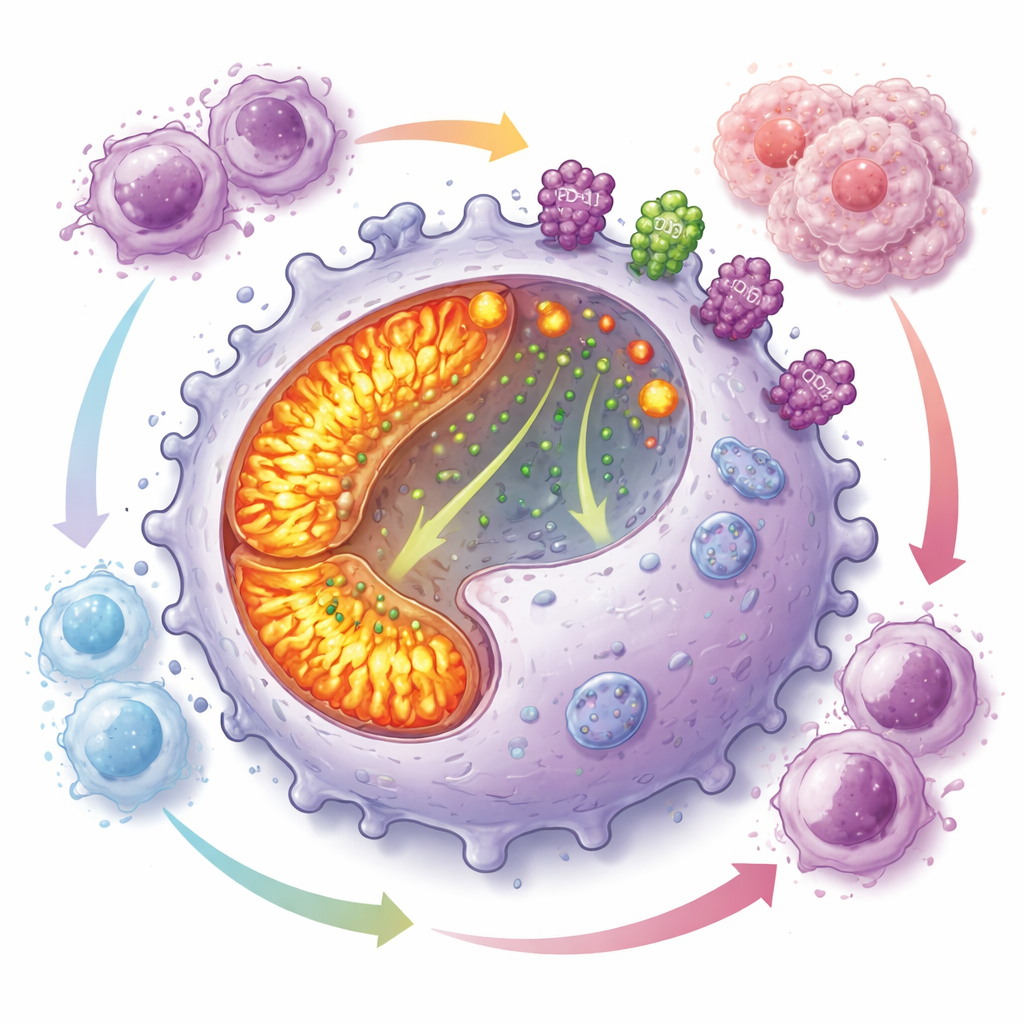
Um programa faminto por energia que neutraliza o ataque imune
Aprofundando, a equipe descobriu que os macrófagos CD19‑positivos operam suas “usinas” internas em alta potência. Suas mitocôndrias — os organelos que geram energia — eram mais numerosas e mais ativas do que nas demais células, com aumento da fosforilação oxidativa e de espécies reativas de oxigênio. Apesar desse estado energético, essas células tinham baixa capacidade de fagocitose, mas se dividiam rapidamente, o que lhes permitia acumular‑se nos tumores. Ao mesmo tempo, exibiam altos níveis de PD‑L1 e CD73 na superfície — duas moléculas conhecidas por bloquear respostas de células T e gerar adenosina, uma pequena molécula que suprime fortemente a imunidade. Experimentos de co‑cultivo mostraram que esses macrófagos inibiam fortemente a proliferação de múltiplos tipos de células T.
A chave mestra por trás dos macrófagos traidores
Os pesquisadores identificaram um fator de transcrição chamado PAX5 como o motor central desse programa deletério em macrófagos. PAX5 é mais conhecido por orientar o desenvolvimento de células B, mas aqui estava altamente ativo em macrófagos CD19‑positivos. Forçar células do tipo macrófago a expressar PAX5 aumentou a biogênese mitocondrial, elevou a produção de energia e aumentou os níveis de proteína — mas não de mRNA — de PD‑L1, CD73 e CD19. Experimentos mecanísticos mostraram que PAX5 promove a entrada de cálcio nas mitocôndrias, reduzindo o cálcio no fluido celular e impedindo que um regulador chave chamado TFEB entre no núcleo. Com o TFEB retido, a produção e a função dos lisossomos caem, de modo que proteínas como PD‑L1 e CD73 deixam de ser degradadas de forma eficiente e passam a se acumular na superfície celular, intensificando a supressão imune.
Transformando a descoberta em melhores opções de tratamento
Como esses macrófagos dependem fortemente da atividade de CD73 e do metabolismo mitocondrial, os autores testaram se bloquear essas vias poderia tornar a imunoterapia mais eficaz. Em câncer de fígado em camundongos, combinar bloqueio de PD‑L1 com anticorpos contra CD73 ou com um inibidor de CD73 levou a tumores menores, mais infiltração de células T e menor proliferação das células tumorais. De forma semelhante, associar anticorpos anti‑PD‑L1 a um inibidor da fosforilação oxidativa mitocondrial melhorou o controle tumoral e aumentou a entrada de células imunes nos tumores. De forma marcante, esses benefícios desapareceram em camundongos cujos macrófagos não expressavam PAX5, confirmando que os efeitos dos fármacos estavam ligados à desativação do programa macrofágico CD19‑positivo dirigido por PAX5. Em conjunto, o trabalho sugere que direcionar seletivamente esse subconjunto de macrófagos — por meio de terapias celulares dirigidas a CD19, inibição de CD73 ou drogas metabólicas — poderia ajudar a converter um tumor hepático imunologicamente “frio” em outro que responda muito melhor aos tratamentos atuais de bloqueio de checkpoint.
Citação: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
Palavras-chave: carcinoma hepatocelular, macrófagos associados ao tumor, imunoterapia, PD-L1 e CD73, metabolismo mitocondrial