Clear Sky Science · pt
Expressão tumoral específica de HORMAD1 perturba a parada mitótica e aumenta a sensibilidade a inibidores de quinases mitóticas
Por que isso importa para o tratamento do câncer
Quando nossas células se dividem, elas dependem de verificações de segurança intrincadas para transmitir o conjunto correto de cromossomos. O câncer frequentemente sequestra ou enfraquece essas salvaguardas, levando a genomas caóticos que tanto impulsionam a doença quanto moldam a resposta dos tumores a medicamentos. Este estudo revela como uma proteína incomum chamada HORMAD1, normalmente ativa apenas em células reprodutivas, é religada em muitos cânceres de mama agressivos e em outros tumores. Ao sabotar sutilmente um ponto de verificação chave da divisão celular, HORMAD1 torna as células cancerosas mais instáveis — mas também incomumente vulneráveis a uma nova classe de medicamentos experimentais.
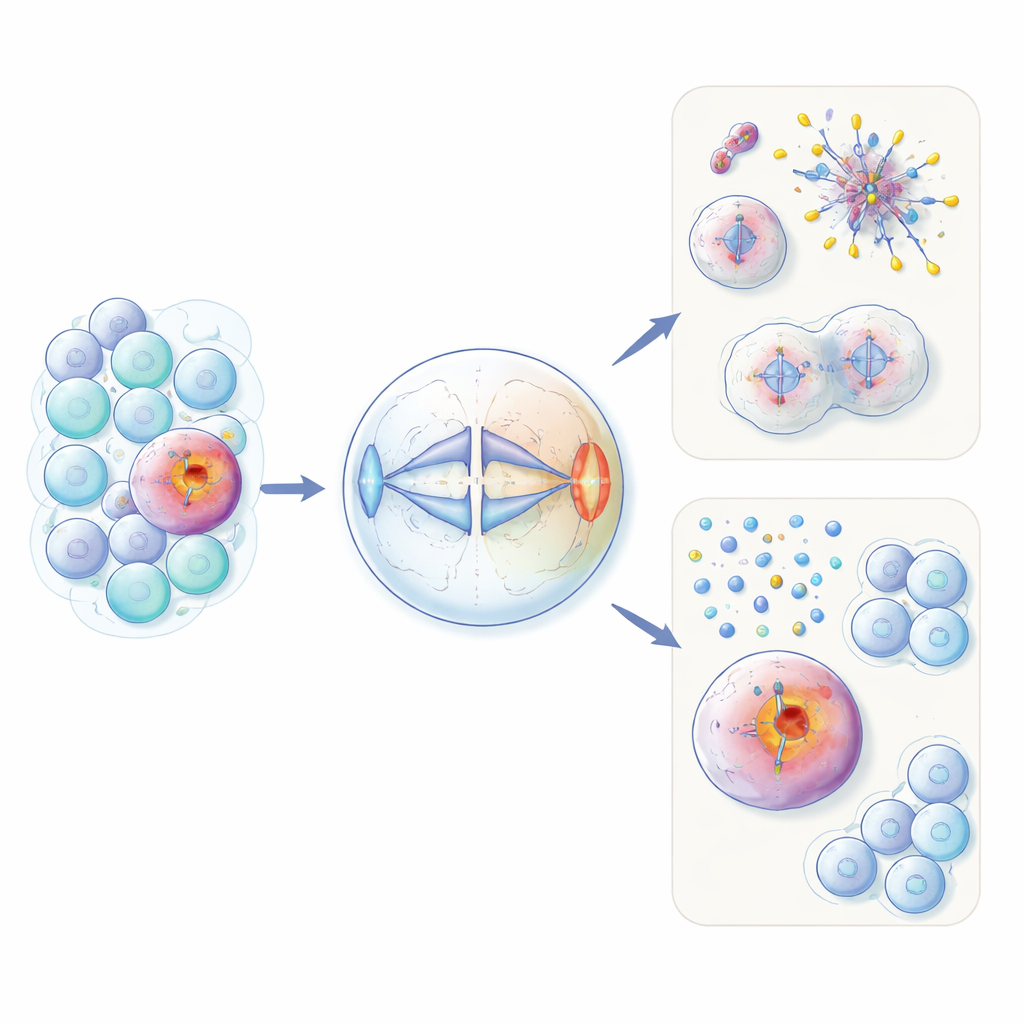
Uma proteína da fertilidade fora do lugar em células cancerosas
HORMAD1 costuma aparecer apenas em células germinativas, onde os óvulos e os espermatozoides são formados. Lá, ela ajuda a gerenciar a reorganização do DNA e o controle de qualidade durante o tipo especial de divisão celular chamado meiose. Os autores mostram que em cerca de 60% dos cânceres de mama triplo-negativos — e em subgrupos de vários outros tipos tumorais — essa proteína é reativada inapropriadamente. Usando tanto células não cancerosas geneticamente modificadas quanto linhagens de células tumorais, eles descobriram que HORMAD1 extra perturba a separação uniforme dos cromossomos durante a divisão celular ordinária. Células que expressam HORMAD1 desenvolveram mais cromossomos retardados, cromossomos extras ou ausentes (aneuploidia) e pequenas “micronúcleos” contendo DNA, todos sinais de caos genômico observados em cânceres agressivos.
Como as verificações de segurança da divisão celular funcionam normalmente
Para dividir-se corretamente, a célula constrói um fuso de microtúbulos que se prende a cada cromossomo. Um sistema de vigilância conhecido como ponto de verificação do alinhamento do fuso funciona como um freio sensível à tensão: se algum cromossomo não estiver adequadamente anexado, o freio bloqueia a progressão, impedindo a separação até que os erros sejam corrigidos. Diversas enzimas chamadas quinases mitóticas, incluindo MPS1, Aurora B e BUB1, ajudam a detectar conexões ruins e promovem a “correção de erros” para que cada célula filha receba o conjunto correto de cromossomos. A perturbação desse sistema pode tanto alimentar o desenvolvimento do câncer quanto criar fraquezas específicas que certos medicamentos podem explorar.
HORMAD1 enfraquece discretamente o freio
Os pesquisadores descobriram que HORMAD1 mina esse freio de segurança de maneira sutil, porém importante. Em vez de interferir com componentes clássicos do ponto de verificação como a proteína HORMA MAD2L1, HORMAD1 liga-se diretamente à quinase Aurora B. Aurora B normalmente faz parceria com outra proteína, INCENP, para tornar-se totalmente ativa e modificar proteínas em centrômeros e cinetócoros — locais críticos nos cromossomos onde as fibras do fuso se anexam. Quando HORMAD1 está presente em células tumorais em divisão, ela compete com INCENP pelo acesso à Aurora B, reduzindo essa parceria e atenuando a atividade de Aurora B. Como resultado, os sinais habituais de fosforilação promovidos por Aurora B em vários alvos ficam enfraquecidos, a correção de erros é menos eficaz e o ponto de verificação torna-se “permeável”: as células saem da mitose cedo demais, mesmo quando as conexões estão defeituosas, levando a segregação incorreta dos cromossomos e à instabilidade genômica.
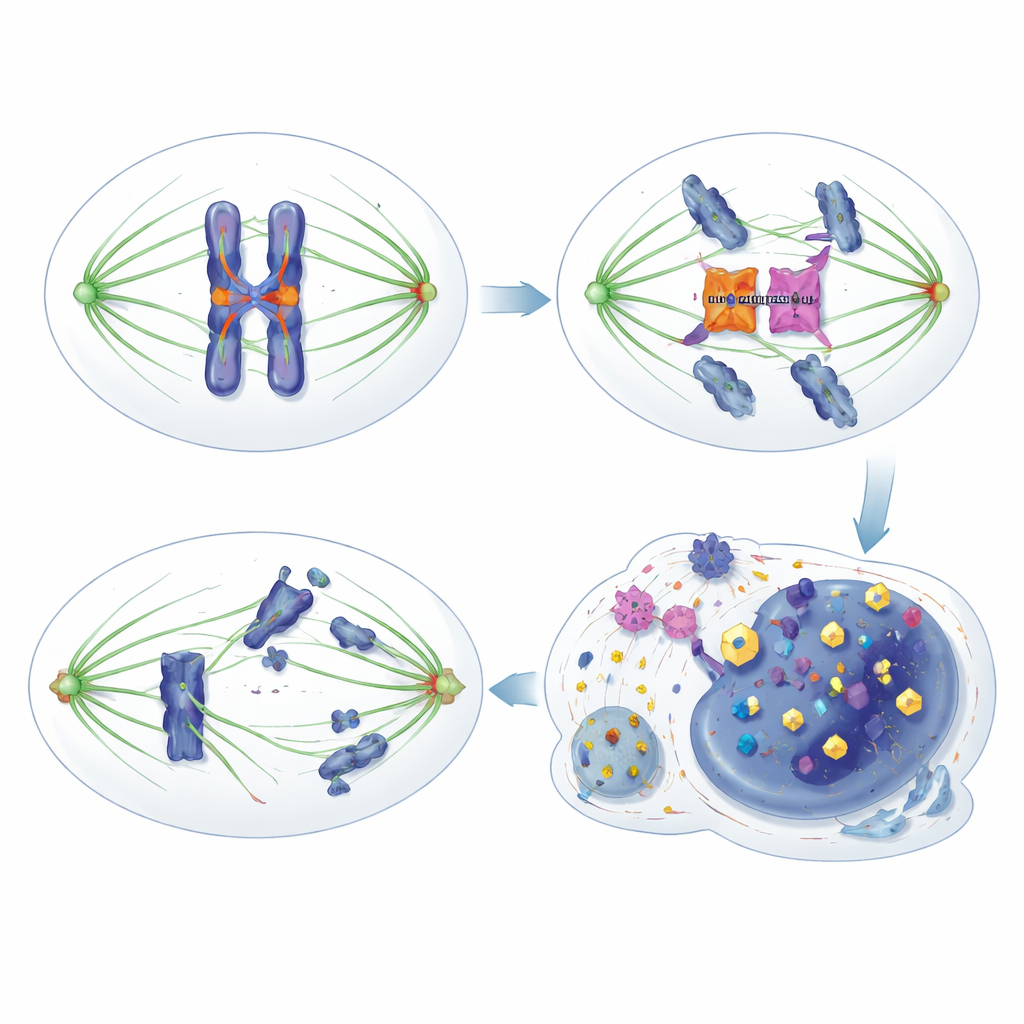
Da fraqueza à oportunidade terapêutica
Porque HORMAD1 desabilita apenas parcialmente Aurora B e as salvaguardas relacionadas, as células cancerosas permanecem apenas suficientemente viáveis para crescer, mas dependem fortemente da função remanescente das quinases mitóticas para sobreviver a divisões defeituosas repetidas. A equipe testou isso expondo células positivas e negativas para HORMAD1 a inibidores experimentais de MPS1, Aurora B e BUB1. Em múltiplos modelos, a expressão de HORMAD1 tornou as células muito mais sensíveis a esses fármacos, reduzindo dramaticamente sua capacidade de proliferar ou formar colônias. A depleção genética de BUB1 foi especialmente letal apenas na presença de HORMAD1, revelando uma dependência seletiva e forte. Em modelos de camundongos utilizando tumores de mama triplo-negativos derivados de pacientes, aqueles com níveis altos de HORMAD1 encolheram ou cresceram mais lentamente quando tratados com uma formulação nanoparticulada de um inibidor de Aurora B, enquanto tumores negativos para HORMAD1 resistiram amplamente ao mesmo tratamento.
O que isso significa para os pacientes
Para um observador leigo, HORMAD1 age como uma espada de dois gumes no câncer: ela empurra as células tumorais em direção a uma desordem cromossômica maior, o que pode impulsionar a doença, mas ao fazê-lo também as torna perigosamente dependentes de algumas salvaguardas remanescentes da divisão celular. O estudo mostra que essa proteína da fertilidade deslocada enfraquece um ponto de verificação chave ao redirecionar Aurora B, deixando tumores positivos para HORMAD1 particularmente vulneráveis a fármacos que têm como alvo Aurora B, MPS1 ou BUB1. Como HORMAD1 está amplamente ausente nos tecidos normais, mas presente em um subconjunto claro de cânceres, ela pode servir como um biomarcador para identificar pacientes com maior probabilidade de se beneficiar desses inibidores mitóticos emergentes, abrindo potencialmente novas vias de tratamento direcionado para cânceres de difícil tratamento, como o câncer de mama triplo-negativo.
Citação: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
Palavras-chave: HORMAD1, câncer de mama triplo-negativo, instabilidade cromossômica, quinase Aurora B, inibidores do ponto de verificação mitótico