Clear Sky Science · pt
Polímeros proteomiméticos heterobifuncionais para degradação direcionada de MYC e KRAS
Novas ferramentas para derrubar as proteínas mais difíceis do câncer
Muitas das proteínas que mais impulsionam o câncer, como MYC e KRAS, foram rotuladas por muito tempo como “indrogáveis” porque medicamentos não conseguem se prender facilmente a elas. Este estudo revela um novo tipo de material sintético e macio — chamados polímeros HYDRAC — que podem agarrar essas proteínas escorregadias e direcioná‑las ao sistema de descarte da célula. Para os leitores, o trabalho oferece um vislumbre de como a química e a nanotecnologia podem abrir opções de tratamento para cânceres que resistiram às drogas tradicionais.
Uma plataforma flexível em vez de uma única pílula
A maioria dos medicamentos anticâncer direcionados são pequenas moléculas que se encaixam em cavidades na superfície de uma proteína, como uma chave na fechadura. Mas proteínas como MYC são flexíveis e carecem de cavidades bem definidas, enquanto KRAS frequentemente sofre mutações que vencem os fármacos clássicos. Os autores desenharam, em vez disso, polímeros longos em forma de corrente, construídos a partir de unidades repetitivas. Ao longo dessas cadeias eles acoplaram dois tipos de componentes: segmentos curtos que se ligam à proteína e reconhecem um alvo como MYC ou RAS, e segmentos “degron” que recrutam a maquinaria de eliminação da própria célula. Como muitas cópias de cada componente decoram a mesma cadeia, uma única molécula HYDRAC pode alcançar múltiplas proteínas e enzimas ao mesmo tempo — algo difícil de conseguir com uma molécula de fármaco única e rígida.
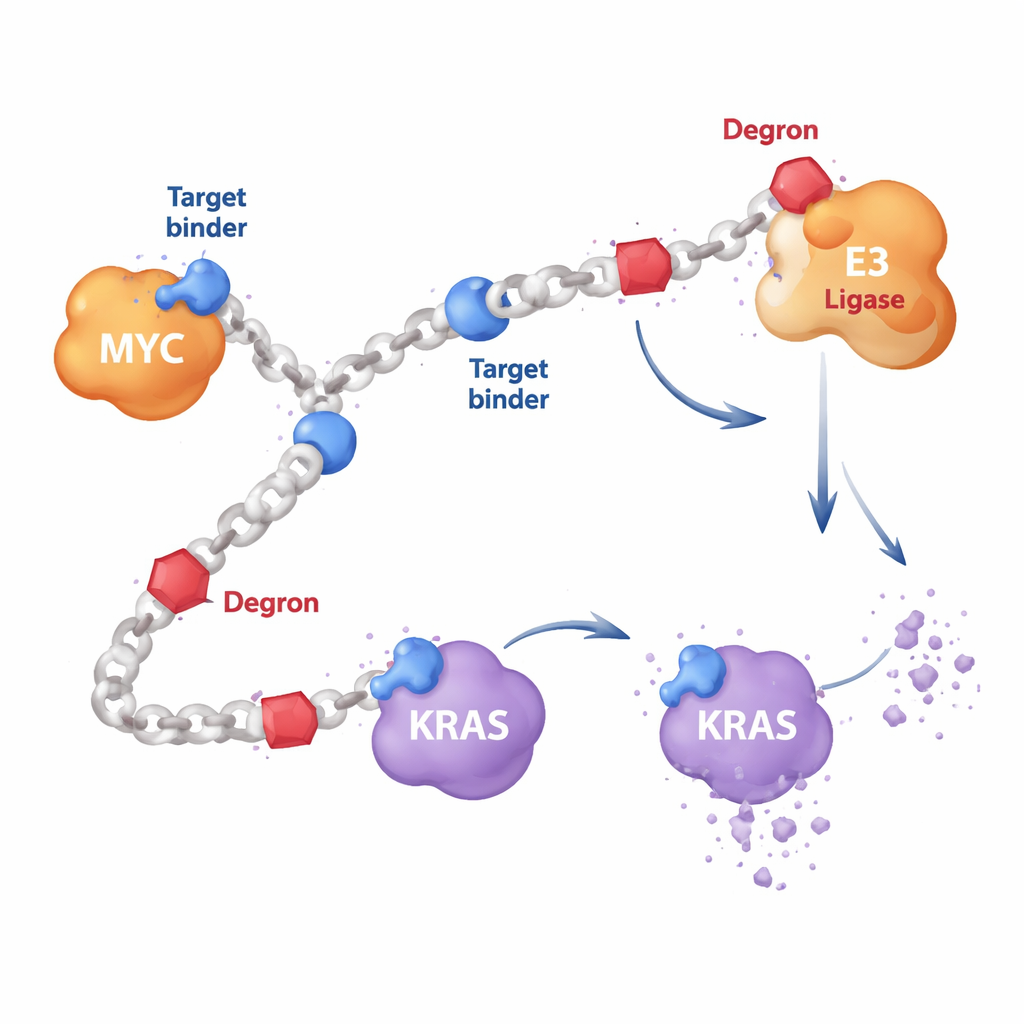
Ensinando as células a degradar MYC
Como primeiro teste, os pesquisadores focaram em MYC, um interruptor mestre que impulsiona o crescimento em muitos cânceres, mas que resistiu a ataques diretos por décadas. Eles construíram polímeros HYDRAC exibindo um peptídeo conhecido por se ligar a MYC ao lado de um motivo degron simples que marca proteínas para destruição pelo proteassoma da célula, seu principal triturador de proteínas. Em experimentos de proveta, esses polímeros dobraram‑se em formas compactas semelhantes a proteínas e ligaram‑se fortemente ao MYC, mas não a proteínas não relacionadas. Em células cancerosas, os HYDRACs entraram com facilidade, desorganizaram programas gênicos controlados por MYC e desencadearam morte celular — efeitos que dependiam de os componentes de direcionamento e degron estarem presentes na mesma cadeia polimérica.
Da cultura celular ao encolhimento de tumores
Dentro das células, o tratamento com HYDRAC fez os níveis de proteína MYC cair acentuadamente sem reduzir o RNA de MYC, indicando destruição real em vez de simples inibição da expressão. Bloquear o proteassoma ou enzimas chave que ativam certas vias de degradação salvou os níveis de MYC, mostrando que os polímeros atuam redirecionando os próprios sistemas de eliminação celular. Análises proteômicas em larga escala revelaram que muito poucas outras proteínas foram afetadas, sugerindo seletividade notável. Em modelos de camundongos com tumores impulsionados por MYC, HYDRACs marcados com fluoróforo se acumularam preferencialmente nos tumores após injeção e ali permaneceram por dias. Doses repetidas desaceleraram o crescimento tumoral sem perda de peso significativa ou danos teciduais evidentes, e amostras tumorais mostraram menos células em divisão e mais sinais de morte celular programada.
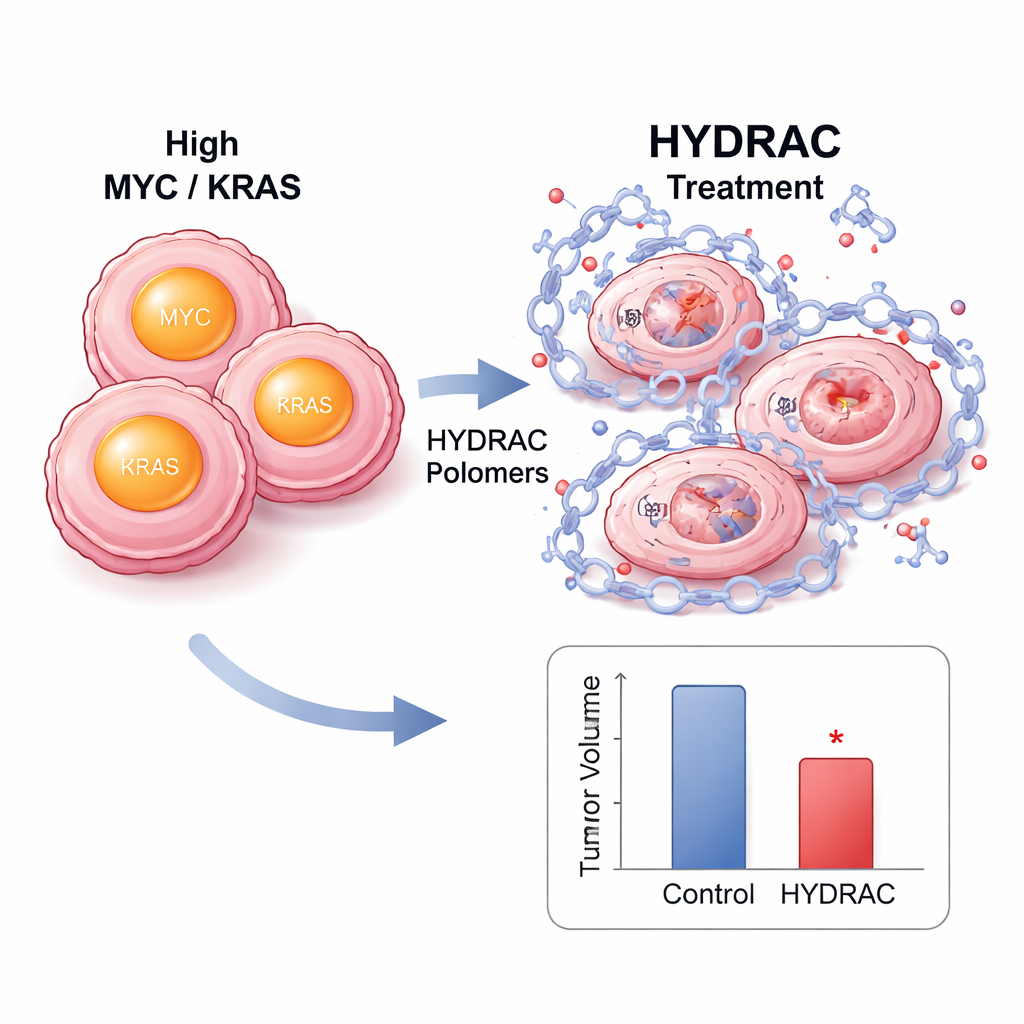
Uma plataforma plug-and-play para muitos alvos de doença
Uma força da abordagem HYDRAC é que seus grupos laterais podem ser trocados como peças intercambiáveis. A equipe substituiu o degron original por outros elementos recrutadores que ativam diferentes enzimas celulares, incluindo aquelas que reconhecem a droga talidomida. Cada versão degradou MYC apenas quando a enzima pretendida estava presente e funcional, confirmando que os polímeros podem ser ajustados para usar rotas celulares distintas. Para testar a generalidade, os pesquisadores então construíram HYDRACs direcionados a RAS usando um peptídeo que reconhece proteínas RAS. Esses constructos degradaram com sucesso o KRAS mutante em duas diferentes linhagens celulares cancerosas, sugerindo um potencial “pan‑KRAS” que não depende de uma mutação específica — um passo importante para cânceres nos quais coexistem muitas variantes de KRAS.
Por que isso importa para o futuro do cuidado do câncer
Este trabalho introduz os HYDRACs como uma nova classe de materiais programáveis que não apenas bloqueiam proteínas problemáticas — eles ajudam as células a apagá‑las. Ao combinar muitas unidades de direcionamento e degradação em um polímero flexível, os HYDRACs contornam os limites de projeto de fármacos tradicionais de pequena molécula e dos PROTACs, que tipicamente só carregam uma unidade de cada. Embora ainda falte muito antes que esses materiais cheguem à clínica, os resultados em modelos impulsionados por MYC e KRAS sugerem que proteínas do câncer consideradas por muito tempo “indrogáveis” podem, de fato, ser vulneráveis quando a medicina se parece mais com uma escova molecular sob medida do que com uma única pílula pequena.
Citação: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
Palavras-chave: degradação proteica direcionada, MYC, KRAS, terapêutica com polímeros, nanomedicina contra o câncer