Clear Sky Science · pt
Paisagem epigenômica integrativa dos cérebros com doença de Alzheimer revela perturbações moleculares em oligodendrócitos associadas à tau
Por que esta pesquisa cerebral importa
A doença de Alzheimer é mais conhecida pela perda de memória e pelo acúmulo de duas proteínas problemáticas no cérebro: amiloide e tau. Ainda assim, pessoas com Alzheimer podem apresentar padrões de dano muito distintos, mesmo dividindo o mesmo diagnóstico. Este estudo investiga uma questão central: quais interruptores dentro das células cerebrais ajudam a determinar quanto dessas proteínas nocivas se acumulam e como elas afetam diferentes tipos celulares? Ao analisar marcas químicas no DNA de centenas de cérebros, os pesquisadores revelam uma ligação surpreendente entre a tau e as células responsáveis pelo funcionamento da “fiação” cerebral.
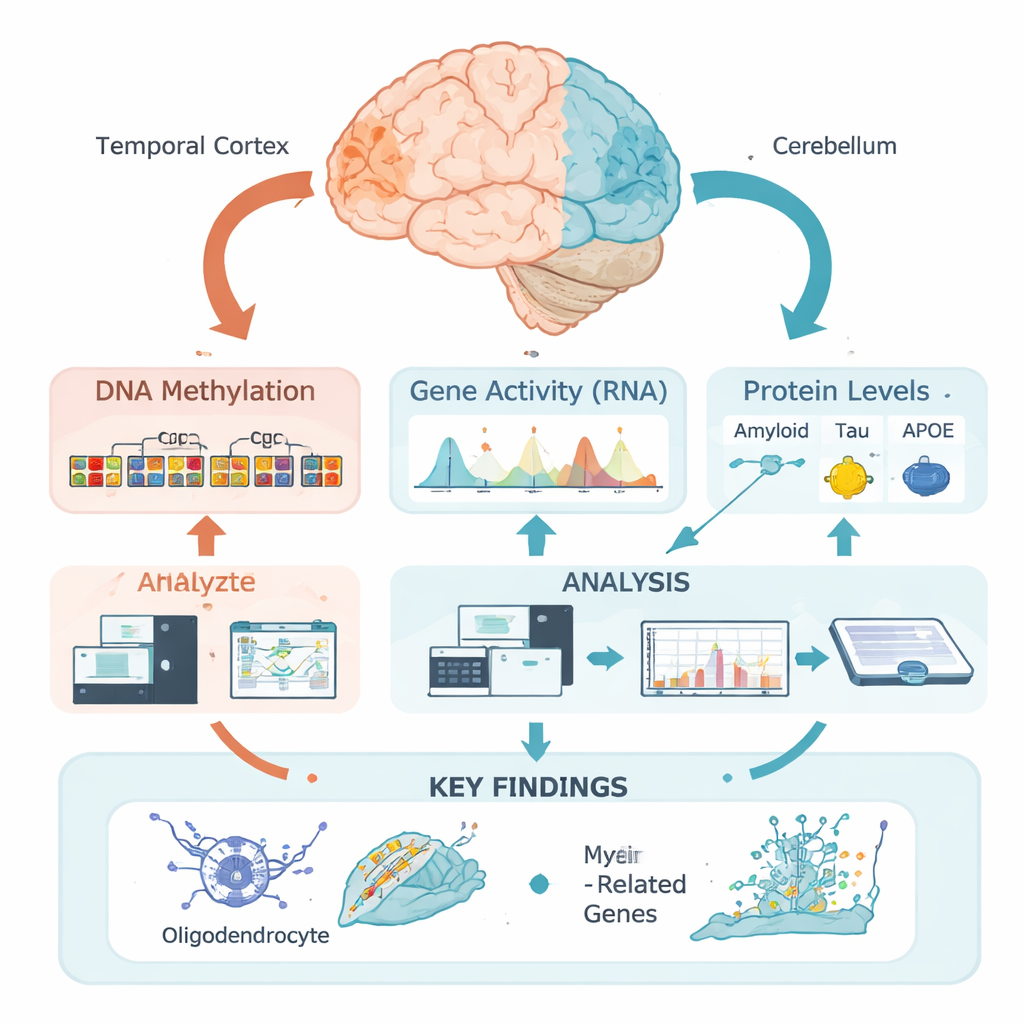
Marcas químicas no DNA como interruptores ocultos
Nosso DNA carrega as instruções básicas para construir e manter as células cerebrais, mas essas instruções são reguladas por marcas epigenéticas—grupos químicos que podem aumentar ou diminuir a atividade de genes próximos sem alterar o código genético. Uma das marcas mais importantes é a metilação do DNA, em que pequenos grupos químicos se ligam a locais específicos do DNA. Em vez de examinar sítios isolados, esta equipe usou uma abordagem “regional”: agrupou muitos sítios próximos em zonas funcionais com base em como o DNA está empacotado no córtex temporal, uma região fortemente afetada no Alzheimer, e no cerebelo, que é relativamente poupado. Isso permitiu perguntar onde, em sentido biológico, os padrões de metilação mudam em relação às características da doença.
Conectando marcas do DNA às proteínas do Alzheimer
Os pesquisadores analisaram tecido cerebral de 472 pessoas com Alzheimer confirmado post-mortem. Para cada amostra do córtex temporal, mediram níveis detalhados de amiloide, tau e proteínas APOE em diferentes formas bioquímicas, assim como escores microscópicos clássicos de placas amiloides e emaranhados de tau. Em seguida realizaram estudos de associação epigenômica ampla, testando se os níveis regionais de metilação do DNA se correlacionavam com essas medições. De forma marcante, quase todas as associações fortes que encontraram estavam ligadas não à amiloide, mas à tau—especialmente à tau solúvel total e a uma forma fosforilada ligada à membrana, considerada particularmente tóxica.
Um sinal forte nas células da fiação cerebral
Muitas das regiões de DNA associadas à tau situavam-se em partes “ativas” do genoma que influenciam genes próximos. Ao combinar dados de metilação com medições de atividade gênica dos mesmos cérebros, a equipe mostrou que essas regiões frequentemente controlavam genes usados por oligodendrócitos—células que envolvem fibras nervosas com mielina isolante, permitindo que sinais elétricos viajem rápida e confiavelmente. Genes essenciais relacionados à mielina, como MBP, MAG e MYRF, juntamente com o gene de risco para Alzheimer BIN1 e um gene candidato mais recente chamado LDB3, apareceram nesse conjunto. Níveis mais altos de tau fosforilada tóxica tendiam a coincidir com maior metilação nessas regiões e menor expressão dos genes associados a oligodendrócitos e mielina, enquanto o conjunto mais benigno de tau total solúvel mostrava o padrão oposto.
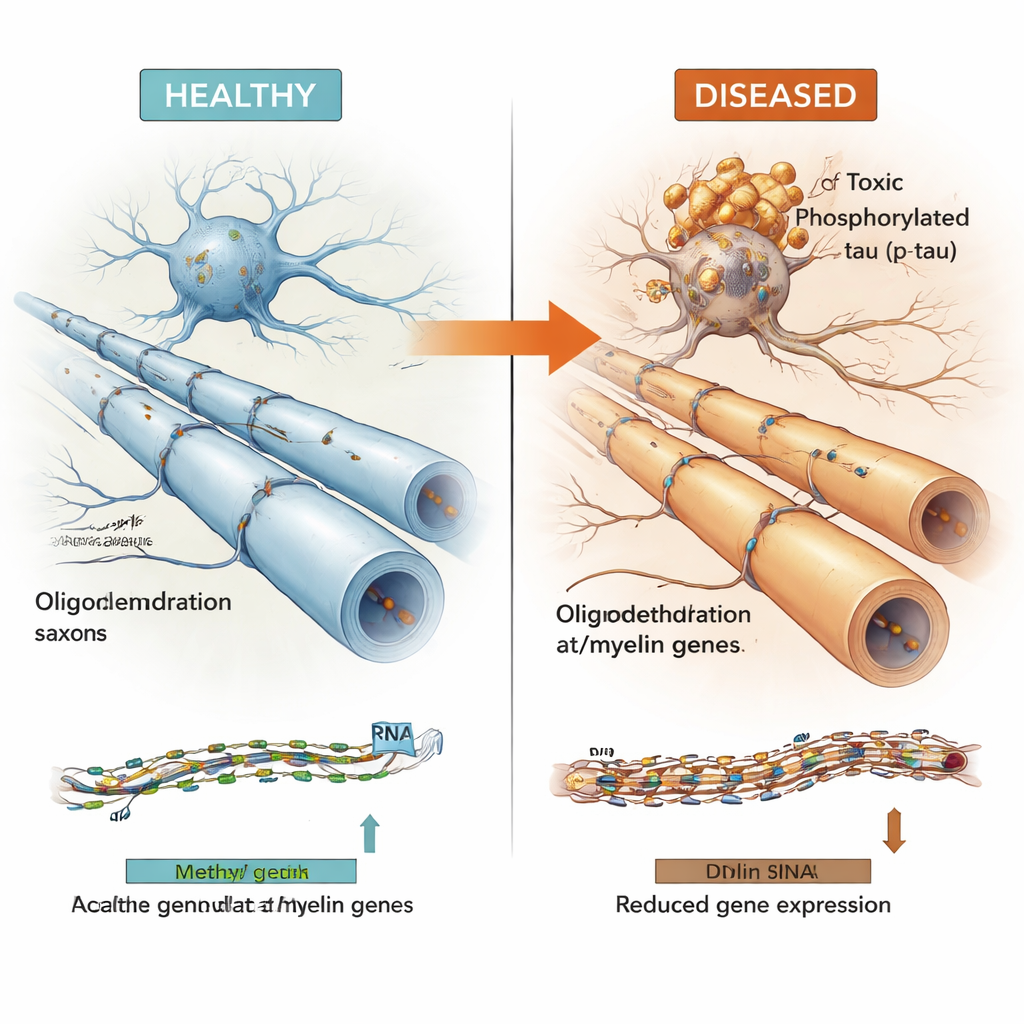
Um padrão observado em várias doenças cerebrais
Para testar se essas descobertas eram robustas e gerais, os autores examinaram grandes conjuntos de dados independentes de outras coleções de cérebros com Alzheimer e de cérebros afetados por tauopatias primárias, como paralisia supranuclear progressiva e doença de Pick. Mesmo que essas coortes fossem medidas com tecnologias diferentes e muitas vezes em regiões cerebrais distintas, muitas das mesmas regiões de DNA e genes de oligodendrócitos exibiram comportamento consistente: seus níveis de metilação se relacionavam com a carga de emaranhados de tau, e sua expressão estava reduzida em cérebros doentes e em estudos de célula única focados especificamente em oligodendrócitos. Importante, esses padrões não parecem ser explicados simplesmente pela genética ou pela perda geral de células, sugerindo uma mudança epigenética genuína no funcionamento dos oligodendrócitos.
O que isso significa para a compreensão do Alzheimer
Em conjunto, os resultados sustentam um modelo no qual o aumento de níveis de tau nociva está fortemente ligado a mudanças epigenéticas em oligodendrócitos que suprimem genes relacionados à mielina, potencialmente enfraquecendo a fiação cerebral e contribuindo para o declínio cognitivo. Ainda não está claro o que vem primeiro—acúmulo de tau ou a perturbação desses genes de mielina—mas as associações recorrentes e robustas observadas em milhares de amostras e em várias doenças apontam para um mecanismo compartilhado. Ao mapear esses interruptores no DNA e integrá-los em um “Atlas Multiômico” público, este trabalho destaca os oligodendrócitos e sua regulação epigenética como alvos promissores para terapias futuras voltadas a estabilizar circuitos cerebrais, em vez de focar exclusivamente em neurônios ou placas de amiloide.
Citação: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
Palavras-chave: Doença de Alzheimer, proteína tau, metilação do DNA, oligodendrócitos, mielina