Clear Sky Science · pt
Base estrutural do sinalizador humano ativado por zinco (ZAC) e sua modulação
Como um Metal Traço Ajuda Células Nervosas a Conversar
O zinco é mais conhecido como nutriente em comprimidos multivitamínicos, mas no interior do corpo esse metal também atua como um mensageiro químico rápido no cérebro. O estudo descrito aqui revela, em resolução atômica, como uma proteína pouco conhecida chamada canal ativado por zinco (ZAC) detecta zinco fora das células e converte esse sinal em uma resposta elétrica. Entender esse portão especial na membrana celular pode esclarecer como o zinco molda a atividade cerebral e sugerir novas maneiras de ajustar sinais nervosos na saúde e na doença.
Um Portão Especial para Sinais de Zinco
Muitas mensagens rápidas entre células nervosas são transmitidas por químicos familiares como serotonina ou acetilcolina, que abrem canais em forma de anel na membrana celular. O ZAC é um parente distante desses receptores, mas em vez de responder a uma molécula orgânica, é ativado por íons metálicos como zinco, cobre e prótons. O ZAC está presente em vários tecidos humanos, incluindo o cérebro, mas está ausente em animais de laboratório comuns como camundongos e ratos, o que atrasou o progresso. Este trabalho usa microscopia crioeletrônica de alta resolução para capturar várias imagens tridimensionais do ZAC humano: em sua forma de repouso, com zinco ligado e com dois fármacos diferentes que inativam o canal. Juntas, essas estruturas revelam como o zinco se encaixa no topo do canal, como os íons passam e como os bloqueadores prendem o portão fechado ou o escancaram em um estado não condutor.
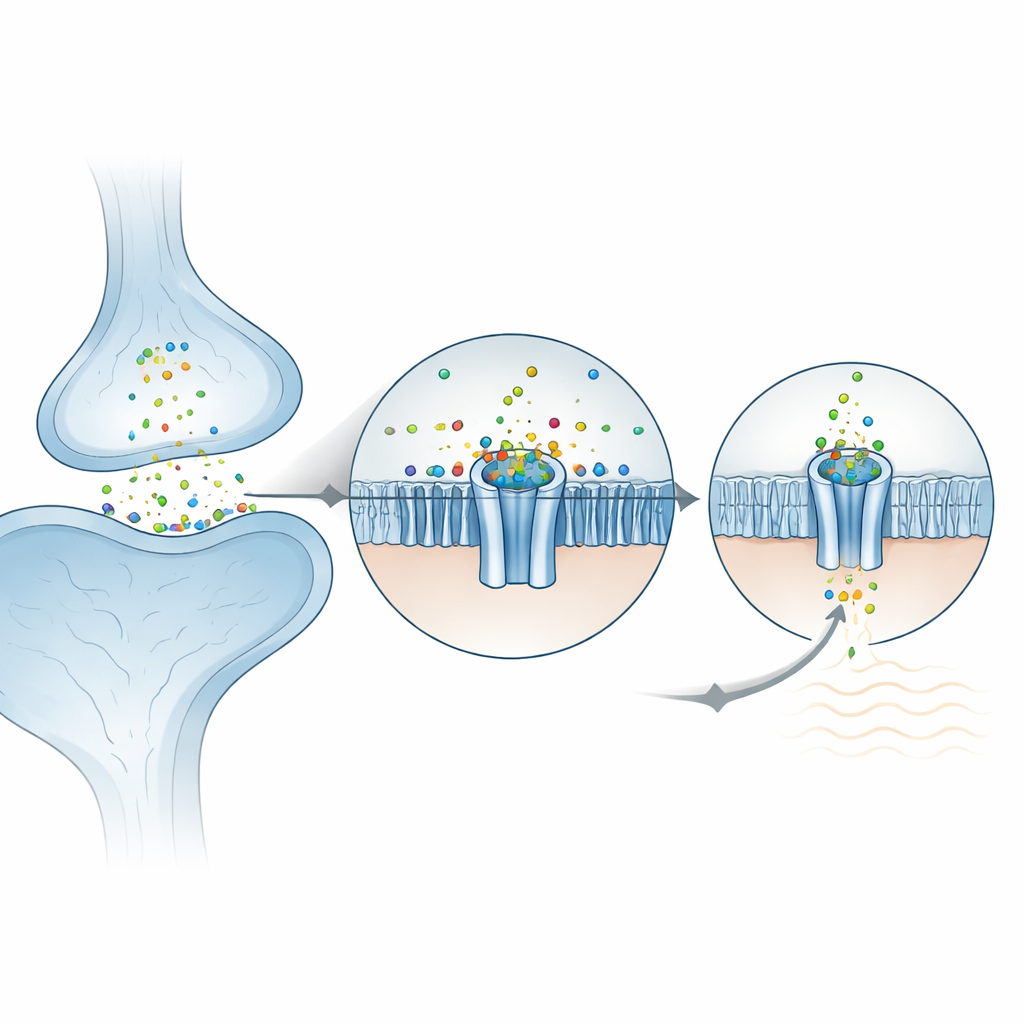
Como o Zinco Se Encaixa no Canal
Na superfície externa da célula, o ZAC é composto por cinco subunidades idênticas que formam uma roseta. Os pesquisadores descobriram que íons de zinco se acomodam em cinco bolsos equivalentes, cada um situado entre duas subunidades vizinhas no domínio externo. Surpreendentemente, o zinco não é segurado pelos aminoácidos “agarra‑metais” habituais que normalmente se ligam a metais (como histidina ou cisteína). Em vez disso, é acolhido principalmente por duas cadeias laterais aromáticas em forma de anel que estabilizam o íon positivamente carregado por meio das chamadas interações cátion–π. Quando esses resíduos-chave foram mutados em ovos de rã usados para gravações elétricas, o canal deixou de responder ao zinco, confirmando seu papel central. O ambiente ao redor já está pré‑organizado, o que ajuda a explicar por que o ZAC mostra atividade espontânea notável mesmo sem zinco: a proteína fica perto do ponto de transição entre fechado e aberto e o zinco simplesmente inclina o equilíbrio.
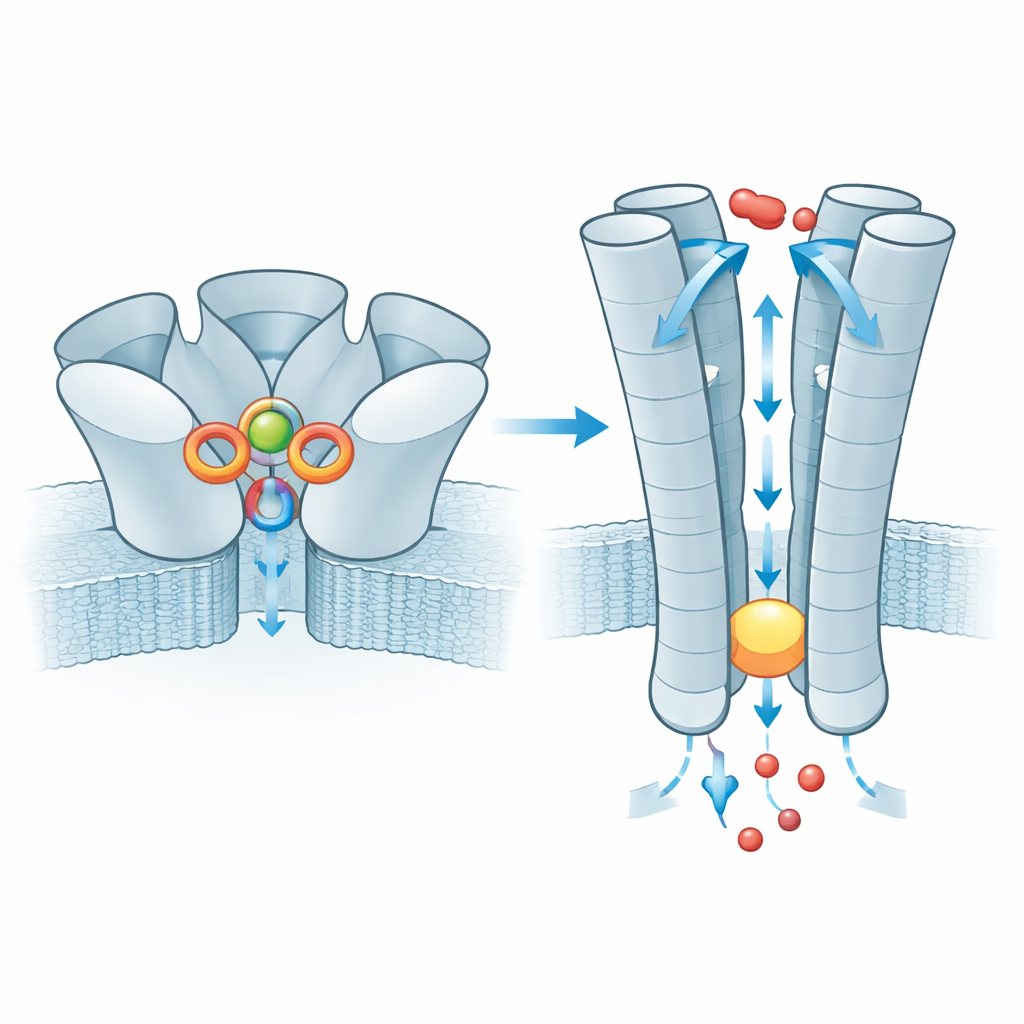
O Caminho para os Íons e uma Variante Genética Comum
Uma vez que o zinco se ligou, o efeito é transmitido para a parte do ZAC que atravessa a membrana, onde cinco hélices internas formam o poro. No estado de repouso esse tubo se estreita em torno de um anel de resíduos de leucina, criando um plugue hidrofóbico que bloqueia a movimentação de íons. Com o zinco ligado, o plugue se alarga o suficiente para permitir que pequenos íons positivos como sódio e potássio passem, enquanto o revestimento carregado do poro ajuda a selecionar esses íons. A equipe também examinou uma variante humana muito comum do ZAC na qual um único aminoácido (treonina) é substituído por alanina em uma curta fita acima do plugue. Essa pequena alteração enfraquece uma rede de interações entre subunidades vizinhas que normalmente ajuda a transmitir a ligação do zinco ao portão, e medidas elétricas mostram que canais formados por essa variante conduzem correntes muito menores. A variante, portanto, atua como um conversor de sinal menos eficiente, embora seu impacto na fisiologia humana permaneça desconhecido.
Como Dois Fármacos Silenciam o Canal
Além do zinco, o estudo também explora como dois antagonistas, TTFB e d‑tubocurarina (d‑TC), inativam o ZAC. O TTFB é uma pequena molécula feita sob medida que acaba se alojando profundamente na região da membrana, deslizando entre duas das hélices que formam o poro logo acima do portão. Ali, interage com um bolso hidrofóbico justo e com resíduos polares próximos, efetivamente travando as hélices para que não possam se mover para um estado condutor totalmente aberto. A d‑TC, um fármaco mais antigo usado como relaxante muscular, age de forma mais ampla. Uma molécula de d‑TC se liga ao mesmo bolso externo que normalmente acolhe o zinco, mimetizando a carga positiva do zinco, mas bloqueando a ligação adequada do zinco real. Uma segunda molécula de d‑TC se posiciona na entrada do próprio poro, tampando fisicamente o túnel. Juntas, essas ligações prendem o ZAC em uma conformação dessensibilizada e não condutora, enquanto a forma da proteína permanece relativamente aberta.
O Que as Descobertas Significam para o Zinco e a Saúde
Este trabalho estrutural mostra em detalhe molecular claro que o ZAC é um sensor genuíno de zinco, usando um berço aromático incomum para detectar o metal no mesmo tipo de sítio onde outros membros da família se ligam a neurotransmissores. Ele também identifica redes de interação específicas que ajustam com que facilidade o canal abre e fecha, e mapeia dois sítios distintos de ligação a fármacos que podem ou enfiar o portão ou emperrar o poro. Para não especialistas, a mensagem principal é que o zinco não é apenas um nutriente estático, mas um sinal ativo, e o ZAC é um de seus receptores dedicados. À medida que os cientistas buscam os papéis do ZAC no corpo humano e em transtornos neurológicos ligados ao desequilíbrio de zinco, essas plantas de nível atômico fornecem um roteiro para projetar moléculas mais precisas para modular esse canal e, potencialmente, corrigir a sinalização por zinco perturbada.
Citação: Zhou, Z., Long, Y., Chao, Y. et al. Structural basis of human zinc-activated channel (ZAC) signaling and modulation. Cell Discov 12, 23 (2026). https://doi.org/10.1038/s41421-026-00878-5
Palavras-chave: sinalização por zinco, canais iônicos ativados por ligante, neurociência, estrutura por crio‑EM, modulação de canais