Clear Sky Science · pt
Palmitoilação de ASCT2 regulada pelo eixo JNK1-ZDHHC14 orquestra o metabolismo da glutamina e a progressão do NSCLC
Alimentando o fogo do câncer de pulmão
Muitos cânceres pulmonares de rápido crescimento são dependentes da glutamina, um aminoácido comum que serve como combustível e bloco de construção. Este estudo revela como as células tumorais ajustam um importante “portão” de entrada de glutamina em sua superfície e como interromper esse sistema de controle pode retardar o crescimento do câncer. Compreender essa válvula de combustível oculta ajuda a explicar por que alguns tumores são tão difíceis de privar de nutrientes e aponta para novas combinações de drogas que podem cortar seu suprimento de energia de forma mais eficaz.
Um portão celular para a glutamina
A glutamina entra nas células principalmente por meio de uma proteína transportadora chamada ASCT2, localizada na membrana externa e responsável por levar a glutamina para o interior. O câncer de pulmão não pequenas células (NSCLC), a forma mais comum de câncer de pulmão, muitas vezes depende fortemente da glutamina para sustentar a rápida divisão celular e a sobrevivência. Níveis elevados de ASCT2 em tumores estão associados a doença agressiva e piores desfechos nos pacientes. Ainda assim, o próprio ASCT2 está constantemente sendo sintetizado, modificado e degradado, levantando a questão: o que determina quanto desse guardião permanece na superfície celular em um dado momento?
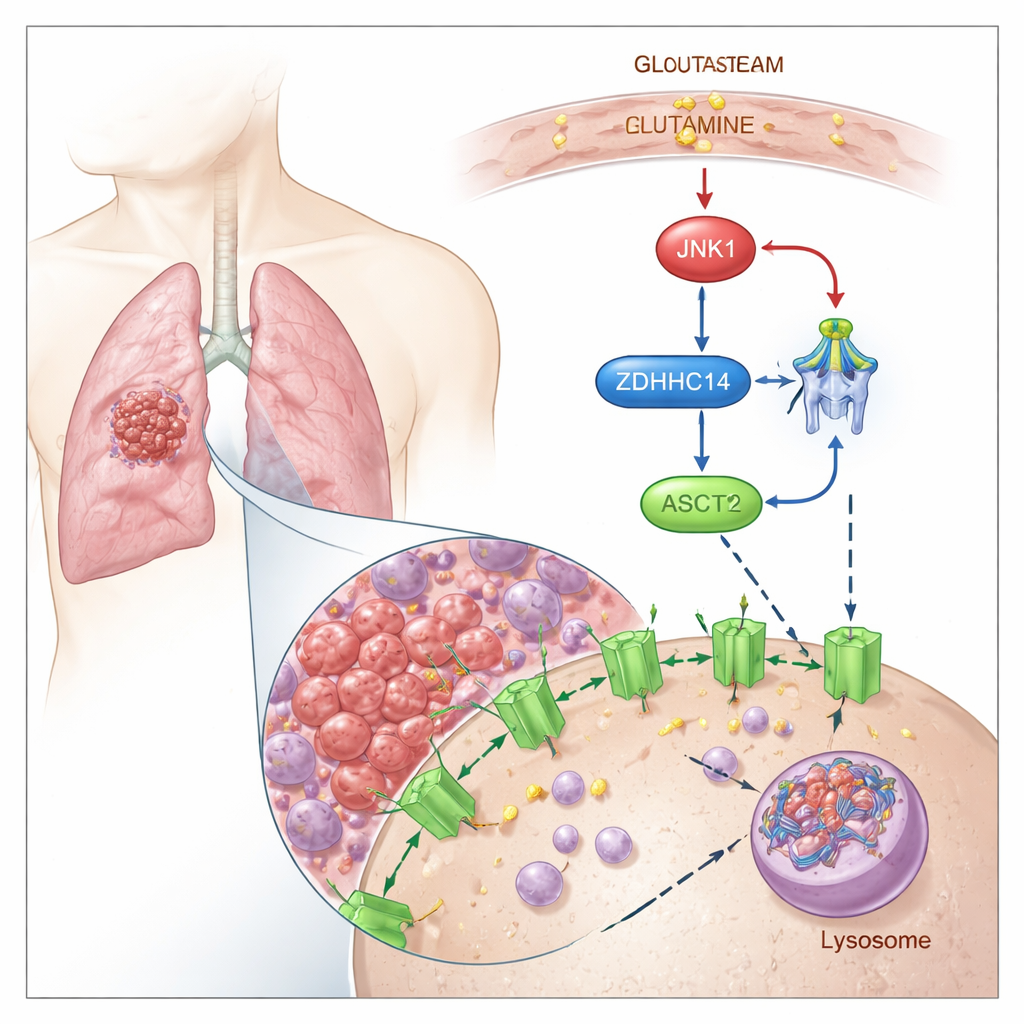
Marcando o ASCT2 para degradação
Os pesquisadores mostram que o ASCT2 é controlado por uma “etiqueta” química chamada palmitoilação, na qual um ácido graxo é ligado a cisteínas específicas da proteína. Eles descobriram que uma enzima chamada ZDHHC14 adiciona essa marca lipídica a dois sítios conservados no ASCT2 (Cys39 e Cys48). Uma vez marcado, o ASCT2 é redirecionado da superfície celular para centros de reciclagem chamados lisossomos, onde é degradado. Bloquear a palmitoilação impede que o ASCT2 seja marcado e degradado, levando a níveis mais altos da proteína ASCT2 e ao aumento da captação de glutamina, sem alterar a atividade gênica subjacente.
Uma contra-enzima que protege o portão
Oposto à ZDHHC14 está outra enzima, ABHD17B, que remove a marca lipídica do ASCT2. Quando a ABHD17B está ativa, o ASCT2 é menos palmitoilado, mais estável e mais propenso a ser reciclado de volta para a superfície celular em vez de enviado ao lisossomo. Esse ciclo de marcação e desmarcação funciona como um regulador fino do fluxo de glutamina: a ZDHHC14 empurra o ASCT2 em direção à destruição, enquanto a ABHD17B o resgata e sustenta o transporte de glutamina. Em células de câncer de pulmão, deslocar esse equilíbrio para menos palmitoilação aumenta a captação de glutamina e favorece o crescimento tumoral em culturas e em camundongos.
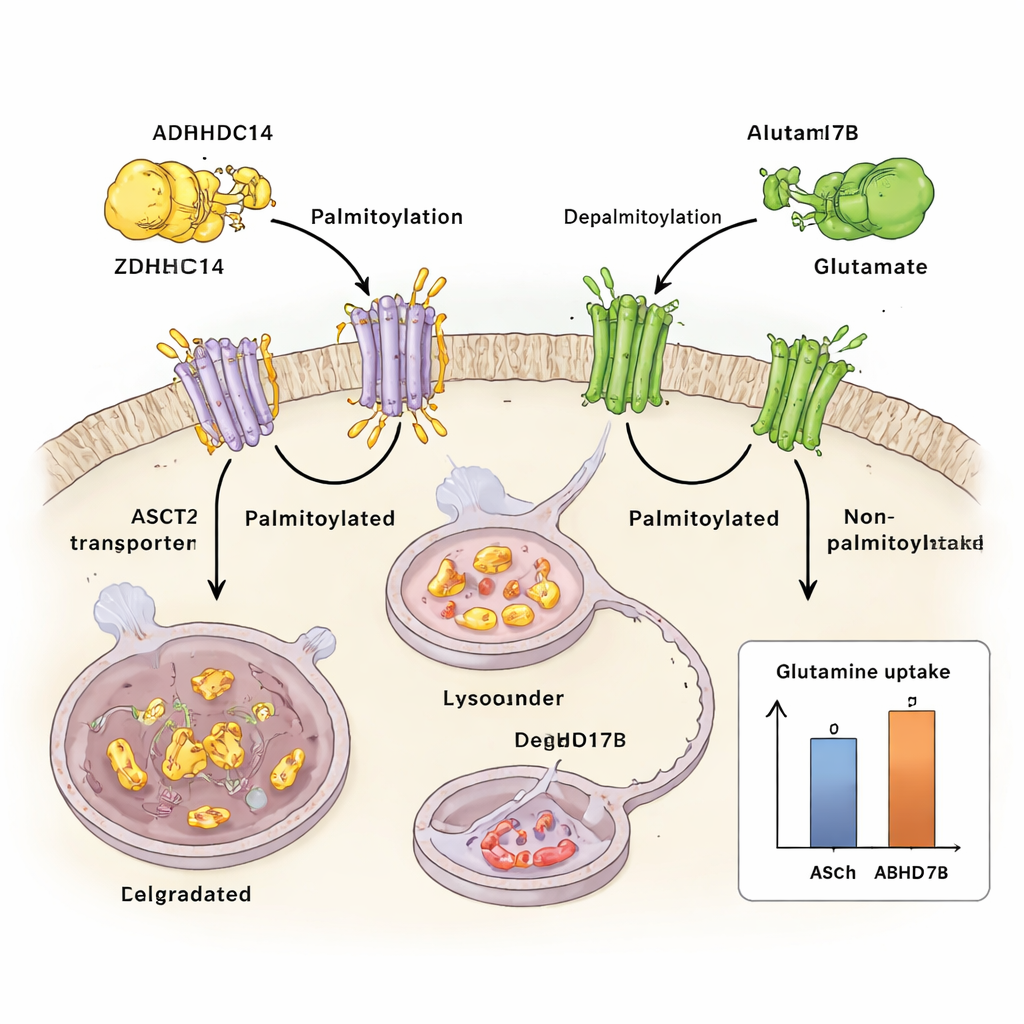
Como o estresse nutricional reprograma o sistema
A equipe então examinou o que acontece quando as células tumorais ficam com pouca glutamina. Sob privação de glutamina, uma proteína de sinalização sensível ao estresse chamada JNK1 é ativada. A JNK1 liga-se fisicamente à ZDHHC14 e adiciona um grupo fosfato em um sítio específico (Thr440), marcando a ZDHHC14 para sua própria degradação lisossomal. À medida que os níveis de ZDHHC14 caem, o ASCT2 recebe menos marcas de palmitoilação, escapa da degradação e se acumula na superfície celular — precisamente quando a célula mais precisa vasculhar a glutamina escassa. A mutação desse único sítio sensível à JNK1 estabiliza a ZDHHC14, restaura a marcação do ASCT2 e reduz a captação de glutamina, ressaltando o quão intimamente o estresse nutricional está integrado a esse circuito de controle.
Traduzindo o mecanismo em terapia
Porque o ASCT2 é tão importante para o metabolismo tumoral, drogas que o bloqueiam, como o composto experimental V9302, estão sendo exploradas como tratamentos contra o câncer. Este estudo revela que a sinalização JNK1 pode contrariar a destruição do ASCT2, protegendo efetivamente o portão de entrada da glutamina. Em modelos celulares e murinos de NSCLC, a combinação de um inibidor de JNK com V9302 reduziu mais fortemente a captação de glutamina, o crescimento das células tumorais e o tamanho do tumor do que cada droga isoladamente. Amostras de pacientes e bases de dados públicas mostram ainda que baixos níveis de ZDHHC14 e altos níveis de ASCT2 são comuns no NSCLC e associados a pior sobrevida, sugerindo que esse padrão molecular poderia ajudar a identificar pacientes mais propensos a se beneficiarem do direcionamento desse caminho.
O que isso significa para os pacientes
Em termos práticos, este trabalho mostra que certos cânceres de pulmão controlam seu combustível preferido ajustando uma válvula molecular em sua superfície. Um trio de atores — JNK1, ZDHHC14 e ABHD17B — decide se o portão de glutamina ASCT2 é marcado para destruição ou mantido aberto. Quando a glutamina é escassa, o sistema se desloca para preservar o ASCT2 e manter o fluxo de combustível, ajudando os tumores a sobreviver em condições adversas. Ao bloquear simultaneamente o ASCT2 e a via JNK que o protege, os pesquisadores conseguiram privar as células cancerosas de nutrientes com mais eficácia em modelos de laboratório e animais. Embora sejam necessários mais testes, esse eixo fosforilação–palmitoilação oferece um novo ângulo promissor para terapias que visam cortar as linhas de vida nutricionais de tumores pulmonares famintos por glutamina.
Citação: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
Palavras-chave: metabolismo da glutamina, câncer de pulmão não pequenas células, transportador ASCT2, palmitoilação de proteínas, sinalização JNK