Clear Sky Science · pt
Inibir HSP27 ativa a interação XBP1s/CerS1, que desencadeia mitofagia dirigida por DRP1, protegendo contra a morte celular e promovendo o ciclo lítico do KSHV em células de linfoma de efusão primária
Quando o estresse celular vira uma espada de dois gumes
Nossas células sobrevivem a agressões diárias ativando programas de emergência que reparam danos e as mantêm vivas. Células cancerosas, no entanto, podem sequestrar esses mesmos programas para crescer e abrigar vírus latentes. Este artigo explora como bloquear uma única proteína de proteção ao estresse em um linfoma raro não apenas empurra as células tumorais na direção da morte, mas também oferece ao vírus oculto nelas uma janela para despertar e se multiplicar. Compreender esse equilíbrio delicado pode ajudar a desenhar terapias que matem o câncer enquanto neguem ao vírus a chance de se espalhar.
Um vírus oculto em um linfoma agressivo
O linfoma de efusão primária é um câncer de células B altamente agressivo, um tipo de glóbulo branco. A maioria dessas células tumorais carrega um passageiro dormente: o herpesvírus associado ao sarcoma de Kaposi (KSHV). Em seu estado silencioso, ou latente, o vírus produz apenas algumas proteínas e se esconde no genoma do hospedeiro. Certos estresses podem empurrá‑lo para uma fase ativa, lítica, na qual copia seu material e produz novas partículas virais, geralmente matando a célula hospedeira. As próprias células tumorais dependem de vários sistemas de resposta ao estresse, incluindo as chamadas proteínas de choque térmico e a resposta a proteínas desnaturadas (unfolded protein response), que as ajudam a lidar com proteínas mal dobradas, metabolismo lipídico perturbado e danos às suas mitocôndrias produtoras de energia. 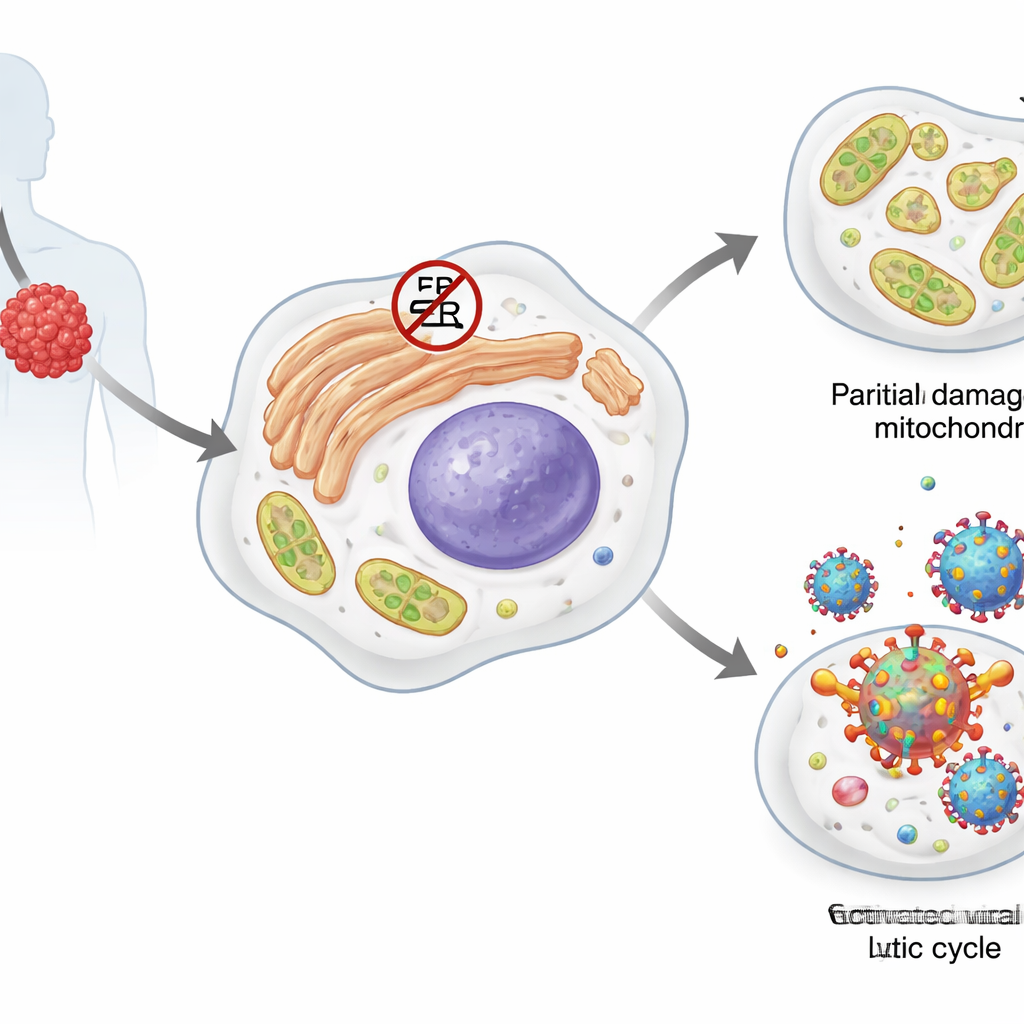
Bloqueando um guarda-costas celular
Os pesquisadores focaram em HSP27, uma pequena proteína de choque térmico conhecida por proteger as células do estresse. Usando um inibidor químico chamado J2 ou silenciando o gene com pequenos RNAs, eles reduziram a atividade de HSP27 em células de linfoma cultivadas em laboratório. Isso tornou as células menos propensas a sobreviver e desencadeou um forte sinal de estresse em uma rede de membranas interna chamada retículo endoplasmático. Marcadores dessa resposta, incluindo fatores protetores e pró‑mortais, aumentaram, e um interruptor chave chamado XBP1s foi ativado. Ao mesmo tempo, as células mostraram mais sinais de morte celular programada, confirmando que retirar HSP27 as empurra para um ponto de inflexão entre sobrevivência e colapso.
Um ciclo de estresse que dialoga com os lipídios celulares
O estresse no retículo endoplasmático está intimamente interligado com a forma como as células lidam com lipídios. A equipe descobriu que bloquear HSP27 aumentou os níveis de CerS1, uma enzima que sintetiza uma molécula lipídica específica chamada ceramida C18. Quando bloquearam quimicamente XBP1s, o aumento de CerS1 desapareceu, mostrando que XBP1s ajuda a ligar o gene CerS1 nessas condições. De forma marcante, inibir CerS1 por sua vez reduziu XBP1s, revelando um circuito de retroalimentação positiva: cada fator sustenta o outro. Esse aperto molecular não apenas remodela o metabolismo lipídico, mas também reforça a capacidade da célula de se adaptar ao estresse do retículo endoplasmático, mesmo enquanto sinais de morte se acumulam.
Mitocôndrias recicladas em vez de destruídas
O estresse em uma parte da célula frequentemente se espalha para as mitocôndrias, as pequenas usinas que geram energia. Depois que HSP27 foi bloqueada, as células do linfoma produziram mais espécies reativas de oxigênio, um sinal de disfunção mitocondrial, e aumentaram os níveis de DRP1, uma proteína que fragmenta as mitocôndrias em pedaços menores. Os autores demonstraram que o circuito XBP1s–CerS1 foi responsável por elevar DRP1. Isso, por sua vez, desencadeou a mitofagia, um processo de controle de qualidade em que mitocôndrias danificadas são envolvidas por membranas e levadas a “centros de reciclagem” celulares chamados lisossomos. Usando corantes fluorescentes e marcadores proteicos, confirmaram que as mitocôndrias estavam sendo removidas seletivamente. Quando bloquearam DRP1 quimicamente ou geneticamente, essa mitofagia foi reduzida e as células morreram mais facilmente, o que significa que o reaproveitamento mitocondrial estava ajudando as células tumorais estressadas a persistir. 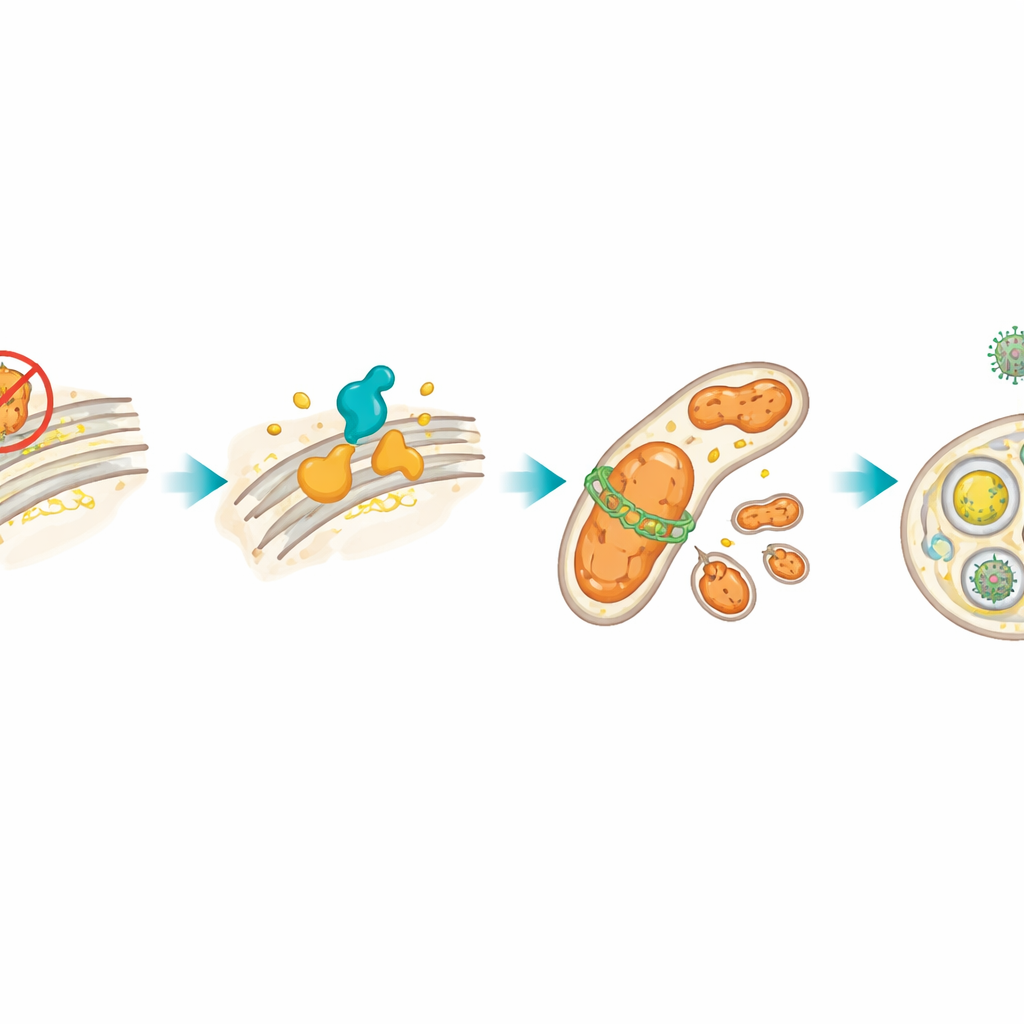
Dando ao vírus tempo para escapar
A mesma mitofagia que protegeu as células tumorais também beneficiou o KSHV. A ativação de XBP1s, o acúmulo de ceramida C18 e o aumento da fissão mitocondrial já foram ligados ao reativamento desse vírus. Aqui, quando HSP27 foi inibida, mais células expressaram proteínas virais precoces e tardias, sinais claros de replicação lítica. Bloquear DRP1, e portanto a mitofagia, reduziu esse reativamento viral. Os autores sugerem que, ao prolongar levemente a sobrevivência celular sob estresse, a mitofagia dá ao KSHV tempo para completar seu ciclo de replicação e sair da célula moribunda, potencialmente infectando novos alvos e contribuindo para o desenvolvimento do câncer.
O que isso significa para tratamentos futuros
Para um não especialista, a mensagem principal é que HSP27 atua como um controlador central do tráfego sobre como células de linfoma lidam com o estresse, como reciclam mitocôndrias danificadas e como um vírus associado ao câncer decide quando despertar. Desligar HSP27 desencadeia uma cadeia de eventos que tanto compromete a sobrevivência celular quanto, paradoxalmente, protege temporariamente as células por meio da mitofagia enquanto permite que o KSHV se replique. Do ponto de vista terapêutico, combinar a inibição de HSP27 com drogas que bloqueiem a mitofagia dirigida por DRP1 poderia empurrar as células tumorais a morrer mais rapidamente e limitar a chance de disseminação viral, oferecendo uma estratégia dupla contra esse linfoma letal.
Citação: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
Palavras-chave: linfoma de efusão primária, vírus da síndrome de Kaposi, resposta ao estresse celular, mitofagia, proteína de choque térmico HSP27