Clear Sky Science · pt
Um modelo viável de camundongo com RIPK3 quinase-inativa D143N revela sua função de andaime na promoção de distúrbio inflamatório induzido por TNF
Por que este estudo em camundongos importa para a inflamação
Muitas doenças graves, de infecções letais a crises autoimunes, são impulsionadas não apenas por germes ou genes, mas pela própria inflamação descontrolada do organismo. Uma proteína chamada RIPK3 tem sido vista há muito tempo como um executor chave de uma forma violenta de morte celular que alimenta essa inflamação, tornando-a um alvo atraente para fármacos. Mas o RIPK3 também tem outros papéis menos compreendidos dentro das células. Este estudo descreve um novo tipo de camundongo de laboratório que separa nitidamente a atividade letal do RIPK3 de seu papel de “andaime” de sinalização, revelando como cada função contribui para a inflamação e apontando para novas estratégias terapêuticas.
Duas maneiras de uma proteína da morte agir
As células podem morrer de forma ordenada ou desordenada. Na morte celular “silenciosa” e organizada, o organismo recicla partes celulares sem grande alarme. Em uma forma mais desordenada chamada necroptose, as células rompem e derramam seu conteúdo, desencadeando fortes respostas imunes. O RIPK3 é central na necroptose: quando ativado, ele estimula outra proteína que perfura a membrana celular. Entretanto, trabalhos anteriores sugeriam que o RIPK3 também pode ajudar a desencadear suicídio celular clássico mediado por caspases e pode ampliar a sinalização inflamatória mesmo sem matar células. Separar esses papéis tem sido difícil porque formas inativas existentes de RIPK3 ou matavam embriões ou reduzíam drasticamente os níveis da proteína, dificultando o estudo de seu comportamento estrutural normal.
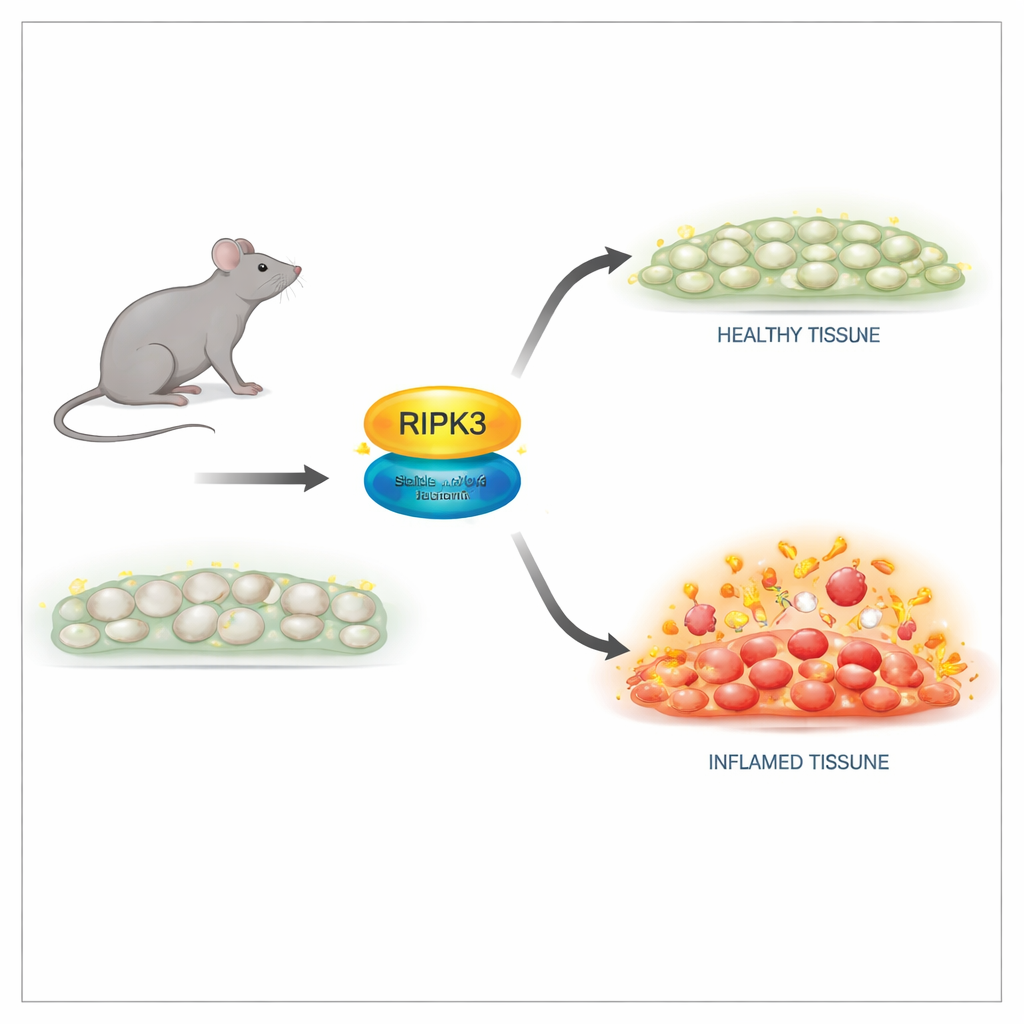
Uma maneira mais segura de desligar a função letal
Os pesquisadores engenheiraram camundongos com uma alteração sutil na proteína RIPK3 em uma única posição, denominada D143N, que desativa sua atividade enzimática preservando sua estrutura. Em células desses camundongos, os níveis de RIPK3 e a arquitetura tecidual pareciam normais, e os animais nasceram e cresceram como seus companheiros saudáveis. Importante, células com a versão D143N foram completamente resistentes a múltiplos gatilhos de necroptose, incluindo sinais do fator de necrose tumoral (TNF), receptores tipo toll e infecção viral. O RIPK3 mutante não conseguia mais ativar seu parceiro a jusante nem formar o complexo destrutivo necessário para a ruptura da membrana, contudo não provocou apoptose espontânea, evitando os efeitos colaterais letais observados em mutantes antigos de RIPK3.
Separando desenvolvimento de doença
Um dos papéis mais conhecidos do RIPK3 aparece em embriões que carecem de outra proteína chave, a caspase-8: sem caspase-8, a necroptose guiada por RIPK3 mata o embrião. Neste estudo, a introdução da versão D143N de RIPK3 resgatou completamente esses camundongos, que seriam de outra forma inviáveis. Eles se desenvolveram normalmente e foram férteis, provando que a atividade letal do RIPK3 é dispensável para o desenvolvimento normal quando sua estrutura é preservada. Ainda assim, quando camundongos adultos foram desafiados com alta dose de TNF para induzir uma síndrome inflamatória tipo choque, o quadro mudou. Animais completamente desprovidos de RIPK3 foram fortemente protegidos contra morte, dano tecidual e moléculas inflamatórias no sangue. Camundongos com a versão D143N, apesar de não apresentarem necroptose, foram apenas parcialmente protegidos. Isso indicou que o papel estrutural não letal do RIPK3 ainda contribuía para impulsionar a inflamação.
Sinalização de andaime que atiça as chamas
Para entender essa contribuição não letal, a equipe examinou a atividade gênica no intestino de camundongos tratados com TNF. Em animais deficientes em RIPK3, muitos genes inflamatórios foram fortemente atenuados. Em camundongos D143N, entretanto, a supressão foi mais fraca, e genes ligados à resposta interferon e à imunidade inata permaneceram mais ativos. No nível proteico, o TNF ativou robustamente as vias de sinalização JAK–STAT1 e ERK em camundongos normais e D143N, mas essa ativação esteve quase completamente ausente quando o RIPK3 foi deletado inteiramente. Isso mostrou que mesmo sem sua função letal, a presença física do RIPK3 em complexos de sinalização ajuda a transmitir sinais do TNF para um programa pró-inflamatório via JAK–STAT1.
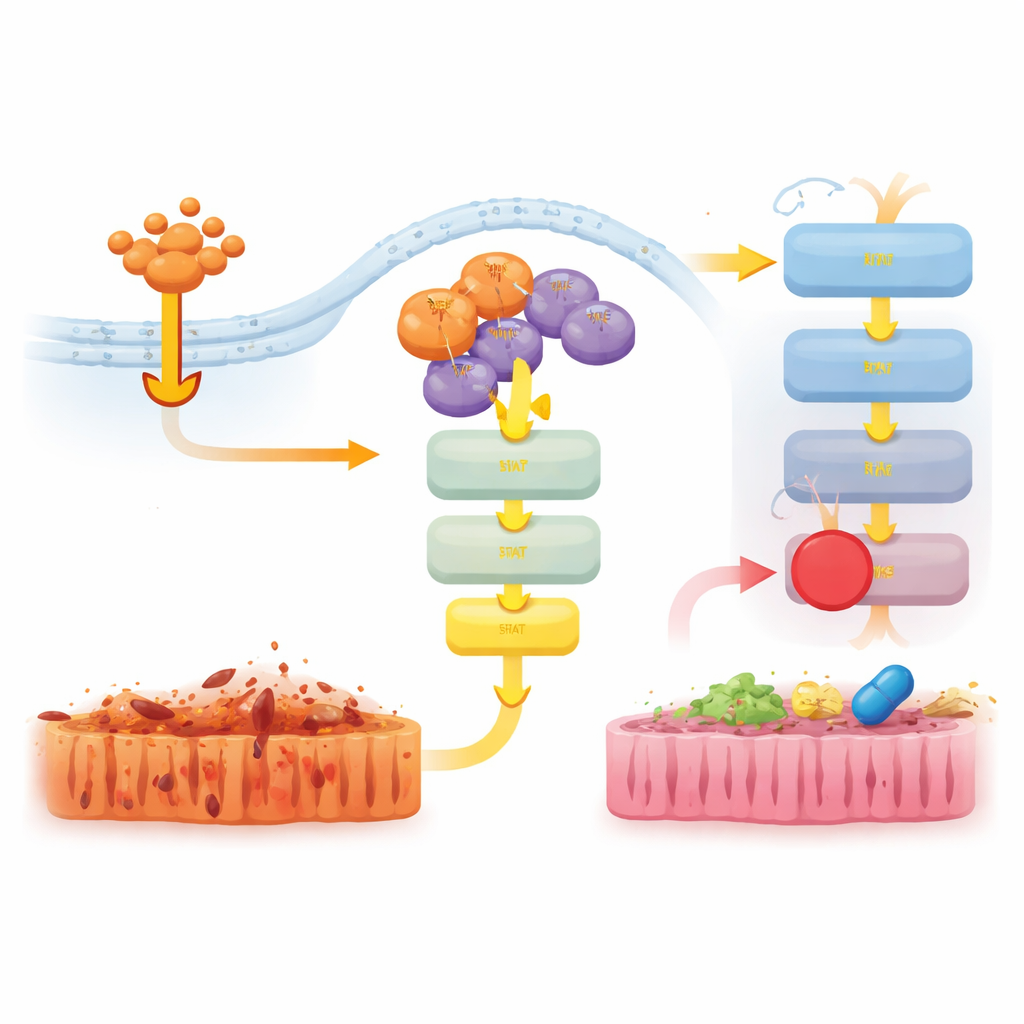
Reduzindo sinais nocivos com fármacos direcionados
Os pesquisadores então testaram se bloquear essas vias a jusante poderia aliviar a doença em camundongos D143N submetidos a choque induzido por TNF. Tratar os animais com um inibidor de JAK1/2, mas não com um inibidor de ERK, reduziu a perda de temperatura corporal, diminuiu os níveis da molécula inflamatória IL-6 e atenuou danos e morte celular no tecido intestinal. Um inibidor à parte direcionado a outra proteína, RIPK1, também protegeu fortemente os camundongos e reduziu a ativação de JAK–STAT1 e ERK. Juntos, esses resultados sugerem que a função de andaime do RIPK3 se associa ao RIPK1 para ativar JAK–STAT1 e promover inflamação, e que interromper essa sinalização pode reduzir lesão tecidual mesmo quando a necroptose já está bloqueada.
O que isso significa para tratamentos futuros
Por anos, o RIPK3 foi visto principalmente como um interruptor de uma forma tóxica de morte celular, e o desenvolvimento de fármacos focou em desligar sua atividade enzimática. Este estudo mostra que isso pode não ser suficiente: o RIPK3 ainda pode atuar como uma plataforma física que amplifica sinais inflamatórios via JAK–STAT1, contribuindo para choque e dano tecidual. O novo modelo de camundongo D143N revela esses papéis duais com clareza incomum, estabelecendo uma ferramenta poderosa para estudar quando e como cada função importa em diferentes doenças. Para pacientes, o trabalho sugere que combinar drogas direcionadas a RIPK3 ou RIPK1 com bloqueadores de JAK–STAT1 pode acalmar de forma mais eficaz a inflamação nociva em condições impulsionadas por TNF e citocinas relacionadas.
Citação: Du, Y., Li, J., Zhao, C. et al. A viable kinase-inactive RIPK3 D143N mouse model reveals its scaffold function in driving TNF-induced inflammatory disorder. Cell Death Discov. 12, 107 (2026). https://doi.org/10.1038/s41420-026-02962-x
Palavras-chave: RIPK3, necroptose, inflamação, choque por TNF, JAK-STAT1