Clear Sky Science · pt
O eixo AdipoR1–AMPK suprime o câncer de mama em subtipos moleculares diversos via vias multimodais de morte celular, incluindo ferroptose e apoptose
Por que as células de gordura importam no câncer de mama
A maioria de nós pensa na gordura corporal como um depósito passivo de energia, mas as células adiposas são fábricas ativas que liberam hormônios e moléculas de sinalização na corrente sanguínea. Este estudo investiga como um desses sinais derivados da gordura, atuando por meio de uma molécula chamada AdipoR1 nas células de câncer de mama, pode retardar o crescimento tumoral. O trabalho é importante porque sugere uma nova forma de tratar muitas formas de câncer de mama ao aproveitar a comunicação entre o tecido adiposo e os tumores, potencialmente ampliando os efeitos de medicamentos existentes.
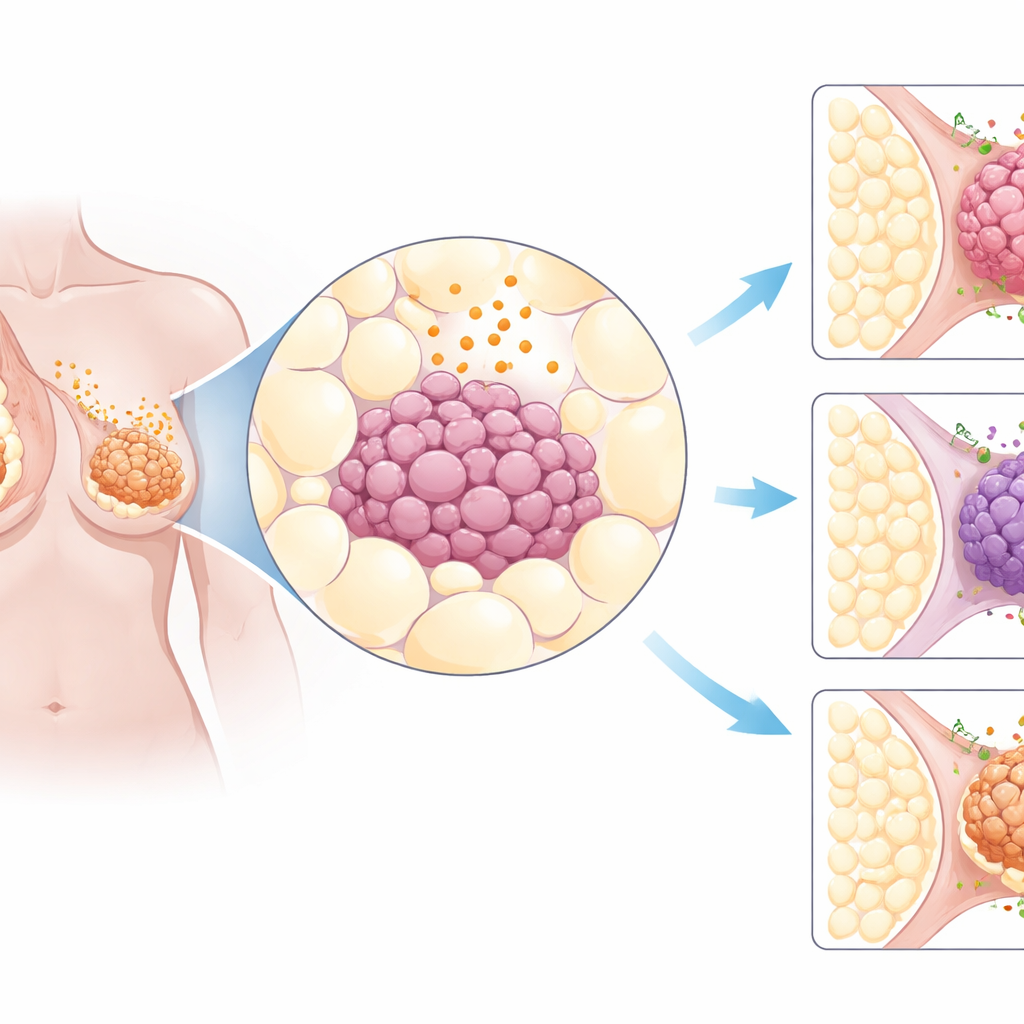
Analisando diversos tipos de câncer
Os pesquisadores começaram minerando grandes bancos de dados públicos de câncer que contêm informações genéticas de milhares de tumores de pacientes. Eles se concentraram em cerca de três dezenas de genes envolvidos em sinais provenientes do tecido adiposo e nas estruturas celulares que recebem esses sinais. Quando compararam tumores de 31 órgãos diferentes com tecido saudável, um padrão se destacou: os cânceres de mama mostraram mudanças especialmente fortes nesses sinais relacionados à gordura. Em particular, o receptor AdipoR1 esteve frequentemente presente em níveis mais altos do que o normal nos tumores de mama, independentemente de serem hormonais, HER2‑positivos ou do subtipo mais agressivo triplo‑negativo. Amostras de tecido de mais de 600 cânceres de mama confirmaram que a proteína AdipoR1 estava amplamente presente nas células tumorais.
Testando um fármaco que mimetiza sinal da gordura em células cancerosas
Para ver o que o AdipoR1 realmente faz dentro dos tumores, a equipe recorreu a linhagens de células de câncer de mama cultivadas em laboratório, representando vários subtipos comuns. Tratou‑as com AdipoRon, uma pequena molécula que ativa o AdipoR1. O AdipoRon acionou rapidamente uma chave conhecida de sensoriamento de energia nas células chamada AMPK, mostrando que o sinal estava sendo transmitido. À medida que a dose de AdipoRon aumentava, as células cancerosas se dividiam mais lentamente, moviam‑se menos em testes de cicatrização de ferida e muitas passaram por autodestruição programada. Quando os pesquisadores reduziram deliberadamente os níveis de AdipoR1 nas células, o AdipoRon perdeu grande parte de sua eficácia, enquanto o aumento de AdipoR1 tornou o fármaco mais eficaz, vinculando o efeito diretamente a esse receptor.
Várias maneiras de empurrar as células cancerosas rumo à morte
Ao analisar a atividade gênica após o tratamento, os cientistas descobriram que o AdipoRon ativou respostas de estresse dentro das células de câncer de mama. Ele ativou genes ligados à morte celular programada clássica, bem como aqueles envolvidos em uma forma mais recentemente reconhecida de destruição celular dependente de ferro chamada ferroptose. Marcadores-chave desse processo aumentaram tanto no nível de RNA quanto de proteínas, especialmente em células de câncer de mama sensíveis a hormônios, e leituras químicas de lipídios celulares danificados apoiaram essa conclusão. Ao mesmo tempo, o AdipoRon reduziu os níveis de proteínas que normalmente ajudam as células cancerosas a sobreviver, incluindo auxiliares de reparo de DNA (BRCA1 e BRCA2), o receptor de estrogênio que impulsiona o crescimento em muitos tumores, e TROP2, uma molécula de superfície associada a comportamento agressivo.
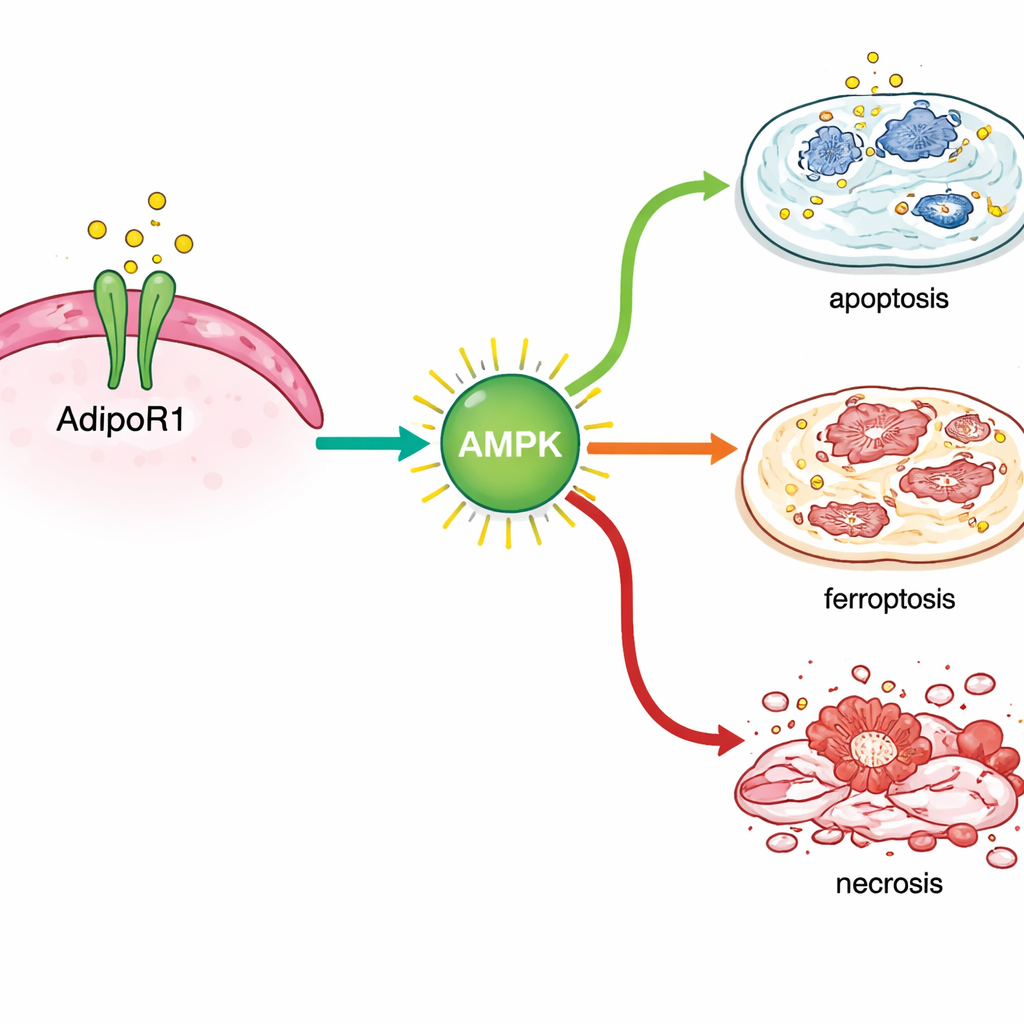
Trabalhando com, e não contra, os tratamentos atuais
A equipe então investigou se ativar o AdipoR1 poderia complementar os medicamentos padrão. Em células de câncer de mama sensíveis a hormônios, AdipoRon combinado com tamoxifeno produziu maior supressão do crescimento do que qualquer um dos fármacos isoladamente. Em linhagens triplo‑negativas, o AdipoRon potencializou os efeitos de agentes quimioterápicos comuns, como paclitaxel e doxorrubicina. Em mice com tumores de mama sensíveis a hormônios, os pesquisadores administraram AdipoRon por via oral. Os tumores nos animais tratados cresceram mais lentamente e continham zonas necróticas maiores quando examinados ao microscópio. Importante, os camundongos não mostraram efeitos colaterais óbvios no comportamento, no peso ou na saúde hepática durante o período de tratamento.
O que isso pode significar para os pacientes
Em conjunto, os achados sugerem que ativar o AdipoR1 nas células de câncer de mama aciona várias rotas sobrepostas para a morte celular enquanto enfraquece sistemas-chave de sobrevivência, e que essa abordagem funciona em diferentes formas genéticas da doença. Em vez de substituir as terapias atuais, fármacos que têm como alvo o AdipoR1, como o AdipoRon, poderiam atuar como complementos que tornam os tumores mais vulneráveis à terapia hormonal, à quimioterapia ou a futuros agentes direcionados. Antes que essa estratégia chegue à clínica, os pesquisadores precisarão desenvolver ativadores de AdipoR1 mais potentes e seletivos, esclarecer em quais tumores de pacientes o receptor é mais fortemente expresso e avaliar cuidadosamente a segurança. Ainda assim, este trabalho aponta para uma ideia intrigante: os sinais do nosso próprio tecido adiposo poderiam ser redirecionados para ajudar a combater o câncer de mama em vez de alimentá‑lo.
Citação: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
Palavras-chave: câncer de mama, adipocinas, AdipoR1, vias de morte celular, metabolismo do câncer