Clear Sky Science · pt
Alvo das variantes cancerígenas de p53 Y220C, Y220N e Y220S com o estabilizador de pequenas moléculas rezatapopt
Por que isso importa para tratamentos futuros do câncer
O câncer frequentemente desativa a p53, uma proteína às vezes chamada de “guardião” da célula, por meio de mutações que a impedem de controlar células perigosas. Uma alteração específica em p53, conhecida como Y220C, é comum em tumores sólidos e se tornou um caso‑teste para fármacos que visam consertar a p53 comprometida em vez de matar as células diretamente. Este estudo faz uma pergunta prática e orientada ao paciente: um candidato promissor em ensaios clínicos, o rezatapopt, que já é testado para Y220C, também pode ajudar pessoas cujos tumores carregam mutações intimamente relacionadas, porém mais raras, na mesma posição da p53?
Um fármaco projetado para vedar uma fissura em p53
Muitas mutações em p53 fazem a proteína se abrir e perder sua conformação precisa. Na mutação Y220C, a alteração cria uma pequena cavidade na superfície da proteína — um defeito que químicos perceberam poder “tapar” com pequenas moléculas sob medida para estabilizar a p53. O rezatapopt é uma dessas moléculas, desenvolvido a partir de séries químicas anteriores que se ligam a essa cavidade e funcionam como um reforço molecular. Os autores concentram‑se em duas outras mutações na mesma posição de aminoácido, Y220S e Y220N, que também escavam uma cavidade semelhante, mas destabilizam a p53 ainda mais que Y220C. Se o rezatapopt puder também reparar essas variantes, poderia ampliar essa abordagem de medicina de precisão para milhares de pacientes a mais a cada ano. 
Medindo quão bem o rezatapopt agarra e estabiliza a p53 mutante
Para testar isso, a equipe purificou o núcleo de ligação ao DNA da p53 com as alterações Y220C, Y220S ou Y220N e expôs cada uma ao rezatapopt (e a análogos químicos próximos). Usando ensaios baseados em calor, mostraram que as três proteínas mutantes tornaram‑se mais estáveis quando a droga se ligou, com Y220C e Y220S recuperando efetivamente uma robustez semelhante à da forma selvagem. Em contraste, Y220N recuperou apenas parte de sua estabilidade perdida. Uma segunda técnica que mede o calor liberado na ligação revelou o porquê: o rezatapopt se liga muito fortemente a Y220C (na faixa de algumas dezenas de nanomolares), um pouco menos firmemente a Y220S, e mais fracamente ainda a Y220N, embora todas estejam em faixas que químicos medicinais consideram promissoras.
Vendo o remendo molecular em detalhe atômico
Estruturas cristalográficas de alta resolução forneceram uma explicação visual. Nas três mutantes, o rezatapopt encaixa‑se na fenda criada pela mutação com uma pose conservada: sua estrutura central preenche a cavidade, uma extremidade alcança o fundo do bolso com um aglomerado de átomos de flúor, e a outra extremidade interage com uma alça proteica próxima. O fármaco estabelece uma rede de contatos, incluindo um átomo de flúor estrategicamente posicionado que interage com a espinha dorsal da proteína. Em Y220S, essas interações são preservadas com apenas pequenos deslocamentos, permitindo forte estabilização. Em Y220N, contudo, a ligação do fármaco força a cadeia lateral de asparagina para o núcleo oleoso da proteína de modo energeticamente desfavorável, e alguns contatos com a “âncora” fluorada do fármaco se perdem. Esse encaixe forçado explica tanto a ligação mais fraca quanto o resgate incompleto da estabilidade. 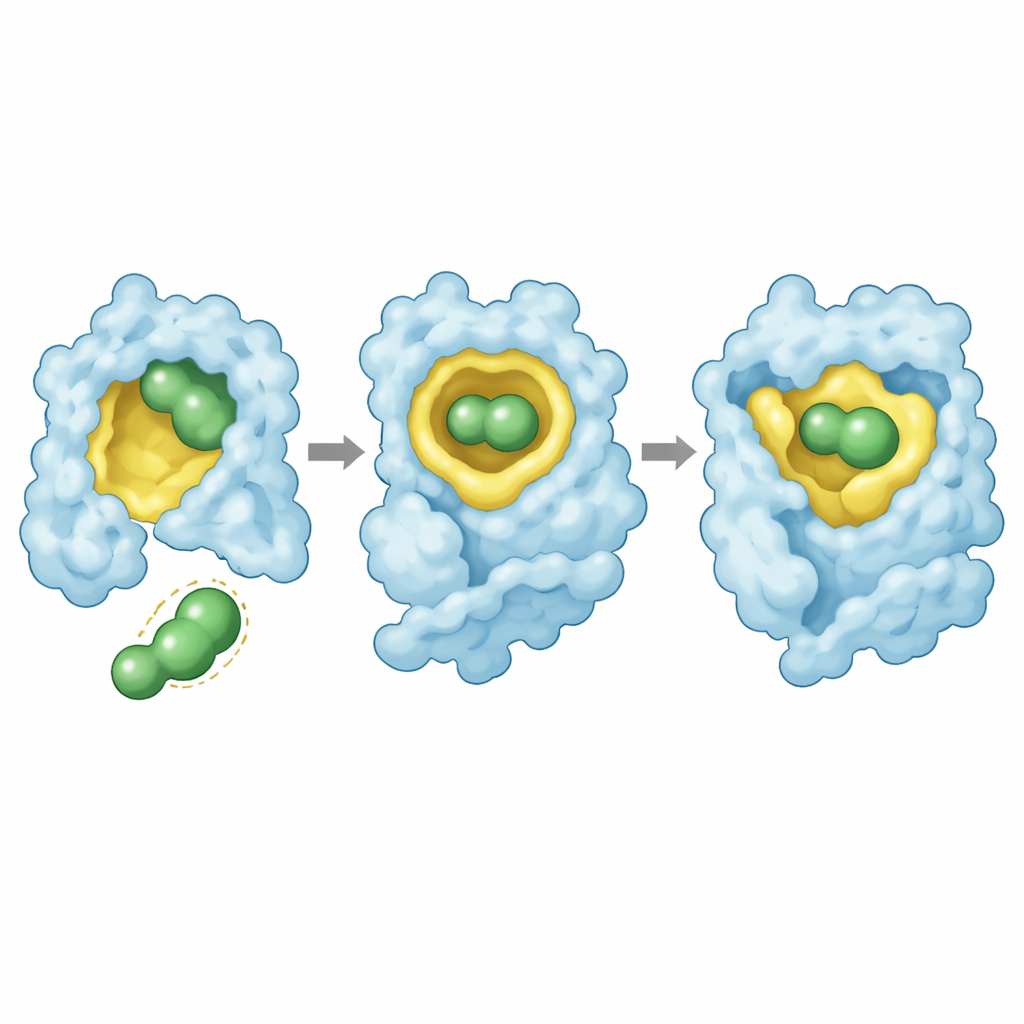
Da reparação da proteína ao comportamento celular
O teste crucial é saber se essa estabilização restaura o papel protetor da p53 dentro de células vivas. Os pesquisadores modificaram células de câncer de pulmão sem p53 natural para expressar as variantes Y220C, Y220S, Y220N ou Y220H. Quando tratadas com rezatapopt, as células com Y220C exibiram uma forte ativação de genes‑alvo clássicos de p53 envolvidos na parada do ciclo celular e na indução da morte celular. As células Y220S mostraram um padrão muito semelhante — recuperação da forma dobrada e ativa de p53, forte ativação gênica, proliferação reduzida e aumento da morte celular — mas apenas em concentrações do fármaco mais de dez vezes maiores que as necessárias para Y220C. As células Y220N, em comparação, não apresentaram ativação clara de genes‑alvo em doses toleráveis e permaneceram em grande parte na forma mal‑dobrada, embora efeitos leves de crescimento tardio sugiram um resgate funcional apenas parcial.
O que isso significa para pacientes e para o design de fármacos futuros
Para pessoas com tumores que carregam a mutação Y220S, esses resultados são cautelosamente encorajadores: o rezatapopt pode, em princípio, restaurar as funções protetoras da p53, mas apenas em doses substancialmente mais altas, que podem ser difíceis de alcançar com segurança em pacientes. Para Y220N, o fármaco atual parece insuficiente para reparar completamente a p53 em condições realistas. Ainda assim, os modelos estruturais deste trabalho mostram por que o desenho atual tem desempenho inferior e como moléculas futuras poderiam ser ajustadas para engajar as três cadeias laterais mutantes sem forçá‑las a posições desfavoráveis. Em outras palavras, criar um verdadeiro fármaco “pan‑Y220” para reparar p53 parece desafiador, mas alcançável, e ampliaria modestamente o número de pacientes que poderiam se beneficiar dessa estratégia emergente de consertar, em vez de substituir, o supressor tumoral do próprio corpo.
Citação: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
Palavras-chave: reativação de p53, rezatapopt, mutação Y220C, medicina de precisão contra o câncer, estabilização de proteínas