Clear Sky Science · pt
A desubiquitinação por OTUD4 estabiliza EGFR e ativa a via PI3K/AKT para promover a invasividade do câncer de mama triplo-negativo
Por que esta pesquisa importa para o câncer de mama
O câncer de mama triplo-negativo é uma das formas mais difíceis de tratar porque carece dos marcadores hormonais e de crescimento que muitos medicamentos visam. Este estudo revela uma molécula “protetora” oculta que ajuda as células tumorais a manter um poderoso interruptor de crescimento ativado. Ao entender esse sistema de suporte invisível, os cientistas podem encontrar novas maneiras de interromper os sinais que impulsionam o crescimento e a disseminação do tumor.
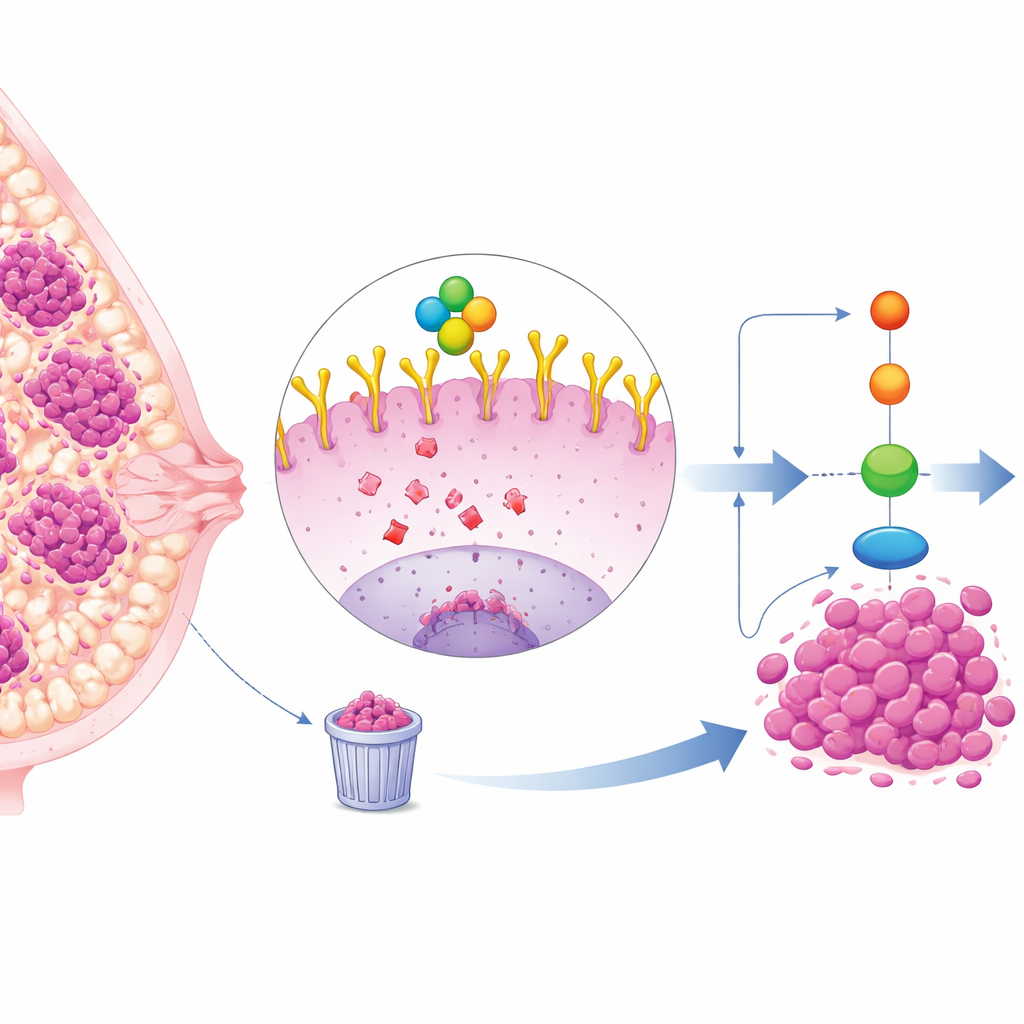
Um subtipo de câncer de mama difícil de tratar
O câncer de mama triplo-negativo (TNBC) representa cerca de um quarto dos casos de câncer de mama e tende a crescer e se disseminar mais rapidamente que outros subtipos. Como as células TNBC não apresentam receptores de estrogênio, progesterona ou HER2, as terapias alvo padrão são menos eficazes, deixando quimioterapia e cirurgia como as principais opções. Muitos tumores de TNBC, porém, exibem altos níveis de uma proteína de superfície celular chamada EGFR, que funciona como uma antena para receber sinais de crescimento e sobrevivência. Níveis elevados de EGFR estão associados a prognósticos piores, mas medicamentos que bloqueiam diretamente o EGFR tiveram resultados decepcionantes na clínica, sugerindo que existem camadas mais profundas de regulação em ação.
Encontrando um ajudante oculto do crescimento tumoral
Os pesquisadores focaram em OTUD4, uma enzima que remove pequenos rótulos proteicos chamados ubiquitinas de outras proteínas. Esses rótulos frequentemente atuam como sinais de descarte, marcando proteínas para serem degradadas, de modo que removê-los pode estabilizar e proteger a proteína marcada. Usando grandes bases de dados de câncer e amostras de tecido de pacientes, a equipe mostrou que OTUD4 está presente em níveis mais altos em tumores e linhagens celulares de TNBC do que em tecido mamário normal. Pacientes cujos tumores apresentavam mais OTUD4 tendiam a ter sobrevida pior, sugerindo que OTUD4 se comporta como um oncogene, um gene que ajuda a impulsionar a progressão do câncer.
Como OTUD4 torna as células cancerosas mais agressivas
Para testar o que OTUD4 faz nas células TNBC, os cientistas reduziram seus níveis em duas linhagens celulares TNBC amplamente estudadas. Quando OTUD4 foi silenciado, as células cancerosas cresceram mais devagar, formaram menos colônias e migraram menos em ensaios de cicatrização de ferida e Transwell, todos sinais de agressividade reduzida. Quando OTUD4 foi aumentado, o oposto ocorreu: as células proliferaram mais rápido e se moveram com mais facilidade, reforçando a ideia de que OTUD4 é um motor do comportamento maligno. Em camundongos, tumores formados por células sem OTUD4 cresceram mais devagar e mostraram redução de marcadores de divisão celular e sinais de crescimento, confirmando esses efeitos em organismos vivos.
Um escudo molecular que protege o EGFR
Aprofundando o mecanismo, a equipe usou triagens de interação proteica e ensaios bioquímicos para identificar o EGFR como parceiro de ligação direto de OTUD4. Eles descobriram que OTUD4 se liga a uma região específica do EGFR e remove cadeias de ubiquitina ligadas via K48, o tipo de rótulo que normalmente marca proteínas para destruição pela maquinaria de reciclagem celular. Quando OTUD4 foi reduzido, o EGFR degradou mais rapidamente, mas a atividade gênica do EGFR permaneceu a mesma, mostrando que OTUD4 age depois que o EGFR é produzido, não ao nível do DNA ou RNA. Bloquear o sistema de degradação proteica da célula restaurou os níveis de EGFR, ressaltando que o passo-chave é a proteção contra a degradação. Com mais EGFR estável na superfície celular, uma importante via de sinalização interna, a PI3K/AKT/mTOR, permanece ativada, impulsionando crescimento e sobrevivência celular.
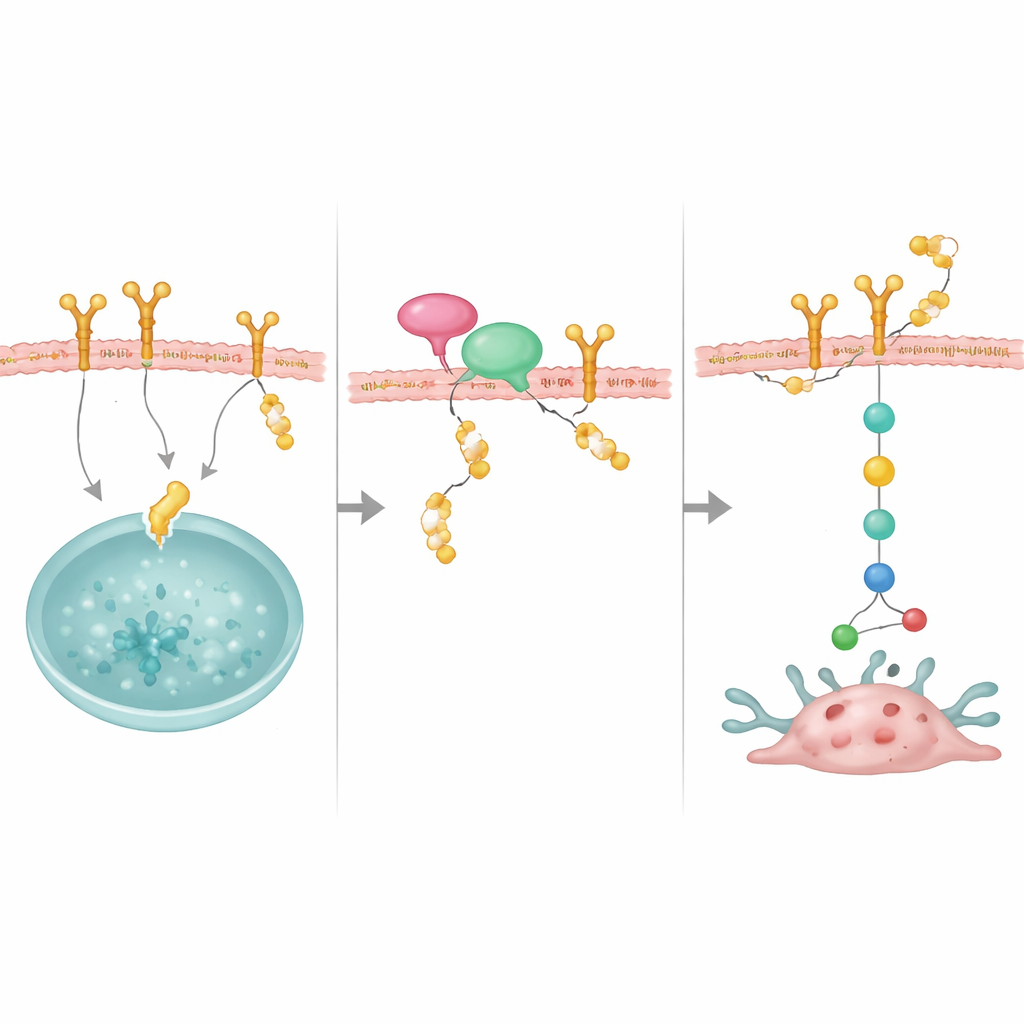
Um adaptador que traz o protetor até seu alvo
O estudo também revelou um parceiro importante, NRP1, uma proteína de membrana previamente ligada a cânceres de mama agressivos. NRP1 liga-se tanto a OTUD4 quanto ao EGFR e ajuda a posicionar OTUD4 para resgatar o EGFR da destruição. Quando NRP1 foi reduzido, o EGFR tornou-se menos estável e seus sinais de crescimento enfraqueceram, mesmo que os níveis de OTUD4 não tenham mudado. A superprodução de OTUD4 conseguiu contornar parcialmente a perda de NRP1, sugerindo que NRP1 atua como uma plataforma de ancoragem que recruta OTUD4 para o EGFR. Juntas, essas moléculas formam um complexo estabilizador que mantém o EGFR abundante na superfície celular.
O que isso significa para tratamentos futuros
Ao revelar como OTUD4 e NRP1 trabalham juntos para proteger o EGFR da degradação, este estudo identifica um novo ponto de controle para um sinal de crescimento chave no câncer de mama triplo-negativo. Em vez de tentar bloquear a atividade do EGFR em seu sítio ativo, terapias futuras podem visar interromper as ações protetoras de OTUD4 ou seu recrutamento por NRP1, reduzindo os níveis de EGFR e atenuando a via PI3K/AKT que alimenta o crescimento tumoral. Embora mais trabalhos sejam necessários para encontrar inibidores de OTUD4 seguros e eficazes e para entender possíveis rotas de escape usadas pelas células cancerosas, as descobertas abrem caminhos promissores para tratamentos mais precisos contra este subtipo desafiador de câncer de mama.
Citação: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
Palavras-chave: câncer de mama triplo-negativo, sinalização EGFR, OTUD4, via PI3K AKT, degradação de proteínas