Clear Sky Science · pt
A desidrogenase de acil-CoA de cadeia curta inicia a desmetilação do mtDNA e seu vazamento para alimentar a imunidade antitumoral no câncer colorretal
Por que nossas próprias células às vezes escondem o câncer do sistema imunológico
O câncer colorretal está entre os tumores mais letais do mundo, em parte porque as defesas imunes do organismo muitas vezes não conseguem reconhecê‑lo e atacá‑lo. Este estudo revela uma ligação inesperada entre como as células tumorais queimam gorduras, como suas pequenas usinas (mitocôndrias) lidam com o DNA e se o sistema imune é alertado sobre a presença do tumor. Ao rastrear essa cadeia de eventos, os pesquisadores também destacam um composto natural antigo, a hipericina, como um possível meio de reativar o ataque imune no câncer colorretal.
Um “guardião” mitocondrial ausente em tumores de cólon
A equipe começou pesquisando grandes conjuntos de dados humanos e de camundongos para encontrar genes metabólicos que mudam de forma consistente no câncer colorretal. Uma enzima se destacou: a desidrogenase de acil‑CoA de cadeia curta, ou ACADS, que normalmente ajuda as mitocôndrias a degradar ácidos graxos de cadeia curta. Tanto em amostras de pacientes quanto em vários modelos de camundongo, os níveis de ACADS estavam marcadamente mais baixos no tecido tumoral do que no cólon saudável adjacente. Quando os cientistas reduziram ACADS em células de câncer de cólon de camundongo, os tumores cresceram mais rápido e de forma mais agressiva; aumentar ACADS retardou o crescimento tumoral. Camundongos geneticamente modificados para não expressar ACADS especificamente no revestimento intestinal desenvolveram tumores maiores e em maior número em um modelo químico de câncer associado à colite, sustentando a ideia de que ACADS atua como supressor tumoral no intestino.
Como os tumores abafam os sinais de alarme imune
Esses efeitos sobre o crescimento não puderam ser explicados apenas pela velocidade de multiplicação das células tumorais em cultura, que mudou pouco. Em vez disso, a perda de ACADS impulsionou o crescimento tumoral apenas em animais com sistema imune intacto, apontando para mudanças no microambiente tumoral. Análises de célula única de cânceres colorretais humanos mostraram que tumores com baixa expressão de ACADS foram cercados por mais células tumorais e células imunes supressoras — como células supressoras derivadas da linhagem mieloide, certos macrófagos e células T reguladoras — e por menos células T efetoras e células natural killer. Esse padrão aponta para um “vizinhança imunossupressora” que protege o câncer do ataque. 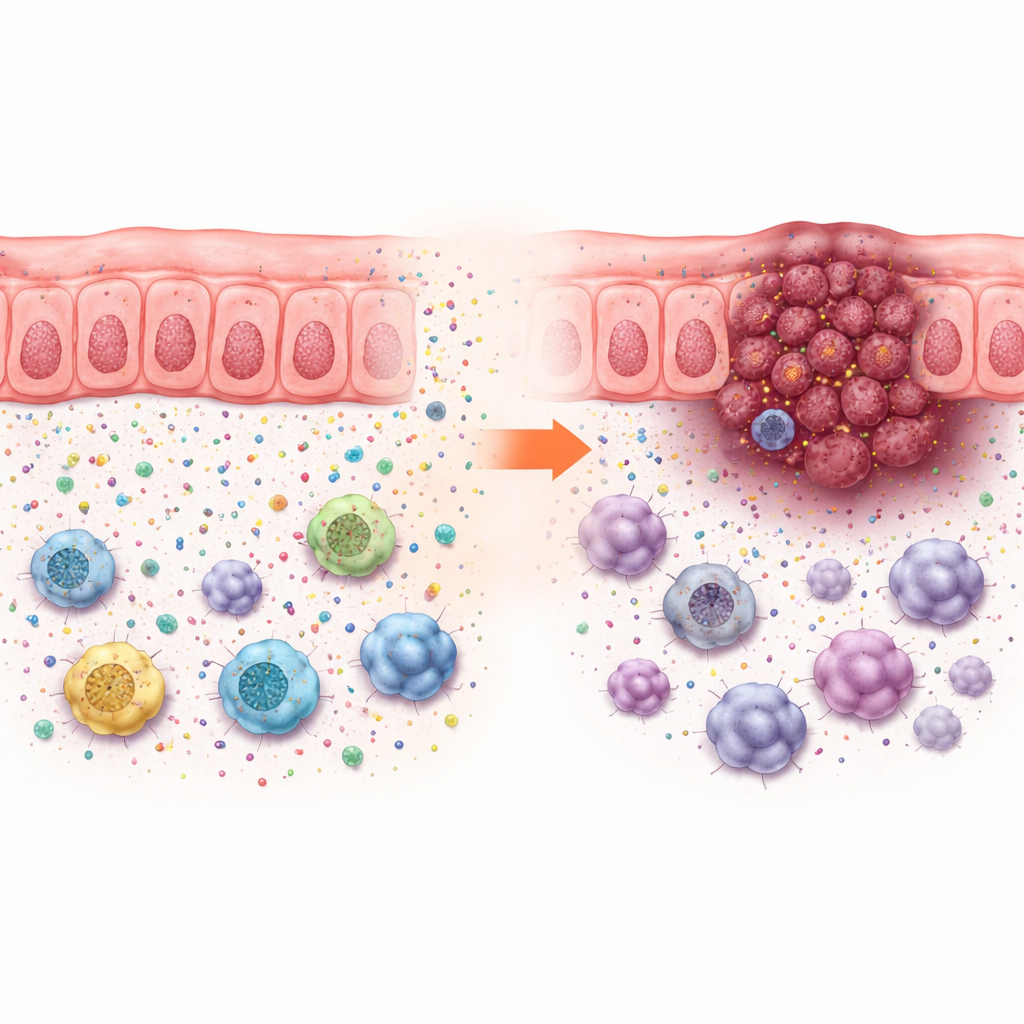
O vazamento de DNA mitocondrial como gatilho oculto
O que conecta uma enzima de queima de gordura a um sensor imune de DNA? A resposta está no DNA mitocondrial (mtDNA). Sob estresse, fragmentos de mtDNA podem vazar das mitocôndrias para o fluido citosólico da célula, onde o cGAS os detecta como sinal de perigo. Os pesquisadores mostraram que células cancerosas deficientes em ACADS tinham menos mtDNA nesse compartimento, embora o mtDNA total permanecesse inalterado. Bloquear o vazamento de mtDNA em células com altos níveis de ACADS desligou a via cGAS–STING, confirmando que esses fragmentos de DNA escapados são o alarme crítico. Surpreendentemente, fatores clássicos de estresse mitocondrial, como espécies reativas de oxigênio, picos de cálcio e mudanças marcantes na morfologia mitocondrial, não explicaram totalmente a diferença. Em vez disso, o estudo aponta para os “portões” na membrana mitocondrial e, mais importante, para as marcas químicas no próprio mtDNA. 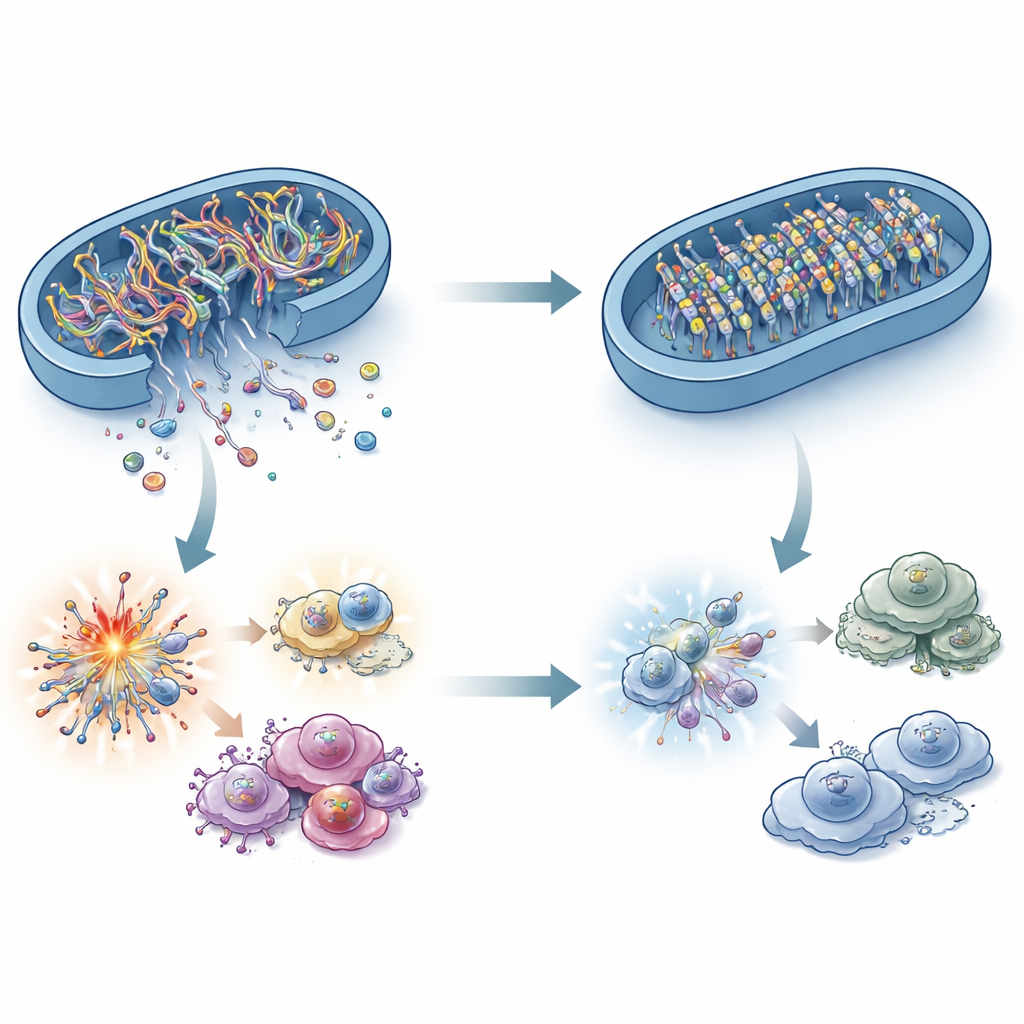
Um parceiro metilador de DNA que tranca o alarme por dentro
Através de triagens de interação proteica, verificou‑se que ACADS se associa a uma forma da enzima metiladora de DNA DNMT1 que se localiza nas mitocôndrias. Quando ACADS foi perdida, essa DNMT1 mitocondrial se acumulou, adicionando grupos metil extras ao mtDNA. Essas marcas tornam o mtDNA mais estável e menos propenso a rompimento e vazamento. Sobrecarregar células com DNMT1 mitocondrial reduziu a fuga de mtDNA, abafou a sinalização cGAS–STING e acelerou o crescimento tumoral, enquanto bloquear a DNMT1 com o fármaco decitabina restaurou o vazamento de mtDNA e retardou tumores deficientes em ACADS. Amostras de pacientes refletiram essas descobertas: baixa expressão de ACADS alinhou‑se com alta DNMT1 mitocondrial, sinalização STING mais fraca, menos células T efetoras, mais células imunes supressoras e uma previsão de resposta pior a imunoterapias de bloqueio de pontos de controle.
Reacordando as defesas imunes com um composto antigo
Para verificar se essa via poderia ser explorada terapeuticamente, os pesquisadores usaram triagem computacional para procurar moléculas que se liguem à ACADS. Eles identificaram a hipericina, um pigmento natural anteriormente testado como tratamento ativado por luz para certos linfomas cutâneos. Em células de câncer colorretal, a hipericina aumentou os níveis de ACADS, reduziu a DNMT1 mitocondrial, aumentou o vazamento de mtDNA e reativou a sinalização cGAS–STING — alterações que dependiam da presença de ACADS. Em modelos murinos de tumor e em culturas de curta duração de tumores colorretais humanos, o tratamento com hipericina reduziu os tumores ou deslocou as células imunes para um estado mais ativo, rico em células T. Embora sejam necessários mais estudos antes do uso clínico, esses resultados sugerem que “religar” farmacologicamente a ACADS pode ajudar a converter um tumor frio e imunossuprimido em outro que responda melhor à imunoterapia.
O que isso significa para pacientes e tratamentos futuros
Em termos práticos, este trabalho mostra que alguns cânceres colorretais crescem em parte porque silenciam uma enzima mitocondrial que normalmente facilita o vazamento de pequenos fragmentos de DNA para o interior da célula, onde atuam como sinalizadores para convocar o sistema imune. Ao permitir que um parceiro metilador de DNA trave esse DNA mitocondrial no lugar, tumores deficientes em ACADS mantêm esses sinais escondidos e evitam a detecção imune. Restaurar a atividade de ACADS, por exemplo com fármacos semelhantes à hipericina, poderia reabrir esse sistema de alarme mitocondrial, fortalecer a imunidade antitumoral e melhorar as respostas às imunoterapias existentes. ACADS, DNMT1 mitocondrial e a atividade da via STING podem, portanto, servir como biomarcadores e alvos úteis na busca por tratamentos mais eficazes para o câncer colorretal.
Citação: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
Palavras-chave: câncer colorretal, imunidade tumoral, DNA mitocondrial, metabolismo lipídico, via cGAS-STING