Clear Sky Science · pt
Mirando o fused in sarcoma (FUS): uma nova estratégia antisense para tratar a fibrose pulmonar idiopática
Por que os pulmões cicatrizados importam
A fibrose pulmonar idiopática (FPi) é uma doença pulmonar implacável em que os delicados alvéolos gradualmente se transformam em tecido cicatricial rígido, tornando cada respiração mais difícil. Os medicamentos atuais conseguem desacelerar esse processo, mas não podem detê‑lo ou revertê‑lo. Este estudo explora um novo alvo chamado FUS, uma proteína que ajuda as células a manipular suas mensagens genéticas, e testa se desligá‑la com uma cadeia desenhada de material semelhante ao DNA poderia acalmar o processo de cicatrização e ajudar pulmões danificados a se reparar.
Um controlador de tráfego celular que deu errado
FUS é uma proteína que normalmente vive no núcleo da célula, onde ajuda a gerenciar como o RNA — a cópia funcional de nossos genes — é processado e usado. Em doenças cerebrais como a ELA, FUS pode se comportar mal, saindo do núcleo, agregando‑se nas regiões externas da célula e perturbando a função celular normal. Os autores perguntaram se um comportamento semelhante poderia impulsionar a formação de cicatrizes na FPi. Eles estudaram fibroblastos pulmonares — as células do tecido conjuntivo que depositam material cicatricial — de pacientes com FPi e de doadores saudáveis. Nas células de FPi, os níveis de FUS eram maiores no geral e, crucialmente, havia muito mais FUS no citoplasma do que em células saudáveis. Usando microscopia eletrônica de alta resolução, eles confirmaram que essa proteína estava anormalmente abundante fora do núcleo, sugerindo que seu controle normal sobre o RNA poderia estar distorcido em pulmões fibróticos. 
Como o FUS alimenta as células cicatriciais
Para entender o que essa proteína desregulada realmente faz, os pesquisadores aumentaram o FUS em fibroblastos saudáveis e o reduziram em fibroblastos de FPi. FUS em excesso levou células saudáveis a se dividir mais rapidamente, enquanto reduzir FUS nas células de FPi desacelerou seu crescimento e movimento — dois comportamentos centrais para a formação de cicatrizes. A equipe então usou uma técnica que “congela” parceiras proteína–RNA no lugar e lê quais RNAs estão ligados ao FUS. Em fibroblastos de FPi, o FUS estava ligado a muitas mensagens genéticas que promovem fibrose, incluindo aquelas que codificam colágeno, fatores de crescimento como TGF‑β e sinais inflamatórios. Em outras palavras, FUS atuava como um hub conectando toda uma rede de mensagens pró‑cicatrização.
Silenciando o sinal com um fármaco de precisão
O estudo testou um oligonucleotídeo antisenso chamado ION363 — uma curta cadeia quimicamente modificada projetada para se ligar ao RNA de FUS e desencadear sua destruição. Quando fibroblastos de FPi foram tratados com ION363, os níveis de FUS caíram, as células desaceleraram sua proliferação e migração, e genes-chave na construção da cicatriz foram silenciados. Importante, esse efeito não dependia de matar as células nem forçá‑las à senescência; em vez disso, parecia redefinir seu comportamento. Quando o mesmo tratamento foi aplicado a fatias finas de tecido pulmonar de FPi mantidas vivas em laboratório, grandes grupos de genes ligados à matriz extracelular, inflamação e revestimento epitelial anormal foram atenuados, enquanto genes associados à produção saudável de surfactante e à função alveolar foram potenciados. O tratamento também reduziu a coloração para colágeno e aumentou marcadores de células de superfície pulmonar funcionais, sugerindo uma mudança da cicatrização em direção ao reparo.
Ajuda para o re crescimento dos alvéolos danificados
Como as pequenas células que revestem os alvéolos, conhecidas como células alveolares tipo II, são cruciais para o reparo pulmonar, os pesquisadores construíram “alveolosferas” tridimensionais a partir de células de pacientes para imitar unidades pulmonares em miniatura. Em culturas de pacientes com FPi, essas estruturas normalmente sobrevivem pouco. Com o tratamento com ION363, mais alveolosferas se formaram, cresceram mais e mostraram maior atividade lisossomal — uma marca de renovação ativa. Colorações detalhadas revelaram mais células com marcadores de células maduras trocadoras de gás, indicando que silenciar o FUS não apenas acalmou os fibroblastos, mas também encorajou o epitélio lesionado a reconstruir uma superfície mais saudável. 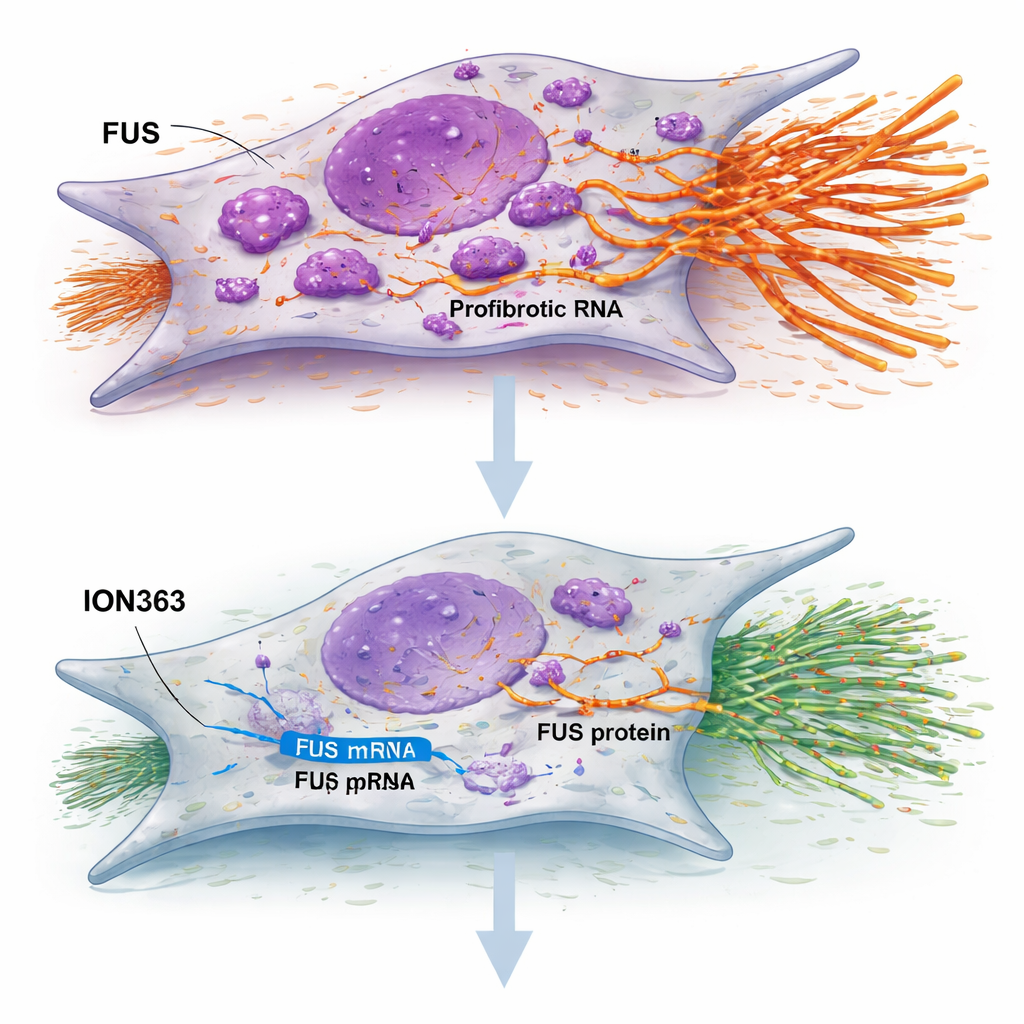
O que isso pode significar para os pacientes
Em conjunto, o trabalho pinta o FUS como um interruptor mestre na FPi que liga fibroblastos superativos formadores de cicatriz ao fracasso do reparo dos delicados alvéolos. Ao reduzir o FUS com um fármaco antisenso direcionado, os pesquisadores puderam diminuir programas genéticos profibróticos, aliviar o acúmulo de colágeno e promover a regeneração em modelos pulmonares derivados de pacientes. Embora essa abordagem ainda esteja em estágio de laboratório e exija testes cuidadosos em modelos animais e ensaios clínicos, sugere que a FPi um dia possa ser tratada não apenas desacelerando a cicatrização, mas reequilibrando diretamente os programas celulares que controlam lesão e reparo pulmonar.
Citação: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
Palavras-chave: fibrose pulmonar idiopática, oligonucleotídeo antisenso, proteína FUS, fibrose pulmonar, reparo alveolar