Clear Sky Science · pt
Truncação parcial do domínio C-terminal de PTCH1 no câncer promove tumorigenese por ativação não canônica de um circuito GLI-PI3K
Por que uma pequena alteração na proteína importa no câncer de cólon
O câncer de cólon geralmente surge de um acúmulo lento de falhas genéticas. Este estudo focaliza uma alteração surpreendentemente pequena numa proteína de superfície celular chamada PTCH1 e mostra como remover parte de sua “cauda” pode ajudar células de câncer de cólon a crescer mais rápido, disseminar-se com mais facilidade e possivelmente resistir a alguns medicamentos atuais. Entender esse interruptor de crescimento oculto pode abrir caminho para tratamentos novos e mais precisos para um subconjunto de pacientes.
O guardião celular com uma função oculta
PTCH1 é mais conhecido como o guardião da via Hedgehog, uma via de comunicação que as células usam durante o desenvolvimento e a reparação tecidual. Em seu papel clássico, PTCH1 mantém sob controle uma proteína parceira, Smoothened, e assim regula uma família de controladores do DNA chamados GLI. Mas PTCH1 também tem uma longa cauda flexível que fica dentro da célula, atuando como uma faixa de ancoragem para outras proteínas que influenciam morte celular, reciclagem de componentes celulares e mais. Trabalhos anteriores mostraram que alguns cânceres do cólon, do estômago e do útero carregam mutações que cortam parte dessa cauda interna. Essas mutações não pareciam romper o interruptor clássico de Hedgehog, mas tornaram as células cancerosas melhores em sobreviver ao estresse, sugerindo que esse segmento da cauda contribui silenciosamente para o papel supressor de tumor de PTCH1.
Modelando células cancerosas para testar o impacto
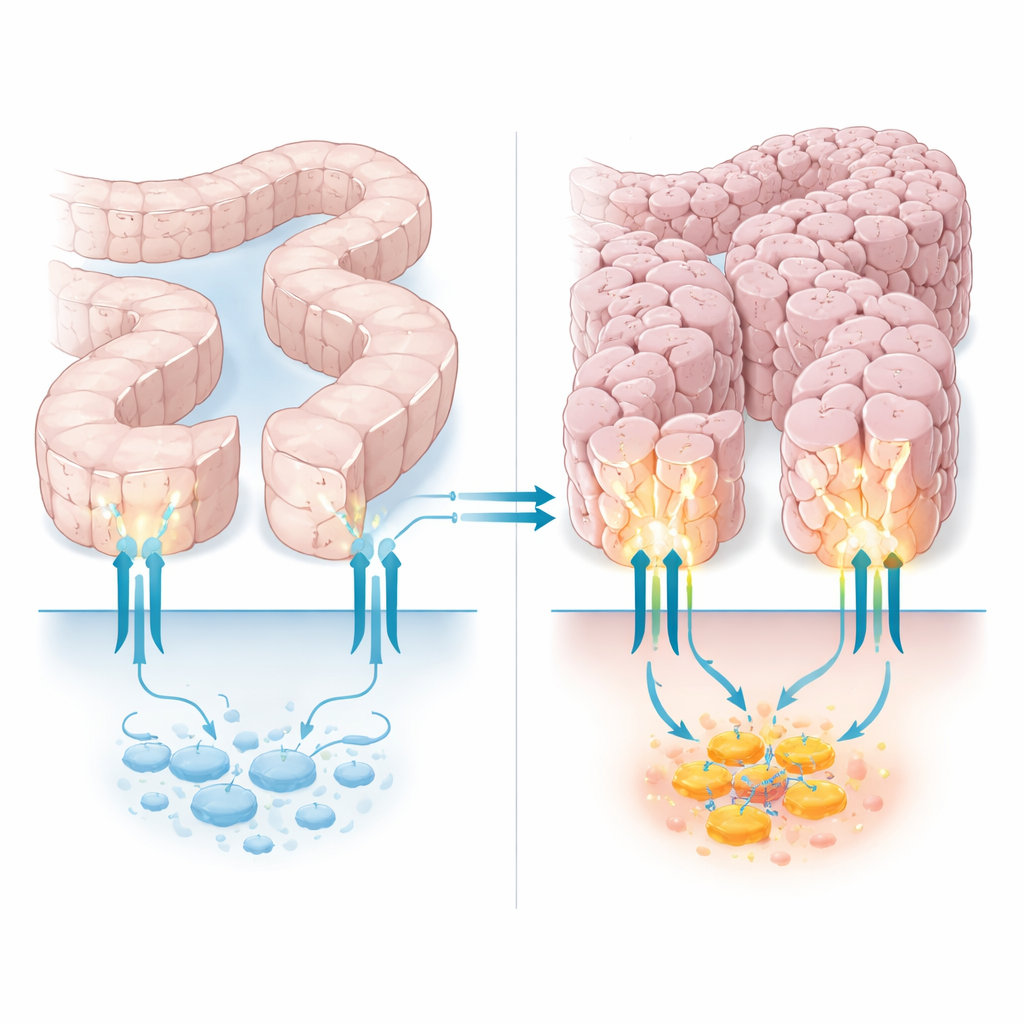
Para ver o que essas mutações de encurtamento da cauda realmente fazem, os pesquisadores usaram edição gênica CRISPR/Cas9 para recriá‑las em uma linhagem de câncer de cólon. Eles compararam dois clones editados, cada um com uma truncação diferente na cauda de PTCH1, com células idênticas que carregavam PTCH1 normal. As células mutantes se dividiram mais rápido, formaram muito mais colônias e prosperaram mesmo quando tiveram que crescer sem anexo — um comportamento ligado à capacidade de se espalhar pelo organismo. Quando implantadas em camundongos, as células com a cauda truncada produziram tumores muito maiores em poucas semanas, com mais células em processo de divisão. Importante: as células editadas ainda produziam PTCH1 e mantinham sua função principal de guarda, mostrando que a agressividade extra vem da perda das funções internas especializadas da cauda, e não de remover o PTCH1 completamente.
Um atalho surpreendente para um potente interruptor de crescimento
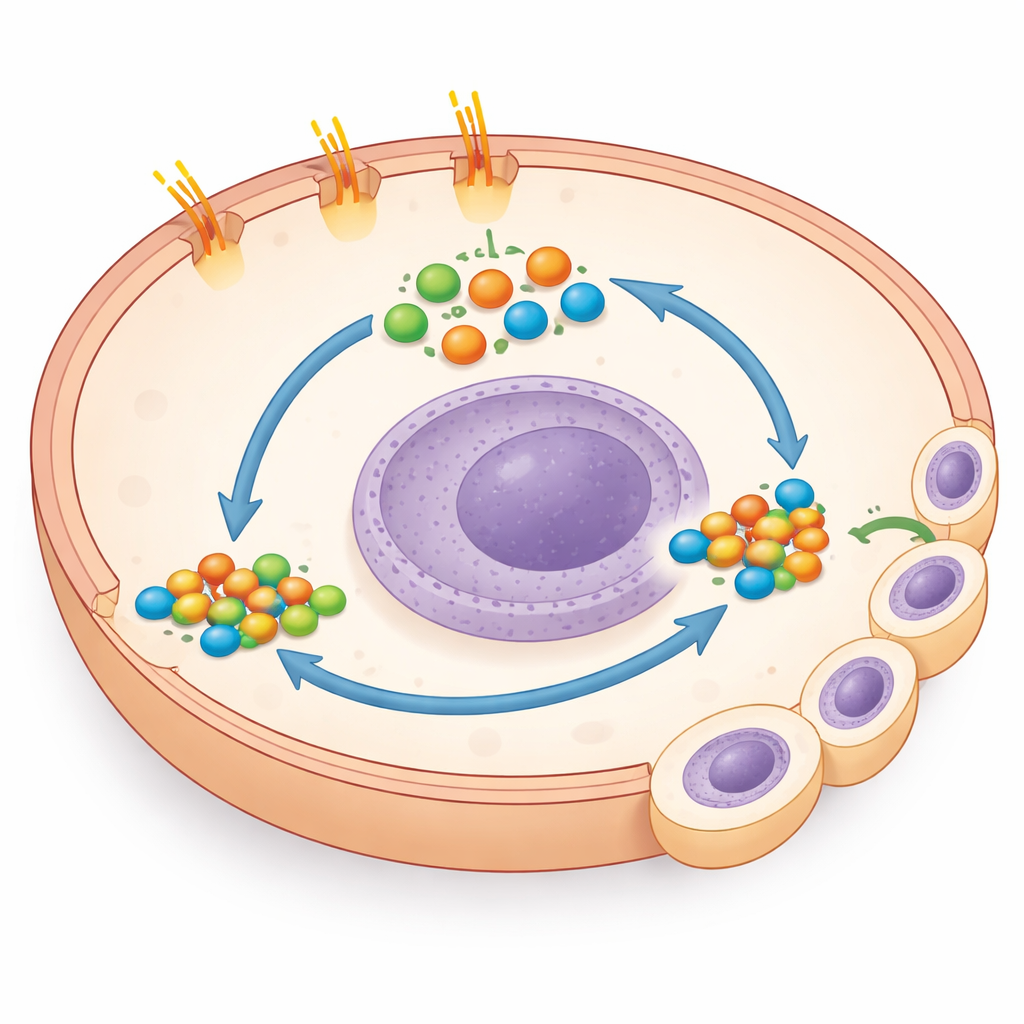
Ao investigar a biologia subjacente, a equipe fez uma descoberta inesperada: as células com a cauda truncada apresentaram níveis muito aumentados de GLI1 e GLI2, motores-chave de programas gênicos que promovem crescimento e sobrevivência. Normalmente, a atividade de GLI aumenta quando Smoothened é liberado, mas bloquear Smoothened não teve efeito aqui. Em vez disso, bloquear GLI diretamente com uma pequena molécula, ou reduzir GLI1 com ferramentas genéticas, diminuiu drasticamente o crescimento das células mutantes em placas e em outras linhagens de câncer de cólon que naturalmente carregam mutações na cauda de PTCH1. Isso mostrou que a perda da cauda ativa GLI por uma via “não canônica” que contorna o interruptor usual de Hedgehog, e que as células cancerosas passam a depender fortemente desse atalho para seu comportamento agressivo.
Múltiplos circuitos de crescimento se acendem, mas um ciclo domina
Ao sequenciar o RNA das células, os pesquisadores encontraram milhares de genes cuja atividade mudou quando a cauda de PTCH1 foi truncada. Muitos pertenciam a circuitos de câncer bem conhecidos, incluindo aqueles controlados pelo receptor do fator de crescimento epidérmico (EGFR), Ras, e sistemas de sinalização que regulam metabolismo celular e propriedades semelhantes a células-tronco. As células mutantes mostraram atividade aumentada de EGFR e seus ligantes e maior atividade em duas rotas principais a jusante: as vias MAPK e PI3K/Akt. Ainda assim, quando os cientistas bloquearam EGFR ou seu braço MAPK, as células mutantes só foram parcialmente desaceleradas. Em contraste, baixas doses de inibidores de PI3K restringiram fortemente seu crescimento e formação de colônias e reduziram os níveis de GLI1, destacando PI3K/Akt como um parceiro crítico nesse novo mecanismo de ativação de GLI.
Um ciclo autorreforçador que alimenta o crescimento tumoral
Experimentos adicionais revelaram um ciclo de feedback: truncar a cauda de PTCH1 aumenta a atividade de GLI; GLI, por sua vez, ajuda a manter a sinalização PI3K/Akt elevada; e PI3K/Akt ajuda a estabilizar e ativar GLI. Interromper GLI ou PI3K quebrou esse ciclo e tirou das células mutantes sua vantagem de crescimento, enquanto simplesmente ativar PI3K/Akt não foi suficiente para vencer um bloqueio direto de GLI. As células também apresentaram atividade reduzida de PKA, uma enzima que normalmente marca as proteínas GLI para inativação, o que provavelmente inclina ainda mais a balança em favor dos programas dirigidos por GLI.
O que isso pode significar para tratamentos futuros
Para os pacientes, a mensagem-chave é que alguns cânceres de cólon carregam mutações na cauda de PTCH1 que silenciosamente conectam um circuito de feedback positivo GLI–PI3K, ajudando tumores a crescer e a escapar de drogas que miram o interruptor Hedgehog mais familiar ou a via EGFR–MAPK. Esses tumores podem ser especialmente vulneráveis a tratamentos que inibam GLI diretamente ou atinjam PI3K/Akt. O trabalho sugere que sequenciar PTCH1 em tumores de cólon — especialmente aqueles do lado direito do cólon, onde tais mutações são mais frequentes — pode ajudar a identificar pacientes que poderiam se beneficiar de estratégias direcionadas a PI3K ou GLI, transformando um corte sutil na proteína em uma pista terapêutica útil.
Citação: Caballero-Ruiz, B., Bordone, R., Coni, S. et al. Partial truncation of the C-terminal domain of PTCH1 in cancer promotes tumourigenesis by non-canonical activation of a GLI-PI3K loop. Oncogene 45, 1013–1025 (2026). https://doi.org/10.1038/s41388-026-03698-9
Palavras-chave: câncer de cólon, sinalização Hedgehog, mutações em PTCH1, fatores de transcrição GLI, via PI3K Akt