Clear Sky Science · pl
Wnikliwe spojrzenie na heterogeniczność trofoblastu i adaptacyjną dysfunkcję w selektywnym zahamowaniu wzrostu płodu
Kiedy jeden z bliźniąt pozostaje w tyle
Dla rodziców oczekujących bliźniąt bardzo niepokojące może być, gdy jedno dziecko przestaje rosnąć tak dobrze jak drugie, mimo że dzielą ten sam macicę i łożysko. Ten stan, nazywany selektywnym zahamowaniem wzrostu płodu, nie tylko zagraża zdrowiu mniejszego bliźniaka przed narodzinami, ale może też wpłynąć na długoterminowy rozwój. W badaniu użyto nowoczesnej analizy pojedynczych komórek, aby zajrzeć do wspólnego łożyska takich ciąż bliźniaczych i ukazać, jak drobne zmiany w określonych komórkach łożyska i odpowiedziach immunologicznych mogą przechylić równowagę między zdrowym wzrostem a niebezpiecznym niedoborem.
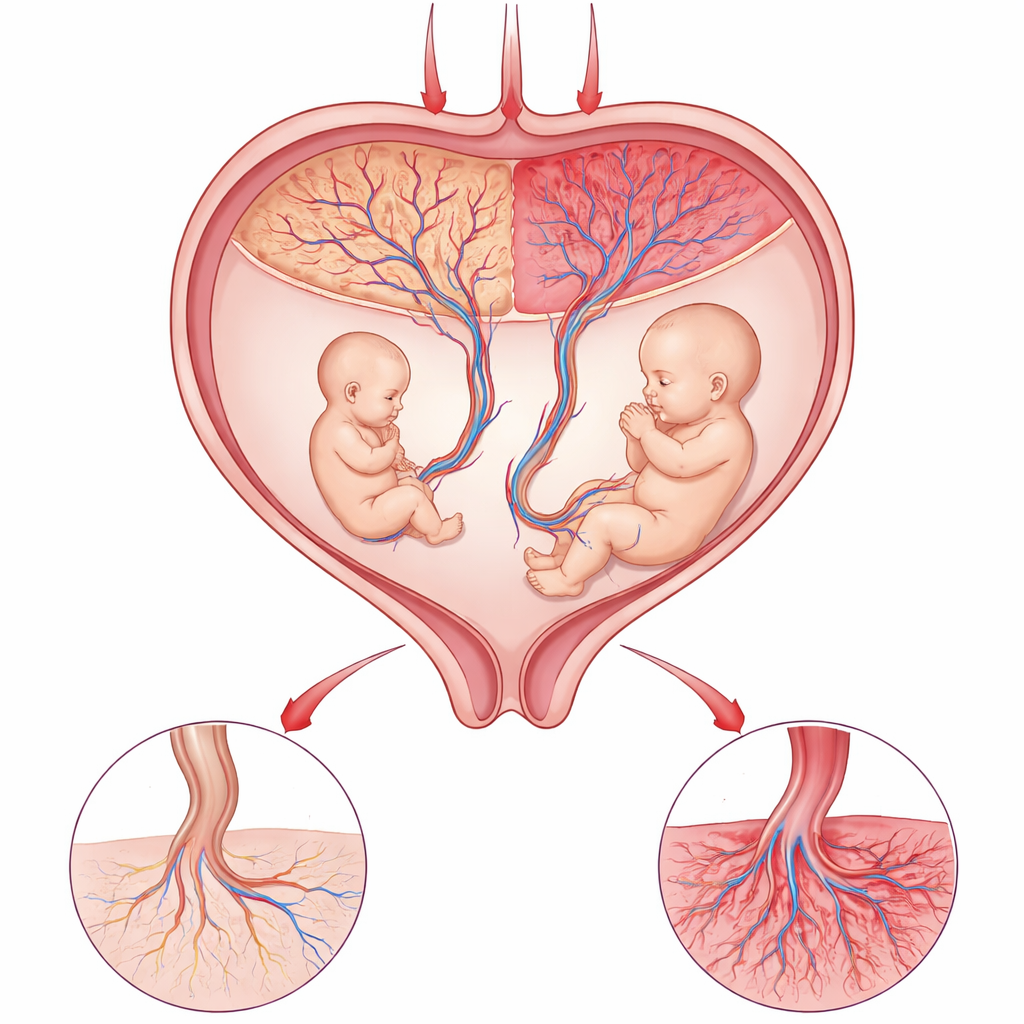
Delikatna równowaga łożyska
Łożysko jest nicią życia między matką a dzieckiem, dostarczając tlen i składniki odżywcze oraz usuwając odpady. W niektórych ciążach bliźniaczych jednokosmówkowych oboje płody dzielą jedno łożysko, ale zajmują różne jego obszary. Gdy jedno z bliźniąt staje się znacznie mniejsze od drugiego, lekarze wiedzą, że lokalnie w tym wspólnym organie coś poszło nie tak. Ponieważ bliźnięta mają tę samą matkę i niemal identyczny genom, stanowią silny eksperyment naturalny: wszelkie istotne różnice we wzroście prawdopodobnie wynikają z funkcjonowania odpowiadających im części łożyska, a nie z różnic między samymi płodami.
Przybliżenie do pojedynczych komórek łożyska
Naukowcy pobrali próbki łożyska z trzech ciąż, w których jedno z bliźniąt było wyraźnie mniejsze od drugiego. Przy użyciu sekwencjonowania RNA pojedynczych komórek — metody odczytującej aktywność tysięcy genów w pojedynczych komórkach — przeanalizowali ponad 175 000 komórek z różnych regionów łożyska. Pozwoliło im to sklasyfikować komórki na odrębne typy, w tym komórki podporowe, komórki naczyniowe i kilka rodzajów komórek układu odpornościowego. Skoncentrowali się na kluczowej grupie zwanej kosmówkowymi cytotrofoblastami, warstwie komórek wyściełającej maleńkie palczaste wypustki, gdzie krew matki styka się z krążeniem płodowym, oraz która stale odnawia i naprawia powierzchnię łożyska.
Dwa kluczowe stany komórek: struktura kontra tryb przetrwania
W obrębie tych kosmówkowatych cytotrofoblastów zespół odkrył dwa główne stany o bardzo różnych rolach. Jedna grupa, oznaczona cząsteczką TP63, działała jak strukturalni opiekunowie: wspierała barierę między matką a dzieckiem, utrzymywała połączenia międzykomórkowe i pomagała zachować organizację tkanki. Druga grupa, oznaczona enzymem LDHA, była nastawiona na intensywną produkcję energii i radzenie sobie ze stresem, z nasileniem szlaków związanych z mitochondriami, stresem oksydacyjnym i kontrolą jakości białek. W obszarach łożyska przynależnych do mniejszych bliźniąt komórki ochronne TP63 były wyczerpane, podczas gdy komórki napędzane stresem typu LDHA rozrosły się i były bardziej aktywne cyklicznie. Analiza „trajektorii” oparta na komputerowych modelach sugerowała, że komórki są popychane wzdłuż ścieżki od zdrowych, strukturalnych ról w kierunku trybu przetrwania, z mniejszą liczbą komórek osiągających w pełni zlane/stabilne stany, które normalnie utrzymują gładką, wydajną powierzchnię wymiany.
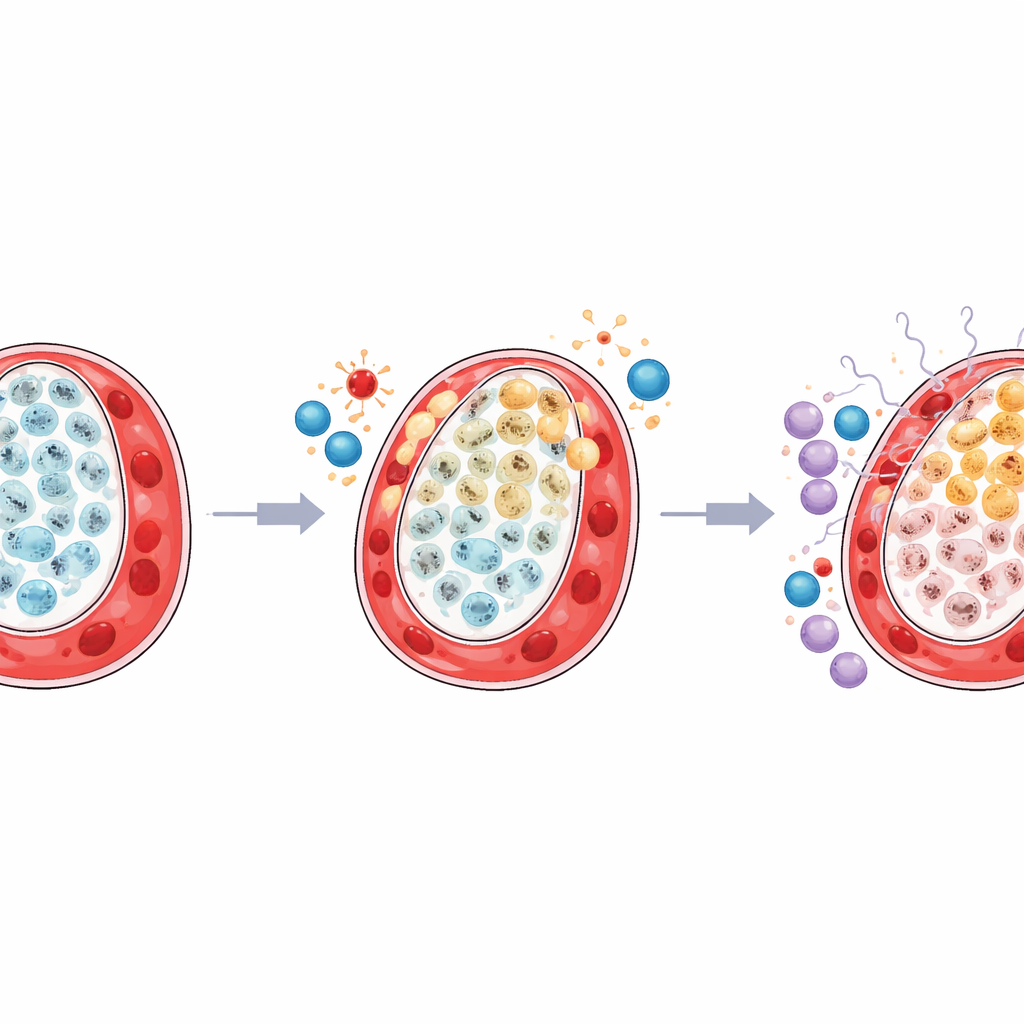
Zapalone sąsiedztwo wokół zestresowanych komórek
Badanie wykazało również, że otaczające środowisko immunologiczne w obszarze łożyska mniejszego bliźniaka zostało przekształcone w sposób szkodliwy. Pomocny rodzaj makrofagów rezydujących, znanych jako komórki Hofbauera, które zwykle wspierają zdrowie tkanki i zarządzanie metabolizmem, był zmniejszony. Jednocześnie pewne komórki NK (natural killers), przygotowane do odpowiedzi przeciwwirusowej i zapalnej, stały się bardziej liczne i bardziej aktywne. Szczegółowe mapowanie sygnałów przekazywanych między komórkami wykazało, że zestresowane trofoblasty typu LDHA nawiązywały silniejsze interakcje z komórkami odpornościowymi poprzez szlaki napędzane interferonami i pokrewnymi cząsteczkami alarmowymi. Tymczasem komunikacja między strukturalnymi komórkami TP63 a wspierającymi komórkami zrębu i naczyniowymi osłabła, co sugeruje utratę zarówno fizycznego wsparcia, jak i łagodnej regulacji immunologicznej.
Trójstronny rozkład, który ogranicza wzrost płodu
W sumie praca ta przedstawia jasny, przystępny obraz tego, co idzie nie tak w łożysku, gdy jedno z bliźniąt pozostaje w tyle. Komórki wspierające strukturę, które utrzymują powierzchnię wymiany zwartą i uporządkowaną, są wyczerpane; komórki obciążone stresem i żądne energii przejmują kontrolę; a układ odpornościowy przesuwa się w kierunku stanu bardziej zapalnego. Te trzy wątki — utrata struktury, przeciążenie metaboliczne i przewlekłe zapalenie — wzajemnie się wzmacniają i stopniowo osłabiają zdolność łożyska do dostarczania wystarczającej ilości tlenu i składników odżywczych mniejszemu dziecku. Wskazując na konkretne typy komórek i zaangażowane szlaki sygnalizacyjne, badanie dostarcza mapy drogowej dla przyszłych testów i terapii mających na celu wcześniejsze wykrywanie problemów łożyskowych i być może przywracanie tych komórek do zdrowszej równowagi.
Cytowanie: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
Słowa kluczowe: łożysko, ciąża bliźniacza, zahamowanie wzrostu płodu, sekwencjonowanie RNA pojedynczych komórek, komórki trofoblastu