Clear Sky Science · pl
Poprawa wydajności biosensora SPR do wykrywania kreatyniny za pomocą powłok z plazmowo polimeryzowanego heptylaminy
Dlaczego to ma znaczenie dla codziennego zdrowia
Problemy z nerkami często rozwijają się po cichu, a gdy pojawiają się objawy, szkody mogą być już znaczne. Lekarze polegają więc na małej cząsteczce odpadowej zwanej kreatyniną, mierzonej we krwi, jako wczesnym sygnale ostrzegawczym. Artykuł opisuje nowy sposób zwiększenia czułości optycznych biosensorów na kreatyninę, co może otworzyć drogę do szybszych i precyzyjniejszych badań nerek przy użyciu niewielkich, nadających się do wielokrotnego użytku chipów zamiast powolnych testów laboratoryjnych.
Przekształcanie światła w sygnał medyczny
Badanie koncentruje się na technologii zwanej rezonansem plazmonów powierzchniowych (SPR), która przekształca subtelne zmiany na powierzchni metalu w mierzalne przesunięcia w świetle odbitym. W tych sensorach cienka warstwa złota jest przyłączona do szklanego pryzmatu i oświetlana laserem pod określonym kątem. Gdy cząsteczki wiążą się z powierzchnią złota, nieznacznie zmieniają zachowanie światła, powodując przesunięcie kąta minimalnego odbicia. Śledząc ten kąt, sensor może „widzieć”, kiedy i w jakiej ilości dociera docelowa substancja na powierzchnię, i to bez stosowania barwników czy znaczników, w czasie rzeczywistym.
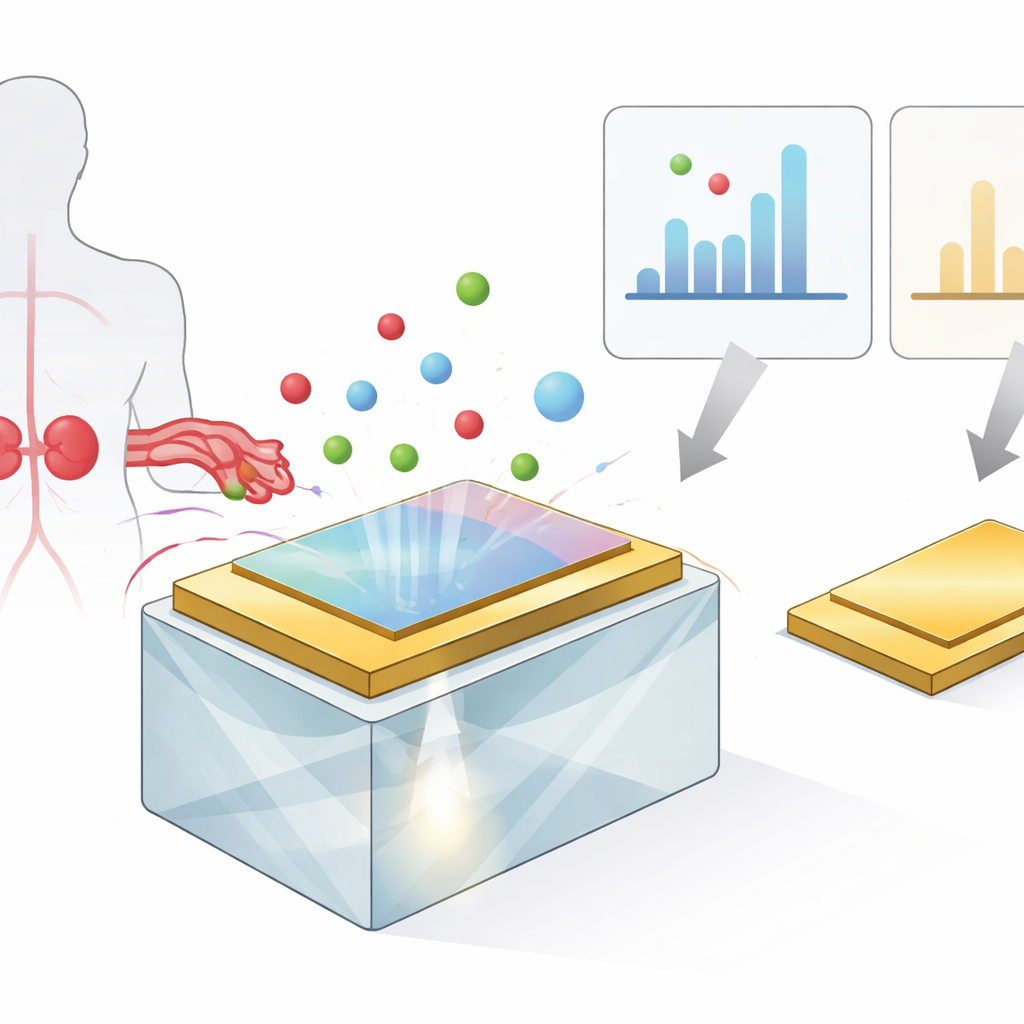
Uczynienie powierzchni sensora bardziej przyjazną
Aby ten sygnał oparty na świetle był silny i wiarygodny, powierzchnia złota musi być starannie przygotowana, tak aby biomolekuły przyczepiały się tam, gdzie powinny, i unikały zlepiania tam, gdzie nie powinny. Naukowcy skupili się na właściwości zwanej zwilżalnością – w praktyce tym, jak łatwo woda rozlewa się po powierzchni – którą mierzyli za pomocą kąta zwilżania wodą. Niski kąt oznacza, że woda się rozlewa (powierzchnia bardziej przyjazna, hydrofilowa), natomiast wysoki kąt oznacza formowanie się kropli (powierzchnia bardziej hydrofobowa). Przy użyciu procesu znanego jako polimeryzacja plazmowa pokryli złoto ultracienką warstwą wykonaną ze związku zwanego heptylaminą. Poprzez regulację mocy plazmy byli w stanie dostroić, jak hydrofilowa lub hydrofobowa stanie się powłoka.
Znajdowanie optymalnego punktu czułości
Zespół systematycznie zmieniał moc plazmy od niskiej do wysokiej i obserwował, jak wpływa to na kąt zwilżania, grubość powłoki i odpowiedź świetlną sensora. Przy niższych mocach powierzchnia pozostawała bardziej hydrofilowa, co sprzyjało równomiernemu rozprowadzaniu cieczy i lepszemu przyłączaniu biomolekuł. Przy wyższych mocach powierzchnia stopniowo przechodziła w zachowanie hydrofobowe, a struktura powłoki ulegała dalszym zmianom. Mikroskopia sił atomowych wykazała, że warstwa wytworzona w plazmie dodaje pewną chropowatość w skali nanometrów, lecz pozostaje w zakresie akceptowalnym dla precyzyjnego pomiaru optycznego. Porównując krzywe odbicia światła dla różnych powłok, badacze wyznaczyli optymalną powłokę wykonaną przy umiarkowanej mocy plazmy, o kącie zwilżania około 60 stopni i cienkiej, dobrze kontrolowanej warstwie.
Budowanie lepszego testu na kreatyninę
Po dostrojeniu powierzchni autorzy zbudowali działający biosensor kreatyniny. Najpierw aktywowali powłokę z heptylaminy za pomocą powszechnie stosowanego sieciującego odczynnika, a następnie przyłączyli enzymy zwane kreatyninazą, które specyficznie rozpoznają i przetwarzają kreatyninę. Gdy przez chip przepływały roztwory przypominające krew zawierające różne poziomy kreatyniny, zdarzenia wiązania w warstwie enzymatycznej powodowały mierzalne przesunięcia kąta SPR. W zakresie klinicznie istotnym dla krwi, od 0,05 do 0,6 milimola na litr, powlekany sensor wykazywał wyraźną, niemal liniową odpowiedź, o czułości znacznie wyższej niż w przypadku gołej powierzchni złotej testowanej w podobnych warunkach. Eksperyment porównawczy wykazał, że niepowlekane złoto wykrywało kreatyninę tylko przy znacznie wyższych stężeniach i z dużo słabszymi sygnałami.
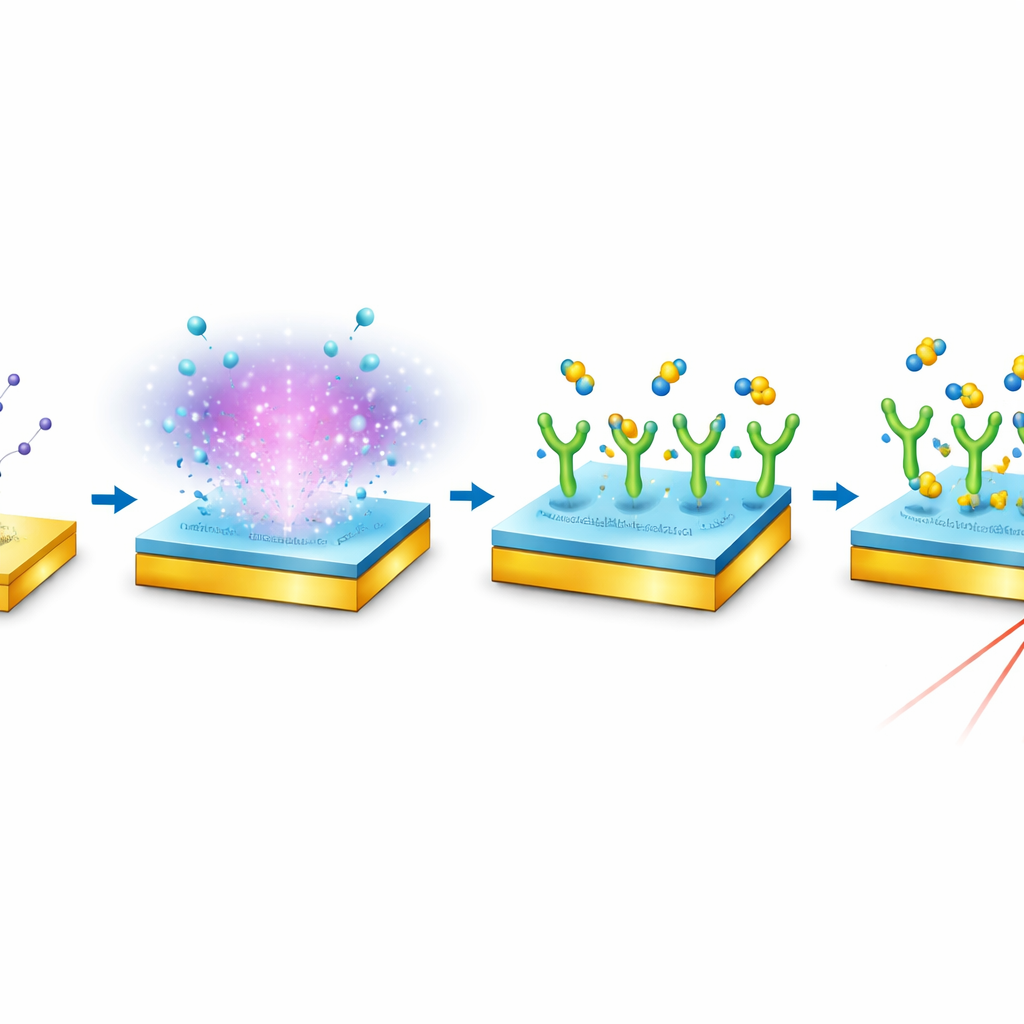
Co to oznacza dla przyszłej diagnostyki
Mówiąc prosto, badanie pokazuje, że staranne dostrojenie „przyjazności wodnej” powierzchni złotego sensora może dramatycznie zwiększyć jego zdolność do wychwytywania i mierzenia śladowych ilości ważnego produktu odpadowego nerek. Powłoka z heptylaminy wytwarzana w plazmie zapewnia właściwą równowagę: nieco obniża surową czułość optyczną gołego metalu, ale znacznie poprawia liczbę enzymów możliwych do przyłączenia i efektywność ich interakcji z kreatyniną. Efektem końcowym jest chip, który może czułe wykrywać medycznie istotne poziomy kreatyniny w czasie rzeczywistym, bez znaczników, oferując obiecującą ścieżkę do kompaktowych, o wysokiej wydajności monitorów stanu nerek. Przyszłe prace będą musiały sprawdzić, jak sensor radzi sobie z innymi substancjami we krwi i jak stabilny pozostaje w czasie, ale opisana strategia powierzchniowa może zostać zaadaptowana do wielu innych celów medycznych poza kreatyniną.
Cytowanie: Jamil, N.A., Fatah Yasin, M.F.H., Karim, I.M. et al. Enhancing SPR biosensor performance for creatinine detection via plasma polymerized heptylamine coatings. Sci Rep 16, 10658 (2026). https://doi.org/10.1038/s41598-026-46647-y
Słowa kluczowe: biosensor kreatyniny, funkcja nerek, rezonans plazmonów powierzchniowych, powłoka z polimeru plazmowego, diagnostyka medyczna