Clear Sky Science · pl
Kwantyfikacja mikronukleusów ze skanów całych preparatów hematologicznych za pomocą sztucznej inteligencji jako przekładalny biomarker farmakodynamiczny inhibitorów odpowiedzi na uszkodzenia DNA
Dlaczego maleńkie kropki we krwi mogą opowiadać wielkie historie
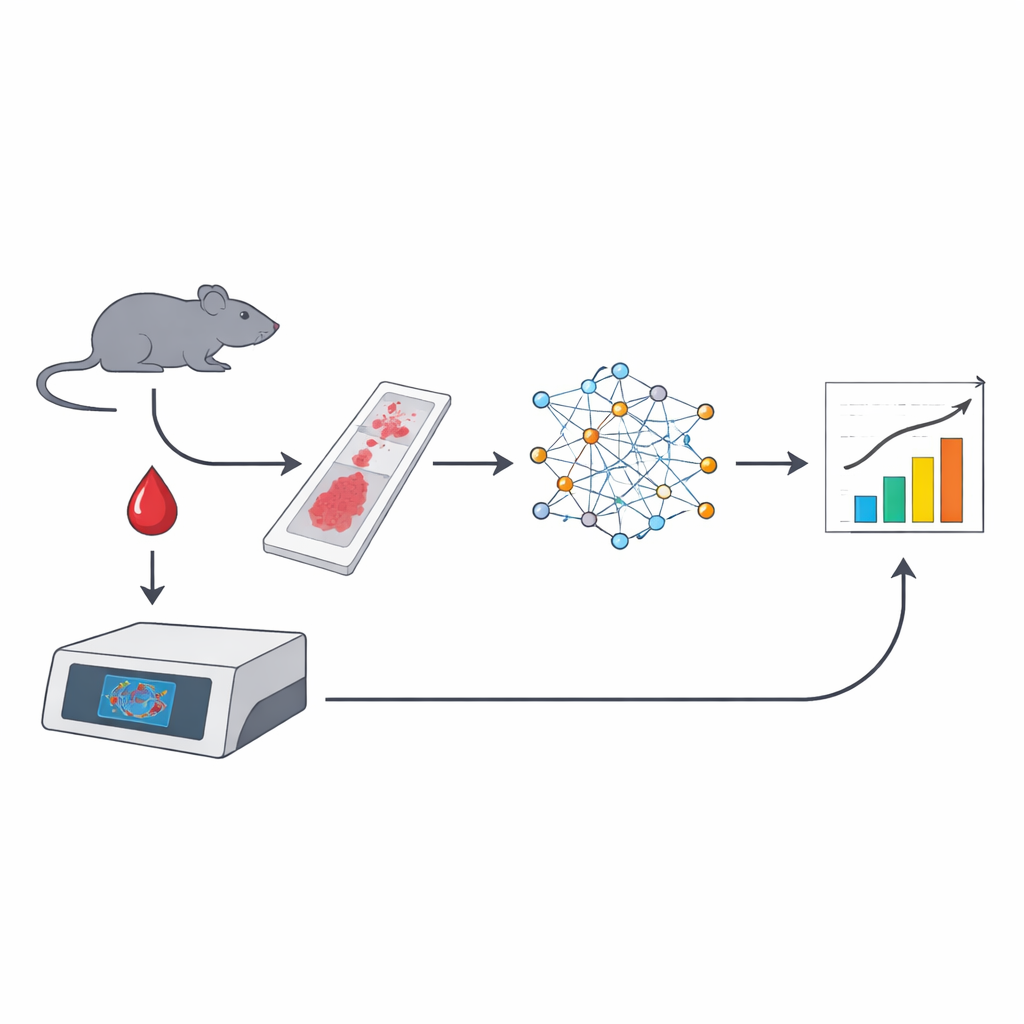
Lekarze i naukowcy nieustannie poszukują prostych sposobów, by sprawdzić, czy lek przeciwnowotworowy robi to, co powinien w organizmie. W tym badaniu pokazano, że drobne kropki w czerwonych krwinkach, zwane mikronukleusami, mogą działać jak naturalne markery uszkodzeń DNA wywoływanych przez niektóre terapie przeciwnowotworowe. Łącząc obrazowanie całych preparatów mikroskopowych z technikami sztucznej inteligencji (AI), badacze przekształcili kilka kropel krwi w bogaty, zautomatyzowany odczyt siły działania leków celujących w DNA.
Małe wyspy DNA w czerwonych krwinkach
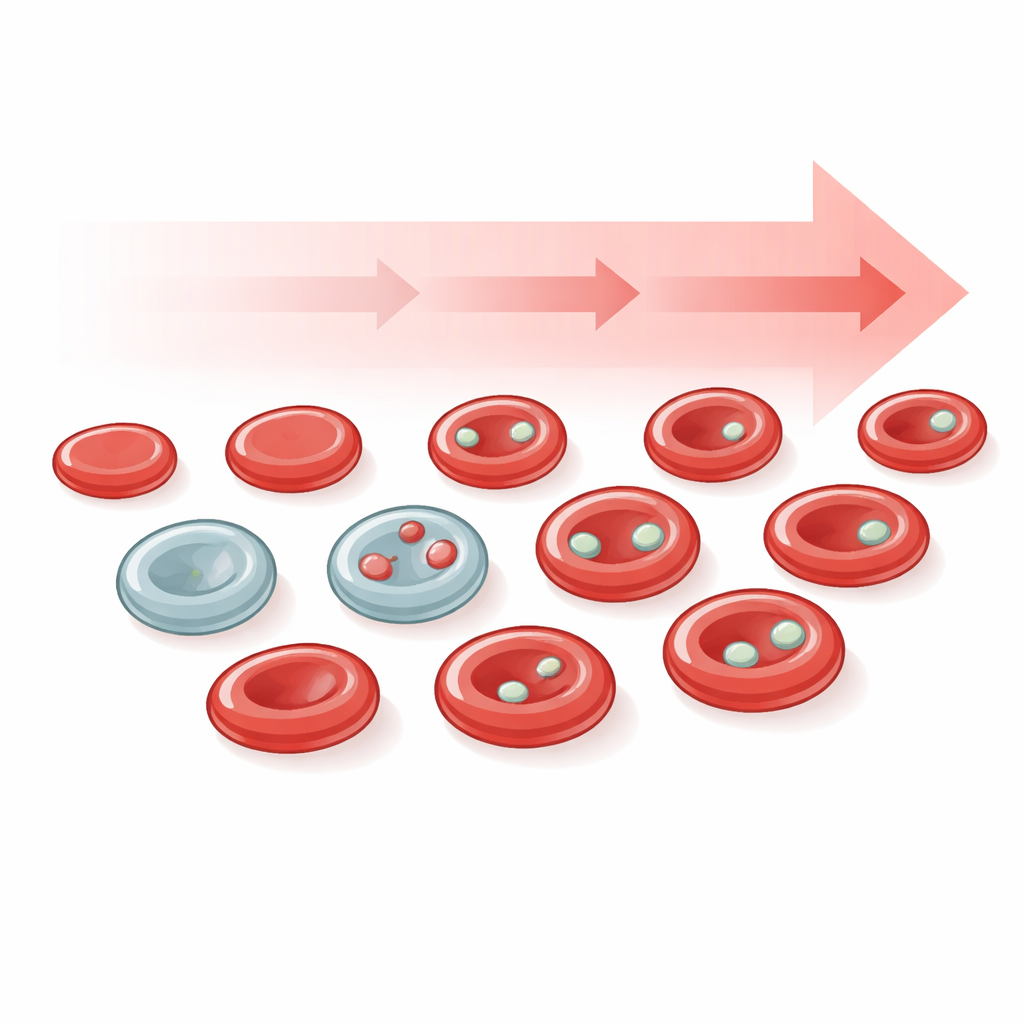
Mikronukleusy to drobne pęcherzyki zawierające DNA, które znajdują się poza głównym jądrem komórkowym. Powstają, gdy chromosomy pękają lub są nieprawidłowo segregowane podczas podziału komórki — zdarzenia powszechne w nowotworach i po ekspozycji na czynniki uszkadzające DNA. W większości tkanek wykrycie prawdziwych mikronukleusów pod mikroskopem jest trudne, ponieważ cienkie wycinki tkankowe mogą wprowadzać w błąd. Erytrocyty dają obejście tego problemu: podczas dojrzewania normalnie usuwają swoje główne jądro, ale wszelkie wcześniej powstałe mikronukleusy mogą pozostać jako drobne, dobrze zdefiniowane punkty. Te od dawna znane struktury, historycznie nazywane ciałkami Howell–Jolly’ego, są więc wygodnymi, autentycznymi mikronukleusami krążącymi we krwi i mogą ujawniać, ile uszkodzeń DNA miało miejsce w niedawnym czasie.
Przekształcanie rozmazów krwi w dane za pomocą AI
Zespół opracował zautomatyzowany proces rozpoczynający się od standardowych rozmazów krwi myszy, barwionych albo fluorescencyjnym barwnikiem DNA, albo powszechnymi barwnikami May–Grünwald–Giemsa stosowanymi w laboratoriach szpitalnych. Całe szkiełka skanowano w wysokiej rozdzielczości, a nadzorowane modele głębokiego uczenia uczono rozpoznawać erytrocyty, wykrywać mikronukleusy oraz odróżniać niedojrzałe retikulocyty od dojrzałych erytrocytów na podstawie subtelnych różnic w rozmiarze i kolorze. Z pojedynczego obrazu system mógł analizować ponad 100 000 komórek, wskazywać te z mikronukleusami, a nawet liczyć komórki zawierające więcej niż jeden mikronukleus — czego konwencjonalna cytometria przepływowa nie zawsze potrafi.
Łączenie drobnych zmian we krwi z siłą działania leku
Następnie badacze sprawdzili, czy częstość występowania erytrocytów z mikronukleusami koreluje z ekspozycją na chemioterapię uszkadzającą DNA oraz na leki blokujące odpowiedź na uszkodzenia DNA, takie jak inhibitory PARP. U myszy leczonych cisplatyną lub paklitakselem liczenia oparte na AI wychwyciły oczekiwane wzrosty liczby komórek z mikronukleusami. U myszy z guzami leczonych inhibitorami PARP — olaparibem lub saruparibem — wyższe dawki generowały większe wzrosty komórek z mikronukleusami i silniejsze kurczenie się guzów. Podczas kilku tygodni codziennego podawania małe, seryjne próbki krwi (tylko około 5 mikrolitrów każda) pozwalały śledzić, jak mikronukleusy powoli się kumulują, a następnie ustępują po zaprzestaniu leczenia. Porównanie metody opartej na skanach szkiełek ze standardową cytometrią przepływową wykazało bliskie zgranie obu podejść, co potwierdza, że nowy przepływ pracy jest zarówno dokładny, jak i odporny.
Skupienie na młodych krwinkach dla wyraźniejszych sygnałów
Ponieważ młode czerwone krwinki (retikulocyty) szczególnie często zawierają świeże mikronukleusy, badacze wyszkolili swoje algorytmy, by rozdzielały populację krwinek na komórki niedojrzałe i dojrzałe na rutynowych, zabarwionych preparatach. To ulepszenie ujawniło, że mikronukleusy były znacznie bardziej skoncentrowane i bardziej dynamiczne w retikulocytach niż w starszych komórkach, dostarczając czułego i szybko zmieniającego się sygnału aktywności leku. Obrazy całych szkiełek umożliwiały też kontrolę jakości próbki — na przykład wykrywanie krwinek zdeformowanych w wyniku złego przechowywania — tak aby słabe jakościowo szkiełka mogły być odrzucone przed analizą, co jest istotnym krokiem w kierunku zastosowań klinicznych.
Co to może oznaczać dla przyszłej opieki onkologicznej
Badanie pokazuje, że tiny próbka krwi, standardowe barwienie preparatu i pipeline obrazowania wspomagany AI mogą wspólnie dostarczyć skalowalny, minimalnie inwazyjny miarę siły działania leków celujących w DNA. Choć prace prowadzone były na myszach, a erytrocyty są tylko przybliżeniem tego, co dzieje się w guzach, silne powiązanie między sygnałami mikronukleusów a odpowiedzią guza sugeruje, że podejście to może stać się praktycznym narzędziem w rozwoju leków i ostatecznie w badaniach klinicznych. Mówiąc prosto, liczenie tych mikroskopijnych „kropek” DNA we krwi może pomóc badaczom i klinicystom w dostrajaniu dawek, porównywaniu nowych leków i śledzeniu efektów terapii w czasie — bez potrzeby powtarzanych, inwazyjnych biopsji.
Cytowanie: Yong, K.H.R., Robak, W.S., Mulderrig, L. et al. Micronucleus quantification from whole-slide haematology images using AI serves as a translatable pharmacodynamic biomarker for DNA damage response inhibitors. Sci Rep 16, 11437 (2026). https://doi.org/10.1038/s41598-026-41458-7
Słowa kluczowe: mikronukleusy, erytrocyty, inhibitory PARP, patologia cyfrowa, odpowiedź na uszkodzenia DNA