Clear Sky Science · pl
Opracowanie i charakterystyka indukowalnego transgenicznego modelu mysiego z deficytem Tensin1
Dlaczego przełączanie genów u myszy ma znaczenie
Nasze organizmy opierają się na niezliczonych białkach, które pomagają komórkom przylegać do otoczenia, wyczuwać siły fizyczne i reagować na uszkodzenia. Jednym z takich białek jest Tensin1, powiązany z chorobami nerek, schorzeniami płuc i rakiem, lecz naukowcy brakowali precyzyjnego sposobu, by badać jego funkcje w tkankach dorosłych bez zakłócania rozwoju. W artykule opisano nowy typ myszy laboratoryjnej, w której Tensin1 można wyłączyć na żądanie, co pozwala badaczom obserwować, jak dorosłe narządy i komórki układu odpornościowego reagują na brak tego kluczowego białka strukturalnego.
Kontrolowany przełącznik dla „klejącego” białka komórkowego
Tensin1 znajduje się w miejscach, gdzie komórki zaczepiają się o otaczającą sieć podporową, łącząc wewnętrzne włókna komórkowe z cząsteczkami zewnątrzkomórkowymi. Aby bezpieczniej badać jego rolę, badacze zmodyfikowali myszy tak, że kluczowy fragment genu Tensin1 został otoczony specjalnymi miejscami w DNA, które można wyciąć, gdy obecne jest inne białko aktywowane przez lek tamoksyfen. Poprzez skojarzenie tych elementów uzyskali myszy, u których krótki kurs tamoksyfenu w wieku dorosłym czysto usuwa Tensin1, nie dotykając innych blisko spokrewnionych białek. Badania tkanki płuc wykazały około 95-procentowy spadek aktywności genu Tensin1 i dramatyczny zanik białka Tensin1 po leczeniu, potwierdzając, że genetyczny przełącznik działa zgodnie z planem.
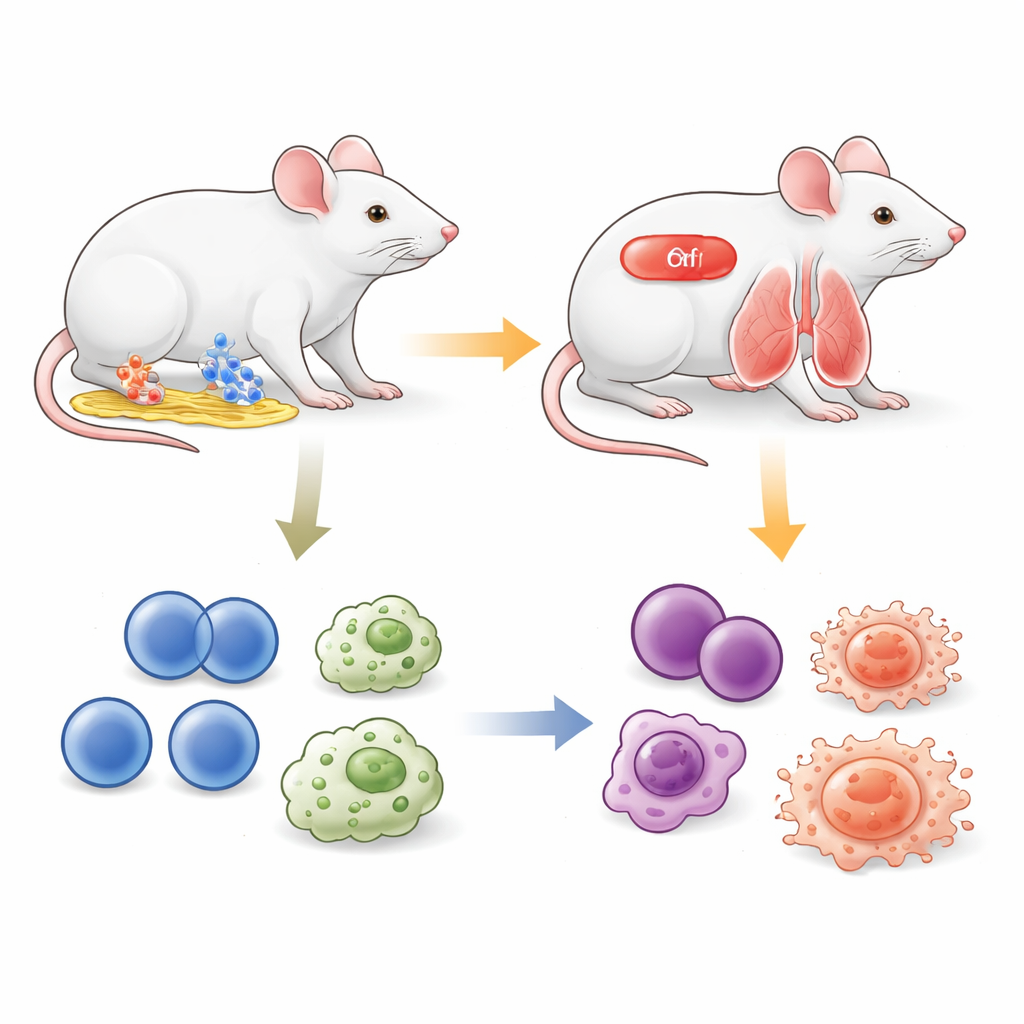
Zewnętrznie zdrowy wygląd kryje subtelne zmiany wewnętrzne
Można by oczekiwać, że usunięcie białka strukturalnego związanego z ciężkimi chorobami nerek szybko odbije się na zdrowiu zwierząt. Zaskakująco jednak indukowalnie pozbawione Tensin1 myszy pozostały widocznie zdrowe. Przed leczeniem tamoksyfenem rozmnażały się normalnie i miały wielkość miotów podobną do standardowych szczepów laboratoryjnych. Po wyłączeniu Tensin1 u dorosłych zwierzęta utrzymywały prawidłową masę ciała w porównaniu z traktowanymi kontrolami. Szczegółowe badanie głównych narządów, takich jak serce, wątroba, śledziona, płuca i nerki w ciągu roku wykazało jedynie łagodne, rozproszone zmiany widoczne zarówno u myszy normalnych, jak i pozbawionych Tensin1. Wiele z tych ustaleń, w tym miejscowe zapalenie w jamie brzusznej i pogrubienie błony śluzowej macicy, odpowiadało znanym skutkom ubocznym samego tamoksyfenu, a nie utracie Tensin1. Badania krwi również nie wykazały wyraźnych różnic w liczbie komórek ani markerach funkcji wątroby i nerek, które można by przypisać wyłączeniu genu.
Niespodziewany sygnał od komórek odpornościowych płuc
Choć myszy wyglądały na zdrowe, badacze przypuszczali, że mogą zachodzić subtelne zmiany molekularne, szczególnie w płucach, gdzie wiadomo, że Tensin1 wpływa na komórki tworzące blizny. Zmierzyli aktywność genów w całych płucach i znaleźli 171 genów, które zostały włączone lub wyłączone po utracie Tensin1. Analiza szlaków wskazała, że wiele z tych genów odnosiło się nie tyle do strukturalnego wsparcia płuca, ile do układu odpornościowego. Zestawy genów związanych z odpowiedziami na infekcje, rozwojem komórek odpornościowych i komunikacją między nimi były silnie zmienione. Jedna duża grupa genów, głównie zmniejszonych, była powiązana z komórkami mieloidalnymi — komórkami odpornościowymi takimi jak monocyty i makrofagi, które patrolują tkanki i pochłaniają pozostałości lub drobnoustroje. Natomiast mniejszy klaster genów o zwiększonej ekspresji nosił sygnaturę komórek B, czyli limfocytów produkujących przeciwciała.
Jak Tensin1 kształtuje zachowanie komórek odpornościowych
Aby lepiej zrozumieć znaczenie tych sygnatur, zespół sięgnął po ludzką linię komórkową naśladującą monocyty i makrofagi. Gdy zastosowali małe cząsteczki RNA do wyciszenia Tensin1 w tych komórkach, stały się one mniejsze i mniej rozpostarte na powierzchniach pokrytych fibryonektyną, głównym białkiem podporowym. Obrazowanie na żywo wykazało, że komórki pozbawione Tensin1 poruszały się na krótsze odległości, co sugeruje upośledzoną migrację. W teście fagocytozy, w którym komórki miały pochłonąć świecące cząstki, komórki bez Tensin1 pochłaniały mniej cząstek niż komórki kontrolne. Razem wyniki te wskazują, że Tensin1 pomaga komórkom mieloidalnym utrzymywać kształt, sprawnie poruszać się po powierzchniach tkankowych i pełnić funkcję sprzątającą. U żywych myszy płyn zmywany z dróg oddechowych krótko po wyłączeniu Tensin1 wykazywał tendencję do większej liczby limfocytów, zgodnie ze zmianami genów związanych z komórkami B obserwowanymi w tkance płucnej.
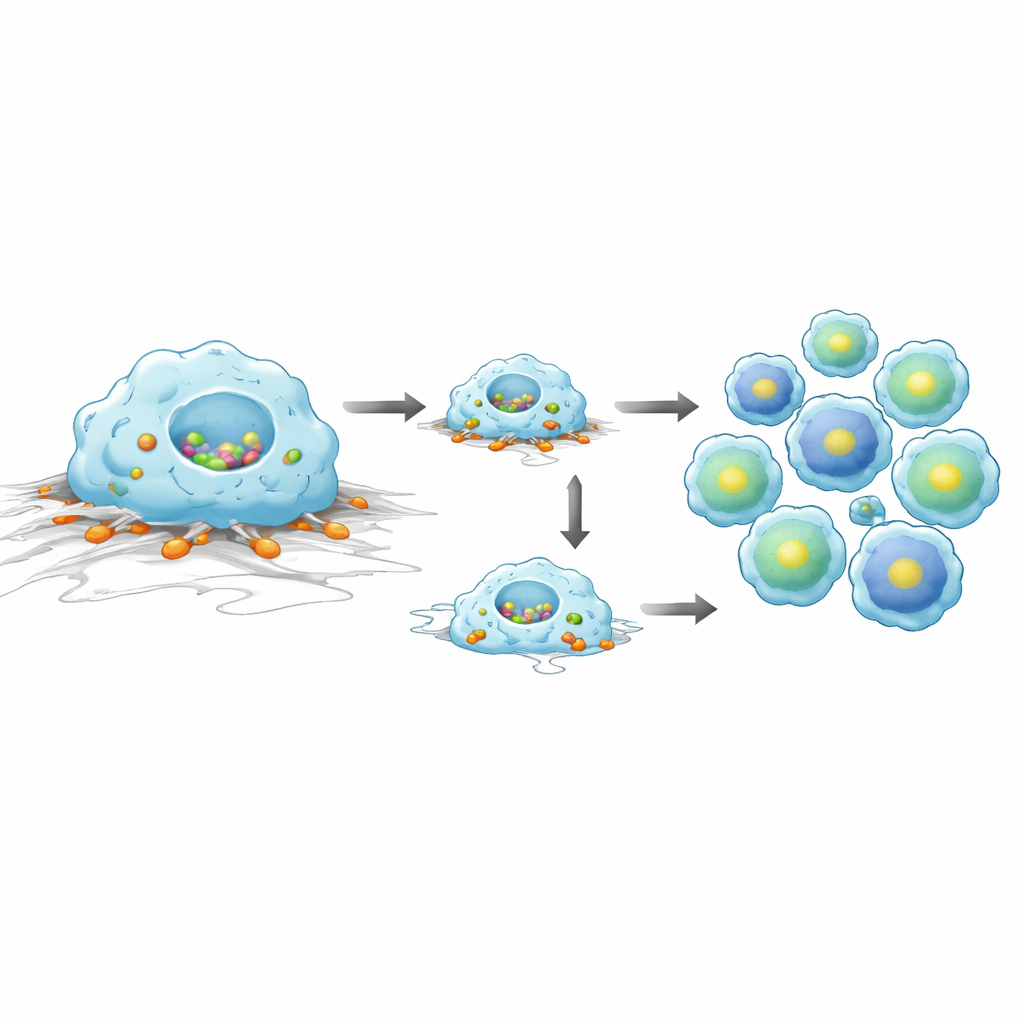
Co to oznacza dla przyszłych badań nad chorobami
Mówiąc prosto, badanie pokazuje, że usunięcie Tensin1 u dorosłych myszy nie powoduje dramatycznego uszkodzenia narządów życiowych, ale cicho przestawia aktywność odpornościową w płucach, osłabiając sygnaturę komórek patrolujących oczyszczanie i wzmacniając sygnaturę komórek związanych z przeciwciałami. Nowy model myszy działa jak ściemniacz, który może wyłączyć Tensin1 w wybranym czasie i w wybranych typach komórek, bez problemów rozwojowych występujących, gdy gen jest nieobecny od urodzenia. To narzędzie pozwoli badaczom badać, jak Tensin1 kształtuje odpowiedzi na uszkodzenia płuc, infekcje i włóknienie, i ostatecznie może wyjaśnić, dlaczego zmiany genetyczne w Tensin1 wiążą się z chorobami płuc i rakiem u ludzi.
Cytowanie: Bernau, K., Holbert, K., McDermott, I.S. et al. Development and characterization of an inducible Tensin1 deficient transgenic murine model. Sci Rep 16, 8639 (2026). https://doi.org/10.1038/s41598-026-41319-3
Słowa kluczowe: Tensin1, transgeniczny model myszy, odporność płuc, funkcja makrofagów, warunkowe wyciszenie genu