Clear Sky Science · pl
Potencjalny korzystny efekt gonadalny sitagliptyny przeciwko uszkodzeniom jąder wywołanym przez paklitaksel poprzez pośredniczenie w szlaku sygnalizacji PERK/CHOP/NLRP3/Sestrin2
Dlaczego to badanie ma znaczenie dla pacjentów onkologicznych
Chemioterapia ratuje życie, ale może dyskretnie uszkadzać płodność, zwłaszcza u mężczyzn. Jeden z powszechnie stosowanych leków przeciwnowotworowych, paklitaksel, jest znany z działania toksycznego na jądra i pogarszania jakości nasienia. Badanie na szczurach stawia praktyczne pytanie o jasnym znaczeniu dla ludzi: czy już zarejestrowany lek na cukrzycę, sitagliptyna, można ponownie wykorzystać, by chronić męski układ rozrodczy przed skutkami ubocznymi paklitakselu, nie osłabiając jego działania przeciwnowotworowego?
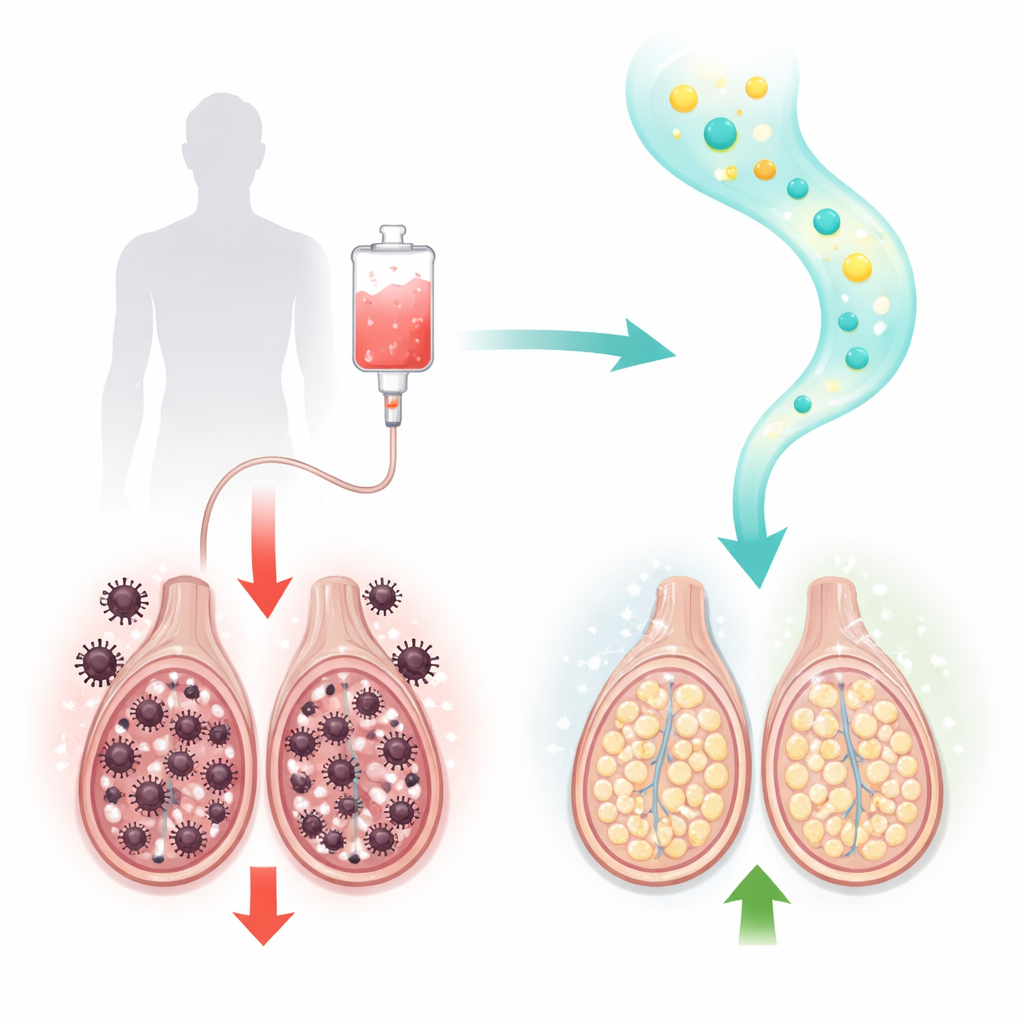
Popularny lek przeciwnowotworowy z ukrytym kosztem
Paklitaksel jest podstawowym lekiem w terapii raka piersi, jajnika, płuca i innych guzów litych. Działa przez blokowanie mechanizmów podziału komórkowego w szybko dzielących się komórkach nowotworowych. Niestety, również dzielące się komórki zdrowych tkanek są narażone. U samców szczurów leczenie paklitakselem prowadziło do typowych objawów uszkodzenia jąder: liczba plemników, ich ruchliwość i żywotność gwałtownie spadły, a odsetek plemników o nieprawidłowym kształcie wzrósł. Pod mikroskopem badacze zaobserwowali uszkodzone kanaliki nasienne (gdzie powstają plemniki) i uszkodzone komórki Leydiga produkujące hormony, wraz ze skurczem warstw tkankowych. Badania krwi potwierdziły istotne obniżenie testosteronu i kluczowego enzymu do jego syntezy, 17β‑hydroksysteroid dehydrogenazy.
Lek przeciwcukrzycowy jako nieoczekiwany ochroniarz
Sitagliptyna jest szeroko przepisywana w celu kontroli poziomu glukozy u osób z cukrzycą typu 2. Wcześniejsze prace sugerowały, że poza działaniem metabolicznym sitagliptyna może łagodzić szkodliwy stres oksydacyjny, zapalenie i śmierć komórek w narządach takich jak wątroba, nerki czy mózg. W oparciu o to badacze podzielili samce szczurów na cztery grupy: kontrolną bez leczenia, grupę otrzymującą jedynie paklitaksel oraz dwie grupy, które otrzymywały paklitaksel wraz z mniejszą lub większą dawką sitagliptyny przez dwa tygodnie. Następnie porównano jakość nasienia, poziomy hormonów, strukturę tkanek oraz zestaw molekularnych „systemów alarmowych” w jądrach, które wykrywają stres i uruchamiają zapalenie oraz apoptozę.
Jak sitagliptyna złagodziła stres komórkowy i zapalenie
Paklitaksel wprowadził jądra w stan stresu oksydacyjnego i wewnątrzkomórkowego: wzrosły poziomy szkodliwych produktów ubocznych (mierzone jako malondialdehyd), podczas gdy naturalne mechanizmy obronne, takie jak zredukowany glutation i enzym katalaza, zmalały. W głębi komórek siłownia fałdowania białek, czyli retikulum endoplazmatyczne, uruchomiła ścieżkę niebezpieczeństwa nazwaną PERK–CHOP, sygnał, że przedłużający się stres popycha komórki w kierunku śmierci. Równocześnie bardzo aktywny stał się zapalny kompleks białkowy NLRP3, zwiększając poziomy mediatorów zapalnych, takich jak interleukina‑1β, oraz aktywując kaskadę białek śmierci komórkowej, w tym cytochromu c i kaspazy‑3. Sitagliptyna odwróciła wiele z tych zmian. Obie dawki zmniejszyły uszkodzenia oksydacyjne i przywróciły mechanizmy antyoksydacyjne. Znacząco obniżyły aktywację szlaku stresowego PERK–CHOP oraz ograniczyły zapalenie i apoptozę napędzane przez NLRP3. Białko ochronne Sestrin2, które pomaga usuwać reaktywne cząsteczki i wiązane jest ze zdrowszym nasieniem, zostało wzmocnione przez sitagliptynę zarówno na poziomie genu, jak i białka.
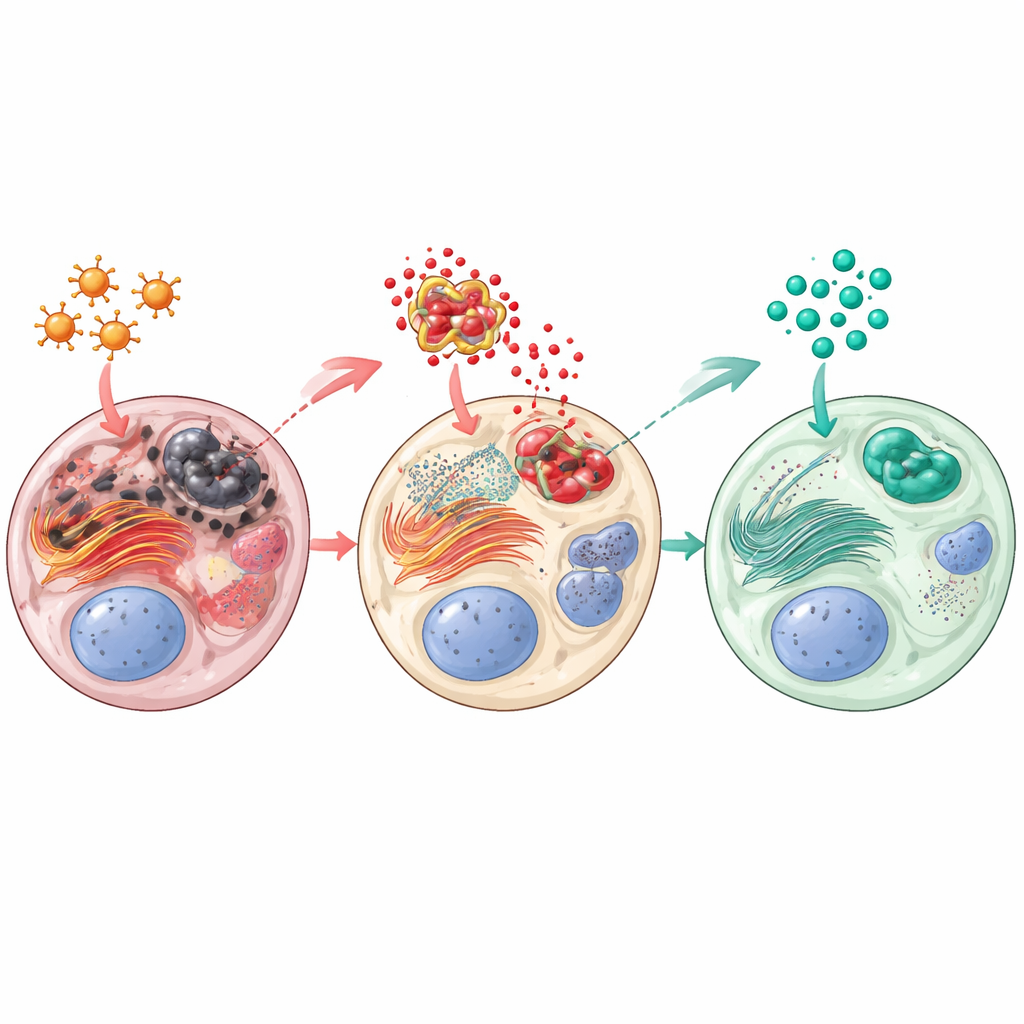
Lepsze nasienie, zdrowsza tkanka, silniejsze hormony
Poprawy biochemiczne przełożyły się na wymierne korzyści funkcjonalne. Szczury otrzymujące sitagliptynę po paklitakselu miały większą liczbę plemników, lepszą ruchliwość i mniej nieprawidłowych plemników niż zwierzęta leczone samym paklitakselem, przy czym wyższa dawka sitagliptyny zbliżała wyniki do normy. Testosterone i 17β‑hydroksysteroid dehydrogenaza odbudowały się, co sugeruje regenerację produkcji hormonów steroidowych przez komórki Leydiga. W mikroskopii świetlnej i elektronowej jądra leczone sitagliptyną wykazywały bardziej uporządkowane kanaliki nasienne, więcej komórek Leydiga, grubsze i zdrowsze warstwy komórkowe oraz mniej zniekształceń strukturalnych. Ogólnie lek pomógł zachować architekturę i funkcję niezbędne do ciągłej produkcji plemników.
Co to może oznaczać dla mężczyzn poddawanych chemioterapii
To badanie na zwierzętach sugeruje, że sitagliptyna może istotnie złagodzić uszkodzenia jąder wywołane paklitakselem przez wyciszenie sieci szkodliwych sygnałów — stresu oksydacyjnego, wewnętrznego stresu fałdowania białek, zapalenia i zaprogramowanej śmierci komórek — głównie poprzez zwiększenie Sestrin2 i stłumienie osi PERK/CHOP/NLRP3. Ponieważ sitagliptyna jest już stosowana klinicznie w cukrzycy, wyróżnia się jako realistyczny kandydat do przetestowania jako dodatek chroniący płodność u mężczyzn otrzymujących paklitaksel, szczególnie u osób z cukrzycą. Autorzy podkreślają, że potrzebne są badania u ludzi, ale ich wyniki dają nadzieję: znana tabletka mogłaby kiedyś pomóc pacjentom onkologicznym zachować nie tylko życie, lecz także szanse na ojcostwo.
Cytowanie: El-Beheiry, K.M., El-Shitany, N.A., El-Sayad, M.ES. et al. Potential gonadal-beneficial effect of sitagliptin against paclitaxel-induced testicular dysfunction via mediating PERK/CHOP/NLRP3/Sestrin2 signaling pathway. Sci Rep 16, 9090 (2026). https://doi.org/10.1038/s41598-026-40511-9
Słowa kluczowe: paklitaksel, sitagliptyna, płodność męska, stres oksydacyjny, toksyczność jądrowa