Clear Sky Science · pl
Zakłócenie homeostazy neutrofili wiąże się ze zmianami funkcji mitochondriów u krytycznie chorych pacjentów z COVID-19
Dlaczego to ma znaczenie dla pacjentów z COVID-19
Większość osób wie już, że COVID-19 to coś więcej niż zapalenie płuc, jednak dokładne mechanizmy, dzięki którym wirus przewraca obronę organizmu przeciwko niemu, wciąż są odkrywane. To badanie przygląda się neutrofilom — powszechnemu rodzajowi białych krwinek — u pacjentów z zagrażającym życiu COVID-19 na oddziale intensywnej terapii. Analizując, jak te komórki żyją, umierają i korzystają ze swoich małych „elektrowni” (mitochondriów), badacze opisują obraz uporczywych, nadaktywowanych neutrofili, które mogą tłumaczyć utrzymujące się zapalenie, uszkodzenia krwi i narządów w przebiegu ciężkiej choroby.
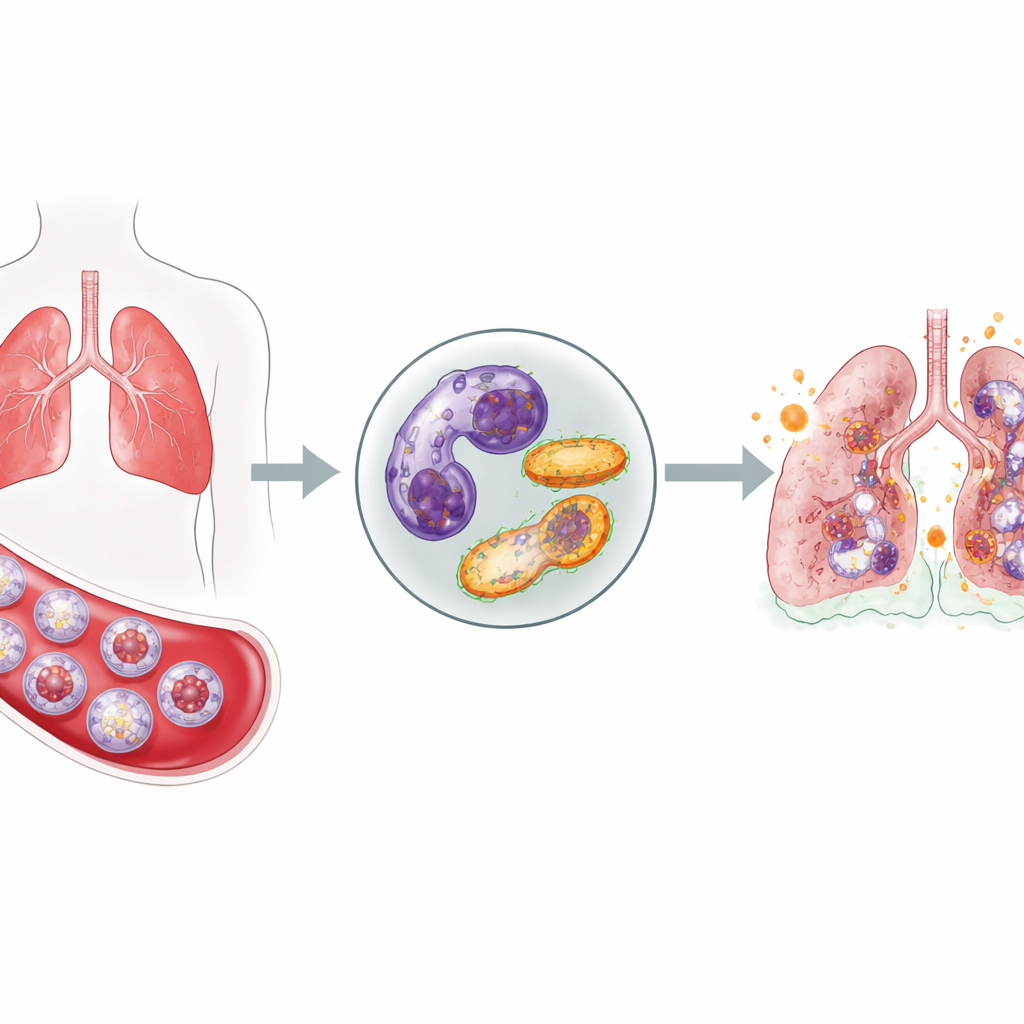
Komórki pierwszej linii, które nie ustępują
Neutrofile należą do pierwszych komórek reagujących na zakażenie: szybko pojawiają się w krwiobiegu, przemieszczają się do tkanek i wydzielają toksyczne związki, by zabić najeźdźców. Zwykle po wykonaniu zadania podlegają kontrolowanej autodestukcji i są usuwane, co zapobiega uszkodzeniu zdrowych tkanek. U krytycznie chorych pacjentów z COVID-19 zespół zaobserwował zupełnie inny obraz. W porównaniu ze zdrowymi ochotnikami pacjenci mieli napływ neutrofili do krwi, a co ważne — wiele z nich to komórki niedojrzałe, przyspieszenie wysłane z szpiku. Jednocześnie liczne testy wykazały, że mniej neutrofili podlegało normalnej zaprogramowanej śmierci, co sugeruje, że te agresywne komórki utrzymują się dłużej, niż powinny.
Subtelne sygnały genetyczne, ale wyraźny wzorzec przeżycia
Badacze przyjrzeli się także małym regulatorowym cząsteczkom zwanym mikroRNA w neutrofilach od osób, które przeżyły pobyt na intensywnej terapii, i od tych, które zmarły. Niektóre z tych cząsteczek były zmienione w sposób, który teoretycznie wskazuje na zaburzenia szlaków kontrolujących śmierć komórkową i równowagę wapnia. Jednak przy pomiarze bezpośrednich markerów śmierci komórkowej nie stwierdzono istotnych różnic między ocalałymi a zmarłymi — obie grupy wykazywały podobnie zmniejszoną autodestrukcję neutrofili w porównaniu ze zdrowymi osobami. Oznacza to, że wzorce mikroRNA są raczej wskazówkami do dalszych badań niż pewnymi prognostykami przebiegu choroby i podkreślają, że ogólna niezdolność neutrofili do wyłączenia się jest wspólną cechą ciężkiego COVID-19.
Przemieszczenia wapnia i przeładowane „elektrownie”
Aby zrozumieć, dlaczego neutrofile nie ginęły na czas, zespół skupił się na dwóch powiązanych systemach w komórkach: sygnałach wapniowych i mitochondriach. Jony wapnia działają jak maleńkie wyłączniki dla wielu decyzji komórkowych, w tym kiedy następuje autodestrukcja. Badacze stwierdzili, że neutrofile od pacjentów z ciężkim COVID-19 miały mniej wolnego wapnia wewnątrzkomórkowego, wraz z obniżonym poziomem kluczowych białek, które normalnie pomagają przenosić wapń do mitochondriów i otwierają zawór bezpieczeństwa uruchamiający śmierć komórkową. Jednocześnie same mitochondria były nadzwyczaj „naładowane”, z wyższym gradientem elektrycznym przez ich błony i zwiększonym zużyciem tlenu, szczególnie przez jeden główny szlak oddechowy. Zamiast wyłączać się, te nadaktywne mitochondria produkowały więcej reaktywnych form tlenu, które mogą uszkadzać otaczające tkanki i podsycać zapalenie.
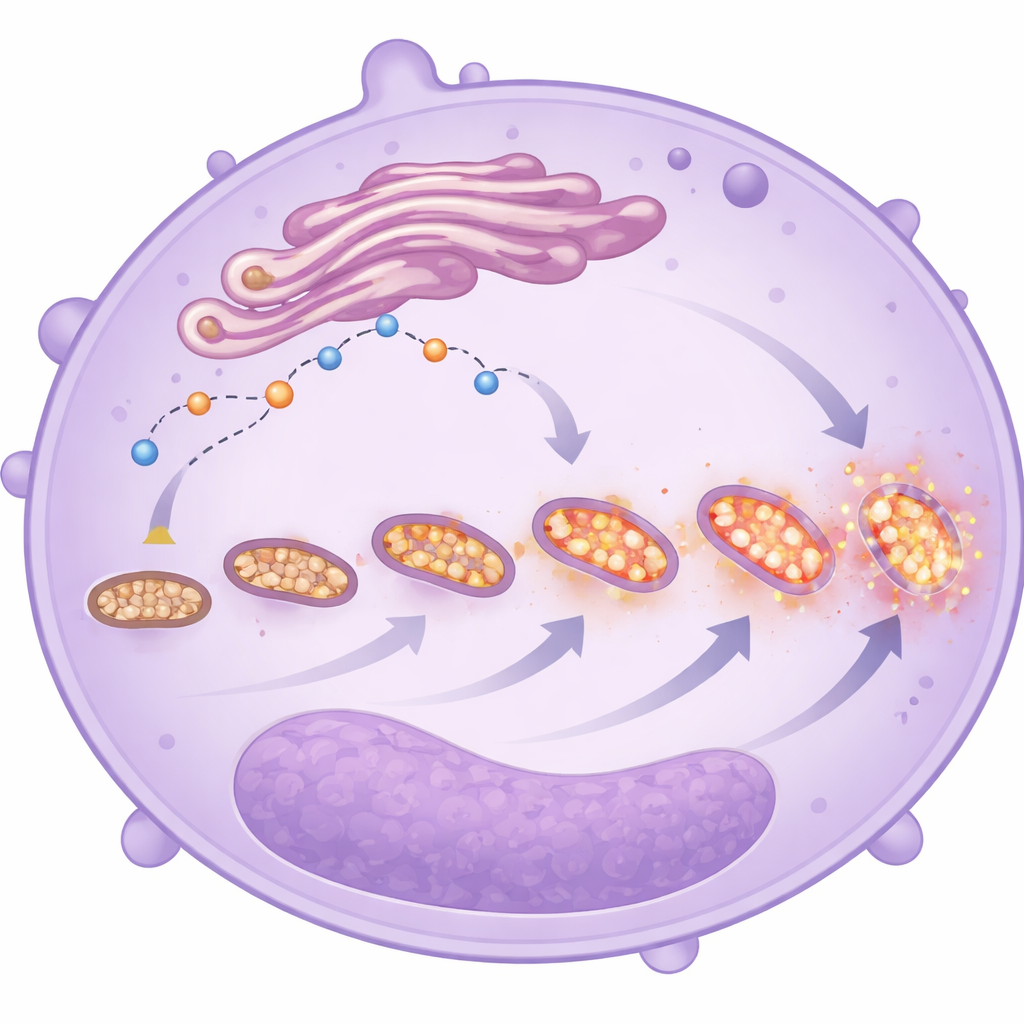
Stresujące i fragmentowane mitochondria
Obrazy uzyskane za pomocą mikroskopu elektronowego i barwniki fluorescencyjne ukazały bliżej kształt i zachowanie tych mitochondriów. W neutrofilach od najbardziej chorych pacjentów mitochondria były liczniejsze, lecz mniejsze i bardziej pofragmentowane — cechy często świadczące o stresie. Te komórki również wykazywały wyższe poziomy mitochondrialnych reaktywnych form tlenu, niezależnie od tego, czy pacjent ostatecznie przeżył. W połączeniu ze zmienioną gospodarką wapniową i opóźnioną śmiercią komórkową zmiany te rysują obraz neutrofili, które zmieniły swoją strategię energetyczną: zamiast opierać się głównie na prostym rozkładzie cukru, polegają bardziej na metabolizmie mitochondrialnym, szczególnie w komórkach niedojrzałych. Ta zamiana może zwiększać ich zdolność do migracji, przetrwania i uwalniania szkodliwych związków w płucach i innych narządach, chociaż badanie nie dowodzi, że są one bezpośrednią przyczyną gorszych wyników.
Co to może oznaczać dla przyszłej opieki
Mówiąc wprost, badanie sugeruje, że w krytycznym COVID-19 neutrofile stają się zbyt liczne, zbyt młode i zbyt trudne do wyłączenia. Ich wewnętrzne sygnały wapniowe i mitochondria są przeprogramowane w sposób, który utrzymuje je przy życiu i wysoce aktywne, produkując wybuchy szkodliwych związków na bazie tlenu. Choć praca ma charakter obserwacyjny i nie wykazuje związku przyczynowo-skutkowego, uwypukla kilka potencjalnych „pokręteł kontrolnych” w tych komórkach — takich jak regulatory wapnia i punkty kontrolne mitochondriów — które mogłyby kiedyś zostać skierowane, by delikatnie nakłonić neutrofile do powrotu do normalnego zachowania. Jeśli przyszłe badania potwierdzą te pomysły, terapie przywracające właściwe wyłączanie neutrofili lub łagodzące ich przeładowane mitochondria mogłyby ograniczyć szkody wtórne spowodowane przez te kluczowe komórki podczas ciężkiego COVID-19, a być może także w innych ciężkich chorobach.
Cytowanie: Elkhodiry, A.A., Yasseen, B.A., El-sayed, H. et al. Disruption of neutrophil homeostasis is associated with functional alterations in mitochondria of critically ill COVID−19 patients. Sci Rep 16, 7838 (2026). https://doi.org/10.1038/s41598-026-38741-y
Słowa kluczowe: COVID-19, neutrofile, mitochondria, zapalnie, ciężka choroba